酸碱盐的溶解性 知识点题库
如表是部分碱、酸、盐的溶解性表(20℃)中的一部分,据此判断下列有关①处物质的说法错误的是( )


 加热一定质量的氯酸钾固体
B .
加热一定质量的氯酸钾固体
B .  向pH=3的溶液中加水
C .
向pH=3的溶液中加水
C .  向一定质量二氧化锰中加入过氧化氢溶液
D .
向一定质量二氧化锰中加入过氧化氢溶液
D .  向一定量氯化钙溶液中加入碳酸钠溶液
向一定量氯化钙溶液中加入碳酸钠溶液
 H2O
H2O  H2CO3
B . Ag
H2CO3
B . Ag  AgCl
AgCl  AgNO3溶液
C . Ca(OH)2溶液
AgNO3溶液
C . Ca(OH)2溶液  Ca(NO3)2溶液
Ca(NO3)2溶液  CaCO3
D . NaCl
CaCO3
D . NaCl  NaHCO3
NaHCO3  Na2SO4溶液
Na2SO4溶液

-
(1) C的化学式为;
-
(2) 写出下列反应的化学方程式:A转化D为,F转化B为;
-
(3) A在工业上用途是。(至少填两种)
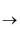 ”表示物质间存在转化关系,图中部分反应物、生成物和反应条件已略去。
”表示物质间存在转化关系,图中部分反应物、生成物和反应条件已略去。 
请回答:
-
(1) 写出下列物质的化学式:A;
-
(2) 写出反应的化学反应方程式
①, ②;
-
(3) 写出G+F→I的化学反应方程式,基本反应类型属于反应。
-
(4) 关于气体H:若H可以供给呼吸,则自然界中可通过来实现C
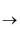 H的转化;若H为一种有毒气体,常用于工业炼铁,请写出一个工业炼铁原理的化学方程式。
H的转化;若H为一种有毒气体,常用于工业炼铁,请写出一个工业炼铁原理的化学方程式。
-
(1) 通过晾晒海水,可以蒸发除去水分,得到粗盐。通常不采用降低海水温度的方法得到粗盐,是因为,相同情况下降温析出的晶体比较少。
-
(2) 根据“粗盐中难溶性杂质的去除”实验,回答有关问题。
①溶解 称取5.0g粗盐,逐渐加入10mL水中,直到不再溶解,剩余粗盐1.1g。
②过滤
③蒸发 在加热过程中,用玻璃棒不断搅拌,防止。当蒸发皿中,停止加热。
④计算产率 得到精盐3.3g,则精盐的产率为(计算结果保留一位小数)。
-
(3) 若经过上述实验得到的精盐中还含有氯化镁、氯化钙,为了除去这两种可溶性杂质,可将得到的精盐全部溶于水,加入过量的氢氧化钠溶液和溶液,充分反应后,接下来的操作顺序是(填序号)。
①蒸发 ②加入过量的稀盐酸 ③过滤
-
(1) 若以上操作的顺序为①②⑤③④,则操作⑤中发生的复分解反应有个。
-
(2) 写出加入过量BaCl2溶液时发生反应的化学方程式。
-
(3) 最后加入适量稀盐酸前溶液中的溶质是什么?(填化学式)
| 选项 | 实验目的 | 实验方案 |
| A | 检验二氧化碳气体 | 用燃着的木条伸入集气瓶内,观察火焰是否熄灭 |
| B | 除去CO2中少量的CO | 通入氧气后点燃 |
| C | 分离MgCl2、NaCl固体混合物 | 依次加入水和适量Ca(OH)2溶液,过滤后向沉淀中加入适量盐酸,再蒸发两种溶液得到固体 |
| D | 鉴别CaCO3、NaCl、NaOH、CuSO4四种固体 | 分别取少量固体于试管中加入适量水,观察现象 |
 右下图为模拟和气处理并得到轻质
右下图为模拟和气处理并得到轻质  的主要流程。下列说法正确的是()
的主要流程。下列说法正确的是() 
 B . 净化时反应的化学方程式:
B . 净化时反应的化学方程式:  C . 沉淀时应先通入
C . 沉淀时应先通入  后,再通入
后,再通入  ,有利于
,有利于  的生成
D . 由沉淀池中发生的反应可知,溶解性:
的生成
D . 由沉淀池中发生的反应可知,溶解性: 
|
OH- |
NO3 |
Cl |
SO42- |
CO32- |
|
|
H+ |
溶、挥 |
溶、挥 |
溶 |
溶、挥 |
|
|
Na+ |
溶 |
溶 |
溶 |
溶 |
溶 |
|
Ca2- |
微 |
溶 |
溶 |
微 |
不 |
|
Ba2+ |
溶 |
溶 |
溶 |
不 |
不 |
|
Cu2+ |
不 |
溶 |
溶 |
溶 |
不 |
请依据上表,按按要求回答下列问题:
-
(1) BaSO4的溶解性为;
-
(2) 写出一种挥发性酸的化学式;
-
(3) 氧化钙溶液与硝酸钠溶液(填“能”或“不能”)发生反应,理由是;
-
(4) 请写出一个盐能与NaOH反应的化学方程式.
-
(1) NaOH溶液和稀硫酸反应,向滴有酚酞的NaOH溶液中加入稀硫酸,现象为,反应的化学方程式为。
-
(2) 为除去NaCl中混有的少量Na2SO4 , 某探究小组设计了如图所示方案进行实验。

①Ⅰ、Ⅱ两步都有过滤操作,过滤中要用到的玻璃仪器有烧杯、和。
②甲、乙同学选用的X分别为BaCl2溶液、Ba(OH)2溶液。写出Ⅰ、Ⅱ两步中发生的任意一个反应的化学方程式:。甲、乙同学的实验中,可能发生的相同反应的化学方程式为。乙的实验中,步骤Ⅲ涉及的操作和现象是。
③丙同学认为甲的实验比乙的实验更合理,理由是。
阴离子 阳离子 | OH﹣ |
| Cl﹣ |
|
|
K+ | 乙 | 丁 | 戊 | ||
Ba2+ | 甲 | 丙 |
-
(1) 探究活动一:认识工具
认识符号:NO
 的名称是;
的名称是; -
(2) 物质分类:五种物质中,属于碱的是(用化学式表示);
-
(3) 溶解能力:五种物质中,只有一种不溶于水,它是(用化学式表示);
-
(4) 相互反应:五种物质中,有两种物质在溶液中能相互反应,其化学方程式为。
-
(5) 探究活动二:运用工具
已知某氯化钠样品中,含有不溶性杂质(泥沙)和可溶性杂质(氯化镁、氯化钙)。为了得到纯净的氯化钠,某实验小组设计了下列实验方案,请你完成相关问题:

在上述实验方案中,操作Ⅰ、操作Ⅱ、操作Ⅲ都是将固体和溶液分离,该操作的名称是,在实验室中进行该操作用到的玻璃仪器有漏斗、烧杯、。
-
(6) 固体乙是,溶液B中的溶质有。(都用化学式表示)
-
(7) 通过上述设计可以看出,除去氯化钠中的可溶性杂质,实质上就是加入试剂把溶液中的(填离子符号)转化为难溶于水的物质,再进行分离而除去,在溶液C中加入适量的稀酸X是为了,写出其中一个反应的化学方程式。
- 某天股票A开盘价为12元,上午12:00跌1.0元,下午收盘时又涨了0.2元,则股票A的收盘价是( )A.0.2元B.
- 小明、小华到某电脑销售公司参加社会实践活动,了解到2011年该公司销售的甲、乙两种品牌电脑在第一季度三个月(即一、二、三
- 下列变化中,必须加入氧化剂才能发生的是( )A. SO2→S B.Na2O2→O2 C.
- 阅读下面一段文言文,完成下题: 李忠字仲都,东莱黄人也。父为高密都尉。忠元始中以父任为郎,署中数十人,而忠独以好礼修整称
- 下列不能做组织培养材料的是( )。 A叶片 B茎尖 C花粉 D导管
- 已知1个C-12原子的质量为akg,则实际质量为bkg的另一种原子的相对原子质量为( ) A.12b/a kgB.
- 已知 IO3-+5I-+6H+===3I2+3H2O,为证明加碘食盐中含有KIO3,可供选用的物质有:①水 ②蓝色石蕊试
- 如图所示,小球P在A点从静止开始沿光滑的斜面AB运动到B点所用的时间为t1,在A点以一定的初速度水平向右抛出,恰好落在B
- 已知动圆M与圆C1:(x+4)2+y2=2外切,与圆C2:(x-4)2+y2=2内切,则动圆圆心M的轨迹方程是() A.
- ___is it ____has made Peter___ he is today? A. What; that;
- 下列是当涂县部分特产食物,其中主要用来为人体提供糖类的是………………【 】
- 用a、b两束单色光分别照射同一双缝干涉装置,在距双缝恒定距离的屏上得到图示的干涉图样,其中甲图是a光照射时形成的,乙图是
- Ⅰ.某溶液中可能含有H+、Na+、、Mg2+、Fe3+、Al3+、等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生
- —Mum, may Iwatch TV now?—No, you _____ finishyour homework f
- (1)在图中作出物体AB所成的像。要体现作图过程(3分)(2)完成图中的光路图。(2分)(3)完成图中的光路图。(2分)
- I wonder _______ he is arguing with and _______they are argu
- 下列不属于亚洲的人类文明发祥地( )A.尼罗河流域B.两河流域C.黄河-长江流域D.印度河流域
- 下图为我国西北地区地区年降水量分布图。2019年起,在新疆塔里木河流域实施胡杨林拯救行动,主要保护塔里木河干流和叶尔羌河
- 17.下列各句中,加点的成语使用不恰当的两项是( )( )(4分) A.现代人在饮食上注重健康养生,曾经是
- Societies all over the world name places insimilar ways. Qui