含杂质物质的化学反应的有关计算 知识点题库
(1)下列用品中,主要利用金属导电性的是 (填字母).
A.铂金饰品 B.铁锅 C.铝导线
(2)为了验证铝、铜、银三种金属的活动性顺序,设计了下列四种方案,其中可行的是 (填序号).①将铝、银分别浸入到硫酸铜溶液中 ②将银分别浸入到硫酸铝、硫酸铜溶液中③将铜、银分别浸入到硫酸铝溶液中 ④将铜分别浸入到硫酸铝、硝酸银溶液中
(3)在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,得到滤渣和滤液.①滤液中一定含有的溶质是 (填化学式);②向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是 (填化学式).
(4)某钢铁厂每天需消耗4900t含Fe2O3 76%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁的质量是 t.

-
(1) 上述物质中属于铁合金的是 .
-
(2) 过程②在炼铁炉中进行.首先焦炭(C)在空气中完全燃烧,得到的产物再与灼热的焦炭反应生成一氧化碳,一氧化碳继续与磁铁矿(Fe3O4)反应得到金属铁.分别写出生成一氧化碳、金属铁的化学方程式: 、 .
-
(3) 为了节约资源,降低成本,防止大气污染,可将炉气(含有大量的碳氧化物、氮气和烟尘等)通过分离得到可循环使用的物质是 .
-
(4) 冶炼29t含四氧化三铁80%的磁铁矿,能得到含杂质2%的生铁的质量是 t(计算结果精确到0.1).
-
(1) 下列用品中,主要利用金属导电性的是 (填字母).A . 铂金饰品 B . 铝壶 C . 铜导线
-
(2) 铁生锈实际上是铁与空气中的氧气和(填名称)发生反应的结果,生活中可以采用(写一种方法即可)的方法防止铁器生锈,铝比铁活泼,但铝却不易腐蚀,原因是(用化学方程式表示).
-
(3) 在氯化铜和氯化亚铁的混合溶液中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液.
①滤液中一定含有的溶质是(填化学式);
②向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是(填化学式).
-
(4) 某钢铁厂每天需消耗4000t含氧化铁80%的赤铁矿石,该厂理论上可日产含铁98%的生铁的质量是;(计算结果精确到0.1).

-
(1) 乙装置的作用是.
-
(2) 丙装置中反应的化学方程式是.
-
(3) 丁装置中的现象是.
-
(4) 戊装置的作用是.
-
(5) 要生产1000t含杂质3%的生铁,需要含Fe2O390%的铁矿石 t(保留整数).
-
(1) 生铁和刚都是铁合金,它们中含碳量较少的是;
-
(2) 铁生锈是铁与空气中的共同发生的复杂的化学反应;
-
(3) 写出高温下,用一氧化碳和赤铁矿(主要成分是Fe2O3)冶炼生铁的化学方程式;
-
(4) 工业上用含Fe2O380%赤铁矿石100t,理论上最多得到纯铁的质量是 t.
【查阅资料】(1)4FeS2+11O2  8SO2+2Fe2O3(2)亚硫酸钠与过氧化氢反应生成硫酸钠和水。
8SO2+2Fe2O3(2)亚硫酸钠与过氧化氢反应生成硫酸钠和水。
【设计方案】甲、乙二个实验小组均设计了下列装置,称取了m1 g黄铁矿样品,将样品放入如下图所示的硬质粗玻璃管中,从a处不断地缓缓通入空气,高温灼烧玻璃管中的黄铁矿样品至反应完全。(假设每步反应均完全,不考虑装置内原有空气对测定结果的影响)

甲组同学仅称量了上述实验所需要的相关装置质量后即完成了测定。
乙组同学则在上述反应结束后,将C瓶中的溶液进行了如下图处理:

【实验分析及数据处理】
-
(1) 上述装置中A瓶内所盛的试剂最好是溶液,其作用是。
-
(2) A、B装置不能对调位置,原因是。
-
(3) C瓶中发生反应的化学方程式为。
-
(4) 甲组同学应称量的数据是(填编号)。
①反应前C装置及其中物质总质量m2 g
②反应前C、D装置及其中物质总质量m3 g
③反应后C装置及其中物质总质量m4 g
④反应后C、D装置及其中物质总质量m5 g
-
(5) 根据(4)中所选数据,甲组同学测得的该黄铁矿中硫元素的质量分数的表达式为。
-
(6) 乙组实验中,检验所加BaCl2溶液是否过量的方法是,若实验过程中未洗涤滤渣就直接烘干称量,则会使测定结果(填“偏大、偏小或不变”),检验滤渣是否洗净所用试剂是溶液。
-
(1) 海水含有等物质(填一种),举例说明物质的用途。
-
(2) 2017年5月我国成功开采海底“可燃冰”, “可燃冰”是甲烷(CH4)和水形成的一种水合物,试写出甲烷完全燃烧的化学方程式。
-
(3) 我国曾在南海整体打捞“南海一号”古商船,在发现的文物中,真金制品完好无损,铜器锈迹斑斑,铁制品锈蚀非常严重,据此判断金、铜、铁三种金属的活动性由强到弱的顺序是;写出生活中防止铁生锈的方法 (答一点即可)。
-
(4) 我国古代已经掌握用焦炭和铁矿石炼铁的反应。公元1世纪,从丝绸之路运到欧洲的铁制品非常受欢迎。写出焦炭和氧化铁反应的化学方程式;焦炭在其中的性质为;某炼铁厂用1000吨含氧化铁80%的赤铁矿石,可以提炼出含杂质4%的生铁的质量为吨。(保留一位小数)
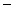 铜合金中铜的质量分数,进行如下实验:取合金样品10克放入烧杯中,将60克稀硫酸分三次加入,充分反应后,测得生成气体的质量如下:
铜合金中铜的质量分数,进行如下实验:取合金样品10克放入烧杯中,将60克稀硫酸分三次加入,充分反应后,测得生成气体的质量如下: | 实验次数 | 第一次 | 第二次 | 第三次 |
| 加入稀硫酸质量 | 20 | 20 | 20 |
| 生成气体质量 | | m | |
请回答下列问题并计算:
-
(1) 第二次实验时生成气体质量
 克;
克;
-
(2) 计算该合金样品中铜的质量分数.
.

-
(1) 石灰石样品的质量分数是(结果保留一位小数,下同);
-
(2) a点溶液的pH7(填“<”“>”或“=”);
-
(3) 求所加盐酸的溶质质量分数(写出计算过程)。
-
(1) 产生氢气的质量为。
-
(2) 该合金中铜的质量分数是。
-
(3) 稀硫酸中溶质的质量分数是。
-
(1) 铜可用来制作导线,是因为其具有良好的延展性和。
-
(2) 天津的解放桥是一座全钢结构可开启的桥梁,它是天津的标志性建筑物之一。
①钢属于(填“单质”、“纯净物”或“混合物”)。
②工业上用一氧化碳和赤铁矿炼铁的原理是(写化学方程式)。
③建造这座桥大约用了112t铁,理论需要含氧化铁80%的赤铁矿t。
-
(3) 为探究铁、铜、银的金属活动性顺序,同学们设计了如图所示的两步实验。

①第1步实验的目的是。
②第2步实验中,为了达到实验目的,溶液甲可以是(填序号)。
A、稀盐酸
B、FeSO4溶液
C、CuSO4溶液
D、ZnSO4溶液
-
(1) 铝土矿的的主要成分(填化学式)。
-
(2) 铝块拉成细丝、压成薄片是利用铝的(填“导热”或“延展”)性。
-
(3) 冶炼 500 t 含杂质 3% 的生铁,需要含氧化铁 80% 的赤铁矿石的质量是t(结 果精确到 0.1)。
-
(1) 生成二氧化碳的质量。
-
(2) 稀盐酸中溶质的质量分数。

根据图示信息,完成下列各题:
-
(1) 钙片中钙元素的质量分数为。
-
(2) 求恰好完全反应时所得溶液的溶质质量分数?(要求写出计算过程)

为测定该化肥中(NH4)2SO4的含量,小红称取5g该化肥放入烧杯中,加水至完全溶解(杂质溶于水但不参加反应),再将200gBa(OH)2溶液分4次加入其中。测得数据如下表所示:
| 次数 | 1 | 2 | 3 | 4 |
| 加入Ba(OH)2溶液质量/g | 50 | 50 | 50 | 50 |
| 生成沉淀质量/g | 2.33 | 4.66 | m | 6.99 |
-
(1) 请把测定过程中反应的化学方程式补充完整:
 。
。 -
(2) 表中m的值为。
-
(3) 计算化肥中(NH4)2SO4的质量分数并判断该化肥是否合格。(写出计算过程)
-
(4) 请在下图画出产生沉淀质量与加人Ba(OH)2溶液质量的关系图。(要标注必要的数值)

-
(1) 该黄铜样品中含锌的质量是克;
-
(2) 所用稀盐酸中溶质的质量分数是(结果保留一位小数);
-
(3) 反应后所得溶液中溶质质量分数是(结果保留一位小数)。
- 选出注音和字形没有错误的一组( ) A.阜盛(fǔ) 敕造(chì) 规矩(ju) 亲和力 声
- When______this kind of computer _______? A.is; used B. was;
- 下列说法中不正确的是 ( ) A.将纯水加热至较高温度,水的离子积变大,
- 科学家利用“同位素标记法”了解到许多化学反应的详细过程。下列说法正确的是( ) A.用32P标记DNA,弄清了
- He (go) to the park on Sundays.
- 阅读下面这首宋诗,完成小题。(8分) 鹧鸪词 李 益 湘江斑竹枝,锦翅鹧鸪飞。 处处湘云合,郎从何处归? 鹧鸪词 李
- 同志强调指出,要以积极的态度、创新的精神,大力发展和传播健康向上的网络文化,切实把互联网建设好、利用好、管理好,满足人民
- “千里之行,始于足下”。汽车是常用的交通工具,但汽车尾气会造成空气污染。下列能源的使用最有利于防止空气污染的是 A.太阳
- 能正确表达下列反应的离子方程式为 A.用醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O B.硫化亚铁与浓硫
- 编辑一个运算程序:11=2,mn=k,m(n+1)=k+3(m、n、k∈N*),12 006的输出结果为…()A.2
- 化简:()÷,当b=﹣2时,请你为a选择一个适当的值并代入求值.
- (5分)集合A=﹛x︳﹜,B=﹛x|a<x<a+ 5﹜,若,求a的取值范围.
- (2013山东省淄博市期末)为了探究加速度与力的关系,某同学设计了如图所示的实验装置,带滑轮的长木板水平放置,板上有两个
- 一个棱锥的底面积是S,经过这个棱锥的高的中点作一个平行于底面的截面,那么这个截面的面积是( )A.S
- 小明学习了汽化和液化后,对书本www练习的第4题感到疑问,于是他回家动手实验,发现水烧开了可纸杯却没有烧着.关于纸杯没有
- 任务型阅读;根据短文内容回答问题,并将答案写在相应位置。 Inmost countries, people usu
- 在“测定匀变速直线运动加速度”的实验中,得到的记录纸带如下图所示,图中的点为计数点,在每两相邻的计数点间还有4个点没有画
- 下列变异的原理一般认为属于基因重组的是() A.将转基因的四倍体与正常的二倍体杂交,生产出不育的转基因三倍体鱼苗 B.血
- 0.32,log20.3,20.3这三个数之间的大小顺序是() A.0.32<20.3<log20.3 B.0.3
- 读“某日洛杉矶几种污染物浓度日变化图”,根据“光化学烟雾”的相关知识回答1~2题。1.“光化学烟雾”的主要污染物是






