溶液的酸碱性与pH值的关系 知识点题库
化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图).他们提出可能是Na2SO4、NaHCO3、Na2CO3溶液中的一种,于是决定对这瓶溶液进行实验探究.查阅资料:三种物质溶液在常温下的pH如下表
|
溶液 |
Na2SO4 |
NaHCO3 |
Na2CO3 |
|
pH |
pH=7 |
pH>7 |
pH>7 |

-
(1) 小新同学认为该溶液不可能的是 , 理由是 .
-
(2) 标签破损的原因 .
-
(3) 为确定其成分,小新同学设计如下方案进行探究
实验步骤
现象
结论
取该溶液少许于试管中,滴加过量的BaCl2溶液,振荡.
①
则该溶液是Na2CO3溶液
过滤,向滤渣滴加稀盐酸.
②
-
(4) 小芳认为可以设计更简单的实验方案,该方案是:(写出实验步骤、现象及结论).
(1)牛奶中富含的营养素是 .
(2)人体摄入不足会引起多种疾病,补锌可通过服用葡萄糖酸锌(C12H22O14Zn)口服液,则葡萄糖酸锌是由 种元素组成,其中属于微量元素的是 (填名称).
(3)化石燃料是不可再生能源,可利用和开发的新能源有 (填一种即可).
(4)“绿色化学”的特点之一是在化工生产中尽可能实现“零排放”.用CO2和H2反应,只生成一种产物并且能实现“零排放”,该反应的基本类型为反应,反应生成物是下列中的 (填字母序号).
A.C2H4O B.C2H4O2 C.CH2O2 D.C3H6O
(5)人呼吸产生的CO2若不能及时排出,滞留在血液中会使血液的pH(填“不变”、“变大”或“变小”).
 B . 检测溶液pH
B . 检测溶液pH C . 检查装置气密性
C . 检查装置气密性 D . 浓硫酸稀释
D . 浓硫酸稀释
颜色 | 红 | 橙 | 绿 | 蓝 | 紫 |
pH范围 | 1~3 | 4~5 | 6~7 | 8~10 | 11~14 |
向滴有少量该指示剂的稀硫酸中,加入氢氧化钠溶液,出现的颜色变化可能是( )
-
(1) 小勇选用的调味品最有可能是;
-
(2) 肥皂水的pH7(填“大于”、“等于”或“小于”);
-
(3) 下列各组物质的溶液,仅用喇叭花不能鉴别的一组是 (填序号).A . HCl,NaOH B . HCl,NaCl C . NaOH,NaCl D . H2O,NaCl


-
(1) 通过如图可知,当碳酸钠溶液质量加到kg 时,废液恰好处理完(盐酸与氯化钙的混合溶液完全转化成氯化钠溶液)。
-
(2) 此时所得溶液能否用于该校生物兴趣小组的小麦选种(选种液要求氯化钠的溶质质量分数在 10%--20%之间)?请通过计算回答。
 B . 向一定量的锌粒中不断加入稀硫酸直至过量
B . 向一定量的锌粒中不断加入稀硫酸直至过量  C . 向相同质量和相同质量分数的稀硫酸中,分别加入过量的镁粉和铝粉
C . 向相同质量和相同质量分数的稀硫酸中,分别加入过量的镁粉和铝粉  D . 向一定量的氯化铁和氯化钾的混合液中,逐滴加入过量的氢氧化钾溶液
D . 向一定量的氯化铁和氯化钾的混合液中,逐滴加入过量的氢氧化钾溶液 

-
(1) 图二从A到B过程中,溶液的pH逐渐(填“增大”或“减小”)。
-
(2) 图二表示酸碱恰好完全反应的点是。
-
(3) 计算稀盐酸中溶质的质量分数。
-
(1) 农业上可用来降低土壤的酸性,改良土壤结构的物质是。(填化学式)
-
(2) 医疗上可用含氢氧化镁的药物来中和过多的胃酸(视为盐酸),有关反应的化学方程式为。
-
(3) 取某硫酸厂排出的一定体积的废水与一定量的氢氧化钠溶液混合后,溶液恰好呈中性。若改用与该氢氧化钠溶液的质量和溶质质量分数均相同的氢氧化钾溶液与上述一定体积的废水混合,则所得溶液的pH7(填“>”、“<”或“=”)。
| 选项 | A | B | C | D |
| 实验目的 | 证明醋酸溶液呈酸性 | 检验氯离子 | 除去氯化钠溶液中的硫酸钠 | 检验长期露置的氢氧化钠溶液是否变质 |
| 方案一 | 滴加几滴酚酞溶液观察是否变红 | 先加硝酸银溶液﹐再滴加稀硝酸 | 加入适量的硝酸钡溶液﹐过滤 | 加足量稀盐酸 |
| 方案二 | 用pH试纸检验溶液的pH | 先加稀盐酸,再滴加硝酸银溶液 | 加入适量的氯化钡溶液,过滤 | 加澄清石灰水 |
【提出假设】
假设一:可能含有氯化镁; 假设二:可能含有镁粉;
假设三:可能含有氢氧化镁。
【查阅资料】①镁可与热水反应生成氢氧化镁和氢气;②氢氧化镁在水中溶解度很小, 其水溶液呈弱碱性。
【设计并进行实验】各取少量灰白色沉淀加入 2 支试管中,进行如下实验:
|
编号 |
实验操作 |
实验现象 |
|
实验 1 |
加入一定温度的蒸馏水、搅拌 |
沉淀未见减少 |
|
实验 2 |
加入适量稀盐酸 |
沉淀全部溶解,没有气泡产生 |
【得出结论】根据实验 2 现象,说明假设二不成立。
【实验思考】
-
(1) 如果假设三成立,请写出实验 2 中发生反应的化学方程式:。
-
(2) 实验后同学们请教老师得知, 灰白色沉淀的主要成分是碱式氯化镁[Mg(OH)2·MgCl2],碱式氯化镁受热易分解产生氯化氢气体。为了验证试管中的 灰白色沉淀中含有碱式氯化镁,小米同学把灰白色沉淀放进试管进行加热,并在试管口放一张湿润的紫色石蕊试纸。如果灰白色沉淀中含有碱式氯化镁,则小米同学将看到的现象是。
-
(3) 镁与稀盐酸反应究竟是一个怎样的过程呢?小组同学进行了如下实验:在小烧杯中加入一定量的稀盐酸和去除氧化膜的镁带,测量溶液 pH 的变化,并观察实验现象。结果如下表:
时间/min
0
2
4
8
12
16
20
24
溶液 pH
2.0
5.3
7.0
8.6
9.3
9.8
10.0
10.0
实验现象
/
镁带溶解较快,产生大量气泡,试管温度升高,无沉淀生成
镁带缓慢溶解,产生气泡速率减慢,溶液变浑浊,烧杯底部有灰白色沉淀
根据表中信息,请你说说溶液 pH 值出现这样变化的原因:。
|
加入稀盐酸的体积/mL |
0 |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
|
烧杯中溶液的 pH |
12.9 |
12.7 |
12.5 |
12.3 |
11.9 |
7.0 |
2.1 |
1.9 |
-
(1) 当加入稀盐酸的体积为mL 时,NaOH 溶液和稀盐酸恰好完全反应。
-
(2) 当加入稀盐酸的体积为3mL时,溶液显色;当加入稀盐酸的体积为14mL时,溶液显色。
-
(3) 当烧杯中溶液的pH=2.1时,溶液中的溶质有:。(用化学式表示)
反应
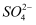 ,所以它不是酸
B . 碱溶液一定是碱性溶液
C . 在常温下pH=7的水溶液显中性
D . 酸溶液也可能呈碱性
,所以它不是酸
B . 碱溶液一定是碱性溶液
C . 在常温下pH=7的水溶液显中性
D . 酸溶液也可能呈碱性
- “《孟子》一书中提到治水的有11次之多,……其中一段更直接指责当时人以洪水冲刷邻国的不道。我们不难从中看出洪水与黄河暨黄
- I want to buy some postcards in the shop, ______ Idon’t have
- 下列省级行政区与简称及行政中心搭配不正确的是( ) A、新疆维吾尔自治区——新——乌鲁木齐 B、安徽——安——合肥
- 图6电路中,电源电压不变,R1 为定值电阻,R2 为滑动变阻器。闭合开关S,移动滑片P,多次记录电压表和电流表示数,绘出
- 高空实验火箭起飞前,仪器舱内气体的压强p0=1 atm,温度t0=27℃,在火箭竖直向上飞行的过程中,加速度的大小等于重
- 我国人民代表大会制度组织和活动最重要的特点,就是实行 A.民主选举制 B.民主决策
- 日本是亚洲经济最发达的国家,2015年中国游客赴日人数大涨至490万人次,旅游市场规模达154亿元人民币,日本成为中国出
- Thepark is so large. Follow your, or you may lose the way.
- 为防止腐败现象的出现,必须加强对权力的制约和监督。下列对权力制约和监督说法正确的是( )①有效制约和监督权力的关
- 战国时邹衍用五行相胜说来解释朝代的变更,创立了五德始终说,按他的说法,夏禹是木德,商汤是金德,周文王是火德。秦始皇采用此
- The failed Skylab will come screaming home to the earth in
- 课题研究小组对附着在物体表面的三个微生物(课题小组成员把他们分别标号为1,2,3)的生长情况进行观察记录.这三个微生物第
- 下列事故或药品的处理正确的是 A.少量浓硫酸溅到皮肤上,立即用氢氧化钠溶液冲洗 B.当出现CO中毒时,应立即将中毒者抬到
- 染色质和染色体的正确关系是A.同种物质在同一时期的两种形态 B.不同种物质在同一时期的两种形态C.同种物质在不同
- 下列说法正确的是( )A.用乙醇或CCl4可提取碘水中的碘单质B.NaCl和SiC熔化时,克服粒子间作用力的类型相
- 下表是苏联20世纪二三十年代粮食产量的统计数据。出现这一变化的主要原因是() 年代 1925—1927年 1928—19
- 抛物线y2=2px动弦AB长为a(a≥2p),弦AB中点到y轴最短距离是()A.
- (一)文言文阅读(19分) 阅读下面文言文。按要求完成4—7题 胡宿,字武平,常州晋陵人,宿为人清谨忠实,内刚外
- Only when _____ the painting _____ decide whether the painti
- 狼根据兔留下的气味进行捕食,兔根据狼的气味或行为特征躲避猎捕,这个事实说明( ) A.生命活动必需依靠信息的传递B.信息



