有关过量问题的计算 知识点题库
下列叙述中正确的是( )
A . 含a mol AlCl3的溶液和含1.5a mol NaOH的溶液,无论正滴和反滴,生成的Al(OH)3的质量相等
B . 含a mol Na2CO3的溶液和含1.5a mol HCl的稀盐酸,无论正滴和反滴,生成的CO2相等
C . 等质量的NaHCO3和Na2CO3分别与足量盐酸反应.在同温同压下,生成的CO2体积相同
D . 将盛有24mL NO2和O2的混合气体的量筒倒立于水槽中,充分反应后还剩余4 mL无色气体,则原混合气体中O2的体积是8 mL 或 1.2mL
用1L1mol·L-1NaOH溶液吸收0.8molCO2 , 所得溶液中Na2CO3和NaHCO3的物质的量之比约为( )
A . 1︰3
B . 1︰2
C . 2︰3
D . 3︰2
将O2和NH3的混合气体448mL通过加热的三氧化二铬,充分反应后,再通过足量的水,最终收集到44.8mL气体。原混合气体中O2的体积可能是(假设氨全部被氧化;气体体积均已换算成标准状况)( )
A . 231.5mL
B . 268.8mL
C . 287.5mL
D . 313.6mL
在标准状况下,进行甲、乙、丙三组实验:三组各取60mL同浓度盐酸,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:
实验序号 | 甲 | 乙 | 丙 |
合金质量/mg | 510 | 770 | 918 |
气体体积/mL | 560 | 672 | 672 |
则下列说法正确的是( )
A . 甲组和乙组的实验中,盐酸均是过量的
B . 盐酸的物质的量浓度为0.8mol/L
C . 合金中镁铝的物质的量之比为1:1
D . 丙组中铝的物质的量为0.009mol
在给定条件下,下列加点的物质在化学反应中完全消耗的是( )
A . 用50mL 12 mol•L﹣1的氯化氢水溶液与足量二氧化锰共热制取氯气
B . 将1g铝片投入20mL 18.4 mol•L﹣1的硫酸中
C . 向100mL 3 mol•L﹣1的硝酸中加入5.6g铁
D . 常温常压下,0.1mol氯气通入1L水中反应
100ml 1mol/L的AlCl3溶液与100ml3.5mol/L的NaOH溶液混合,得到沉淀为( )
A . 7.8g
B . 0g
C . 91g
D . 3.9g
下列各组稀溶液相互反应。无论前者滴入后者,还是后者滴入前者,反应现象都相同的( )
A . Na2SiO3溶液与HCl溶液
B . AlCl3溶液与NaOH溶液
C . KAlO2 溶液与HCl溶液
D . Na2CO3溶液和HCl溶液
现有等体积混合而成的4组气体: ①NO2+NO. ②HCl+N2 ③NO2+O2 ④Cl2+SO2。现将其分别通入体积相同的试管中并立即倒立在足量水中,试管内剩余的气体体积分别为V1、V2、V3、V4 , 则下列关系正确的是( )
A . V1>V3>V2>V4
B . V1>V2>V3>V4
C . V2>V3>V4>V1
D . V3>V1>V4>V2
下列说法正确的是( )
A . 等质量的质量分数均为4%的氢氧化钠溶液与稀盐酸充分反应后,所得溶液显中性
B . 等质量的Al和Mg分别与足量稀硫酸充分反应,生成H2的质量相等
C . 等质量的NaHCO3和MgCO3分别与足量稀盐酸充分反应,生成CO2的质量相等
D . 等质量的CO和CO2 , CO和CO2中氧元素的质量比为1:2
向含Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL 1 mol·L-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法错误的是( )
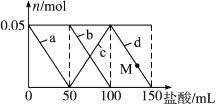
A . a曲线表示的离子方程式为:AlO2-+H++H2O =Al(OH)3↓
B . b和c曲线表示的离子反应是相同的
C . M点时,溶液中沉淀的质量为3.9 g
D . 原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2
将铜与Fe2O3的混合物共28.8g加入300mL2.00mol·L-1 的稀硫酸中,充分反应后剩余固体的质量为6.40g。请计算:
-
(1) 混合物中铜的物质的量为mol。
-
(2) 反应后的溶液中最多消耗锌片的质量为g。
下列示意图与对应的反应情况正确的是( )
A . 向AgNO3和CuCl2的混合溶液中缓慢通入氨水溶液  B . 向NaOH和Ca(OH)2的混合溶液中通入CO2
B . 向NaOH和Ca(OH)2的混合溶液中通入CO2 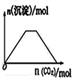 C . KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液
C . KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液  D . NaAlO2、Na2CO3溶液中逐滴加入盐酸
D . NaAlO2、Na2CO3溶液中逐滴加入盐酸 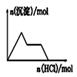
 B . 向NaOH和Ca(OH)2的混合溶液中通入CO2
B . 向NaOH和Ca(OH)2的混合溶液中通入CO2  C . KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液
C . KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液  D . NaAlO2、Na2CO3溶液中逐滴加入盐酸
D . NaAlO2、Na2CO3溶液中逐滴加入盐酸 
向盛有下列固体的试管中逐滴加入盐酸至过量,盐酸只发生一个化学反应的是( )
A . 硝酸银
B . 生锈的铁
C . 碳酸钠
D . 次氯酸钠
向用HCl酸化过的AlCl3溶液中逐滴滴入NaOH溶液,图中能正确表示这个反应的是( )
A . 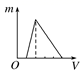 B .
B . 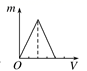 C .
C . 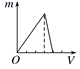 D .
D . 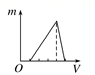
 B .
B .  C .
C .  D .
D . 
将盛有 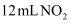 和
和  混合气体的量筒倒立于水槽中,充分反应后,还剩余
混合气体的量筒倒立于水槽中,充分反应后,还剩余 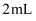 无色气体,则原混合气体中
无色气体,则原混合气体中  的体积和剩余的
的体积和剩余的 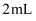 气体可能分别是( )
气体可能分别是( )
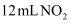 和
和  混合气体的量筒倒立于水槽中,充分反应后,还剩余
混合气体的量筒倒立于水槽中,充分反应后,还剩余 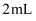 无色气体,则原混合气体中
无色气体,则原混合气体中  的体积和剩余的
的体积和剩余的 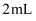 气体可能分别是( )
气体可能分别是( )
A . 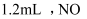 B .
B . 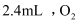 C .
C . 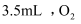 D .
D . 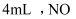
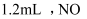 B .
B . 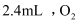 C .
C . 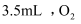 D .
D . 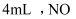
将二氧化碳通入澄清石灰水中,有白色沉淀生成,若继续通入二氧化碳,白色沉淀将完全溶解。其反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;CaCO3+CO2+H2O=Ca(HCO3)2;当二氧化碳持续不断地通入澄清石灰水中时,沉淀质量变化符合下图中的( )
A . 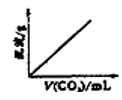 B .
B . 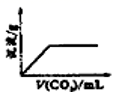 C .
C . 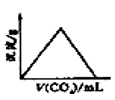 D .
D . 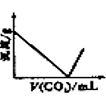
 B .
B .  C .
C .  D .
D . 
下列各组物质互相反应,生成物不随反应条件或反应物用量多少而变化的是( )
A .  和
和  B .
B .  和盐酸
C .
和盐酸
C .  和氯气
D .
和氯气
D .  和
和  溶液
溶液
 和
和  B .
B .  和盐酸
C .
和盐酸
C .  和氯气
D .
和氯气
D .  和
和  溶液
溶液
下列各组中的两种物质作用时,反应条件或反应物的用量改变时,对生成物没有影响的是( )
A . Na与O2
B . Na2O2与CO2
C . NaOH与AlCl3
D . NaOH与CO2
乙酸乙酯是一种重要的化工原料,广泛用于药物染料、香料等工业。
-
(1) I.下图所示是乙酸乙酯的绿色合成路线之一:
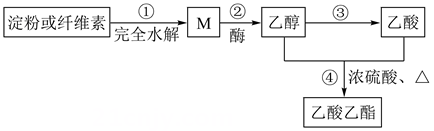
M的分子式为。 -
(2) 下列说法错误的是(填字母)。
a.淀粉和纤维素的分子式均为(C6H10O5)n , 但n值不同
b.反应③的类型为加成反应
c.M可与银氨溶液在碱性、加热条件下反应析出银
-
(3) II.某课外小组同学设计如图所示装置制取并提纯乙酸乙酯。A中盛有浓硫酸,B中盛有一定量无水乙醇和冰醋酸,D中盛有饱和碳酸钠溶液。
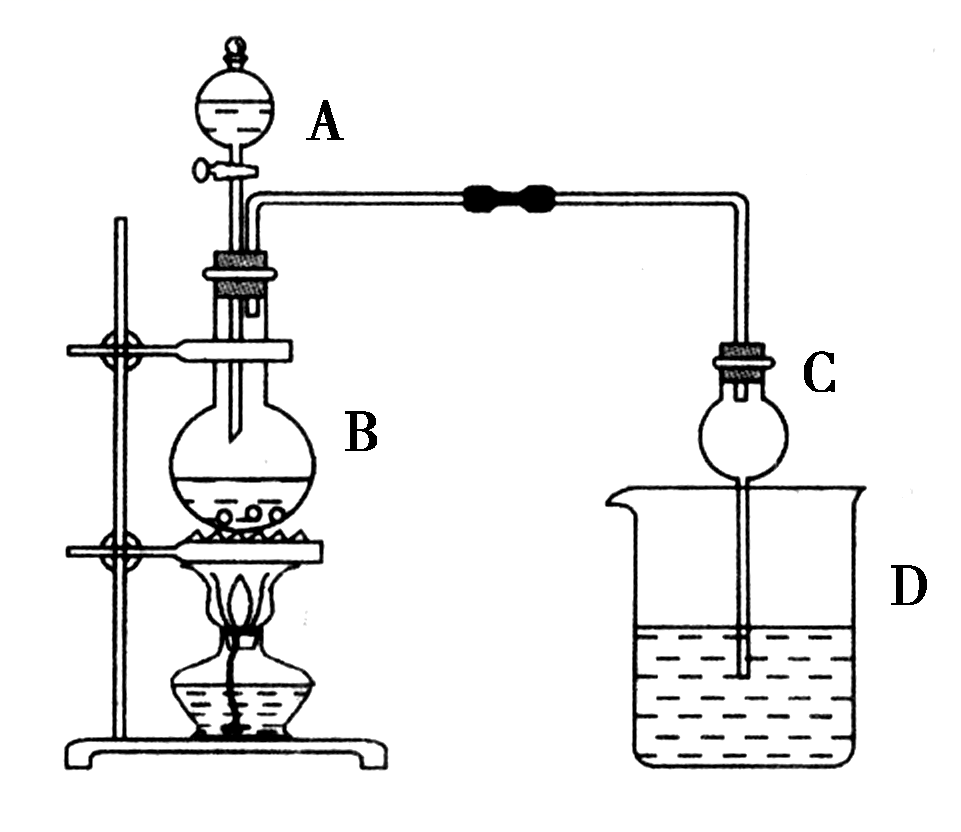
已知:①氯化钙可与乙醇形成微溶于水的
 ;
;②
 ;
;③有关有机物的沸点如下表:
试剂
乙醚
乙醇
乙酸
乙酸乙酯
沸点/℃
34.7
78.8
118
77.1
加热一段时间,B中生成乙酸乙酯的化学反应方程式为。
-
(4) 球形干燥管C的主要作用是。
-
(5) 若反应前向D中加入几滴无色酚酞试液,反应结束后振荡、静置,可观察到D中的现象是。
-
(6) 从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出;再加(填字母)除水;然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
a.五氧化二磷 b.碱石灰 c.无水硫酸钠 d.生石灰
-
(7) 加热有利于提高乙酸乙酯的产率,但实验过程中发现,温度过高乙酸乙酯的产率反而降低,可能的原因是(填一种)。
-
(8) 用30g乙酸与46g乙醇反应,若实际产量是理论产量的70%,则实际得到乙酸乙酯的质量为 g。
一定量CO2通入500mL某浓度的NaOH溶液中得到溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(CO2)的关系如图所示。下列有关叙述不正确的是( )
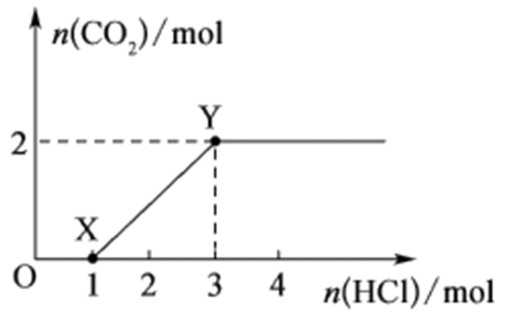
A . X→Y段发生反应的子方程式为HCO +H+=H2O+CO2↑
B . 原溶液中c(NaOH)=6mol/L
C . 通入的CO2气体体积为44.8L
D . A溶液中含Na2CO3和NaHCO3各1mol
+H+=H2O+CO2↑
B . 原溶液中c(NaOH)=6mol/L
C . 通入的CO2气体体积为44.8L
D . A溶液中含Na2CO3和NaHCO3各1mol
 +H+=H2O+CO2↑
B . 原溶液中c(NaOH)=6mol/L
C . 通入的CO2气体体积为44.8L
D . A溶液中含Na2CO3和NaHCO3各1mol
+H+=H2O+CO2↑
B . 原溶液中c(NaOH)=6mol/L
C . 通入的CO2气体体积为44.8L
D . A溶液中含Na2CO3和NaHCO3各1mol
最近更新
- 如图,AB是⊙O的直径,弦CD⊥AB于点E,∠CDB=30°,⊙O的半径为cm,则弦CD的长为()A. cmB.3cmC
- 下列各组原子序数所表示的两种元素,能形成AB2型离子化合物的是( )A.11和16 B.12和9
- 国家杂交水稻工程技术研究中心暨湖南杂交水稻研究中心主任、中国工程院院士袁隆平获得“全国敬业奉献道德模范”称号,这个称号属
- 某气体的摩尔质量是M g·mol-1,分子数为N,在标准状况下所占的体积是VL,质量是mg。某元素原子的摩尔质量是Ag·
- 某人乘小船以一定的速率垂直河岸向对岸驶去,当水流匀速时,关于他渡河所需时间、发生的位移与水流速度的关系的说法中正确的是
- 近代英、法、美资产阶级革命后确立了代议制民主政治。代议制的核心是( ) A、实行民主共和政体
- ________moment he saw Zhao Benshan’s funny performances, he
- (2011年唐山一模)Say“Cheese” but keep________while I take yourpho
- 在盛放浓硫酸的试剂瓶的标签上应印有下列警示标记中的是( )。
- 美国记者史沫特莱曾对一场战役作这样报道:“整个华北地区,从晋北山区到东海岸。从南面的黄河到北面的长城,都成了战场,……一
- 阅读下列材料,分析回答下列问题。 材料一 山西省交城县城西的安定村积极推广使用日光温室、猪圈、厕所和沼气池“四位一体”
- (10分)如图甲所示,足够大的水平面上静置一质量m=lkg的物体,若物体一旦运动就会受到一个阻碍物体运动的阻力f,且f=
- 的夹角为,,则 。
- _______ the warning message, more lives would have been lost
- 设,,…,,n∈N,则= ( ) A. B. C.
- 对于化学反应:4P+5O22P2O5,下列说法正确的是() ①参加反应的物质是磷和氧气②反应前后分子总数不变③反应前后元
- 以下说法中不正确的是( ) A.卡文迪许通过扭秤实验,测定了万有引力常量 B. 奥斯特通过实验研究,发现了电流周围
- ......
- 新航路开辟后,先后成为贸易强国和殖民强国的下列国家,排列正确的是( ) A.葡萄牙、西班牙→荷兰→英国 B.意大利→
- △ABC中,若sin2A=sin2B+sin2C,则△ABC为( ) A.直角三角形



