化学式及其计算 知识点题库
已知一个N2O3分子质量为a kg,一个N2O5分子的质量为b kg,若以氧原子质量的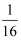 作为相对原子质量的标准,则NO2的相对分子质量是( )
作为相对原子质量的标准,则NO2的相对分子质量是( )
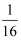 作为相对原子质量的标准,则NO2的相对分子质量是( )
作为相对原子质量的标准,则NO2的相对分子质量是( )
A . 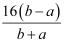 B .
B . 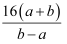 C .
C . 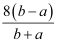 D .
D . 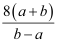
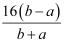 B .
B . 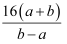 C .
C . 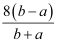 D .
D . 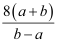
0.8g某物质中含有3.01×1022个分子,该物质的相对分子量是( )
A . 16
B . 16g
C . 32
D . 32g/mol
按要求在下列空格中填出下列有机物的有关式子:
糖尿病患者尿液中含的糖类结构简式 ,甲醛(CH2O)、乙酸(C2H4O2)和果糖(C6H12O6)组成的混合物中,氧元素的质量分数是53.3%,则碳元素的质量分数为
11.7g NaX含有Na+0.2mol,则NaX的摩尔质量为.
一个12C原子的质量为akg,一个12C16O2分子的质量为bkg,若以12C16O2中的一个氧原子质量的1/16作为相对原子质量标准,则12C16O2的相对分子质量为( )
A . 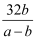 B .
B . 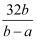 C .
C . 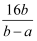 D .
D . 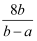
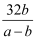 B .
B . 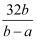 C .
C . 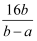 D .
D . 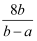
某气体物质的质量为6.4g,含有6.02×1022个分子,则该气体的相对分子质量是( )
A . 64
B . 32
C . 96
D . 124
甲醛(CH2O)、乙酸(C2H4O2)和丙醛(C3H6O)组成的混合物中,氧元素的质量分数是37%,则碳元素的质量分数为( )
A . 27%
B . 28%
C . 54%
D . 无法计算
现有C2H2、CH3CHO、乙二醇三种蒸汽的混合物,已知含碳量为a%,则氢的含量为( )
A . 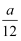 %
B .
%
B . 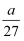 %
C .
%
C . 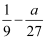 %
D . 无法计算
%
D . 无法计算
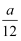 %
B .
%
B . 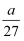 %
C .
%
C . 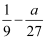 %
D . 无法计算
%
D . 无法计算
某烃含碳元素的质量分数为85.7%,则该烃是( )
A . 甲烷
B . 乙烯
C . 苯
D . 不能确定
下列各组混合气体中,比乙烯含碳量高的是( )
A . 甲烷和丙烯
B . 乙烷和丁烯
C . 环丙烷与丙烯
D . 丙烯与丙炔
由乙炔、苯、乙醛组成的混合物,经测定其中碳元素质量分数为36%,则混合物中氧元素的质量分数为( )
A . 44%
B . 54.22%
C . 39.12%
D . 无法计算
A、B两种化合物由M、X两种元素组成,已知A中M元素的质量分数为44.0%,B中M元素的质量分数为34.5%,A的化学式为MX2 , 则B的化学式为 ( )
A . MX
B . M2X3
C . MX3
D . MX4
在标况下,0.28g某气体的体积为224mL,则该气体的相对分子质量是( )
A . 2
B . 56
C . 28
D . 0.028
下列铁的化合物中,含Fe元素的质量分数最小的是( )
A . FeO
B . Fe2O3
C . Fe3O4
D . FeS2
元素R的最高价含氧酸化学式为HnRO2n+2 , 在它的气态氢化物中,R的化合价为( )
A . 3n-10
B . 3n-4
C . 3n-12
D . 4-3n
取少量某镁铝合金粉末,其组成可用MgxAly表示,向其中加入足量稀硫酸充分反应,收集到3.808L H2(标准状况)同时得无色溶液,向所得溶液中加入过量NaOH溶液,充分反应得到沉淀4.64g。则x∶y为( )
A . 2∶1
B . 4∶3
C . 1∶1
D . 1∶2
甲、乙、丙三种有机化合物的键线式如图所示。下列说法错误的是( )
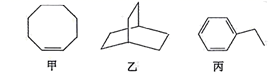
A . 甲、乙的化学式均为C8H14
B . 乙的二氯代物共有7种(不考虑立体异构)
C . 丙的名称为乙苯,其分子中所有碳原子可能共平面
D . 甲、乙、丙均能使酸性高锰酸钾溶液褪色
某溶液中大量存在以下五种离子:MnO4-、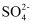 、Fe3+、Na+、R,它们的物质的量之比为n(MnO4-):n(
、Fe3+、Na+、R,它们的物质的量之比为n(MnO4-):n(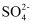 ):n(Fe3+):n(Na+):n(R)=2:2:1:2:1,则R可能( )
):n(Fe3+):n(Na+):n(R)=2:2:1:2:1,则R可能( )
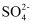 、Fe3+、Na+、R,它们的物质的量之比为n(MnO4-):n(
、Fe3+、Na+、R,它们的物质的量之比为n(MnO4-):n(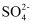 ):n(Fe3+):n(Na+):n(R)=2:2:1:2:1,则R可能( )
):n(Fe3+):n(Na+):n(R)=2:2:1:2:1,则R可能( )
A . Ag+
B . Fe2+
C . CO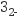 D . K+
D . K+
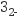 D . K+
D . K+
已知某气态烃A在标准状况下的密度是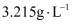 , 取
, 取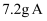 在足量
在足量 中充分燃烧,把燃烧后的产物全部通过浓
中充分燃烧,把燃烧后的产物全部通过浓 , 浓
, 浓 质量增加
质量增加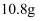 , 再把剩余气体通过碱石灰,碱石灰质量增加
, 再把剩余气体通过碱石灰,碱石灰质量增加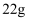 , 下列说法正确的是( )
, 下列说法正确的是( )
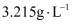 , 取
, 取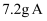 在足量
在足量 中充分燃烧,把燃烧后的产物全部通过浓
中充分燃烧,把燃烧后的产物全部通过浓 , 浓
, 浓 质量增加
质量增加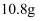 , 再把剩余气体通过碱石灰,碱石灰质量增加
, 再把剩余气体通过碱石灰,碱石灰质量增加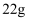 , 下列说法正确的是( )
, 下列说法正确的是( )
A . 该烃的摩尔质量为72
B . 该烃的分子式为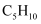 C . 该烃分子中一个氢原子被溴原子取代后,可形成8种同分异构体
D . 该烃化学性质稳定,不能发生氧化反应
C . 该烃分子中一个氢原子被溴原子取代后,可形成8种同分异构体
D . 该烃化学性质稳定,不能发生氧化反应
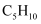 C . 该烃分子中一个氢原子被溴原子取代后,可形成8种同分异构体
D . 该烃化学性质稳定,不能发生氧化反应
C . 该烃分子中一个氢原子被溴原子取代后,可形成8种同分异构体
D . 该烃化学性质稳定,不能发生氧化反应
草酸镍晶体(NiC2O4·2H2O)可用于制镍催化剂,硫酸镍晶体(NiSO4·7H2O)主要用于电镀工业。某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、 Fe 及其氧化物、SiO2、 CaO等,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O)。
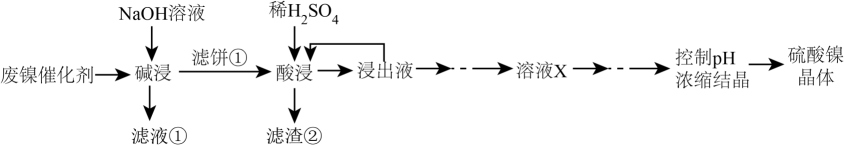
已知:①溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
开始沉淀pH | 7.2 | 3.7 | 2.2 | 7.5 |
完全沉淀pH | 8.7 | 4.7 | 3.2 | 9.0 |
②CaF2的溶解度小于CaC2O4
③NiSO4·7H2O易溶于水,难溶于乙醇
回答下列问题:
-
(1) “碱浸”中NaOH的作用除去Al和Al2O3、。
-
(2) 由流程中的“浸出液”制备硫酸镍晶体的正确实验步骤是:
第1步:取“浸出液”,加入足量的 H2O2调节溶液pH的范围为,充分反应后过滤,以除去铁元素;
第2步:向所得滤液中加入适量NH4F溶液,充分反应后过滤,得“溶液X”;
第3步:调节滤液的pH>8. 7,充分反应后过滤;
第4步:滤渣用稍过量硫酸充分溶解后,蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得硫酸镍晶体。
-
(3) 下列说法错误的是____A . 快速冷却溶液,可以得到细小的晶体颗粒 B . 滤饼①中只含有Fe、Ni两种金属元素 C . 碱浸后抽滤得到滤饼①,该操作过程中需先微开水龙头,让滤纸紧贴布氏漏斗上 D . 将分离出硫酸镍晶体后的母液收集、循环使用,其意义是提高镍的回收率
-
(4) 步骤2若加入适量(NH4)2C2O4会得到草酸钙晶体,某研究所利用SDTQ600热分析仪对草酸钙晶体(CaC2O4·xH2O)进行热分解,获得相关数据,绘制成固体质量一分解温度的关系如图。

①800℃以上时,固体成分的化学式为 。
②残留固体为CaC2O4时的温度范围。
③写出固体质量由12. 8g变为10. 0g时的化学方程式。
最近更新
- 一质量为m的带电液滴以竖直向下的初速度v0进入某电场中。由于静电力和重力的作用,液滴沿竖直方向下落一段距离h后,速度为0
- 为了节能、方便,有的楼道照明灯使用声、光控开关,其原理是:光控开关在黑暗时闭合,声控开关在有一定响度的声音时闭合,图中能
- 22.在下面一段文字的空白处补写恰当的语句,使整段文字语意完整,逻辑严密,前后连贯。每处字数不得超过所给空格数(含标点符
- 下列各物质的名称正确的是 ( ) A.3,3-二甲基丁烷 B.2,3,3-三甲基丁烷 C.2,
- 西周分封制在中国历史上影响深远。下列省、自治区中,其简称源自西周封国国名的是 A.河南、河北 B.湖南、湖北
- 若f(x)是定义在R上的奇函数,且满足f(x-2)=-f(x).给出下列四个结论: ①f(2)=0; ②f(x)是以4位
- . 第三节 完形填空(共20小题,计分30分) 阅读下面短文,掌握其大意,然后从21-40各题所给的四个选项中,选出一个
- 向Ba(OH)2和NaOH混合溶液中缓缓通入CO2气体至过量,生成沉淀物质的量与通入CO2气体的体积V(标准状况)的关系
- 艺术节奏的具体形成方式和构置方式是多种多样的。如我们可以通过落差来来形成艺术节奏。所谓落差就是起落度的差距很大,起如飞涛
- 有机物A、B、C、D、E都是常见的有机物,能发生如图所示的转化,已知A的分子式为C10H20O2,则符合此转化关系的A的
- 1947年上海《大公报》连载漫画《三毛流浪记》,作品揭示了流浪儿童的苦难生活,三毛对当时中国市场上到处充斥着某国商品感到
- 默写(任选一题)( 5分)(1)携幼入室, 。引壶觞以自酌,眄庭柯以怡颜。 ,审容膝
- 2008年1月7日,东北农业大学培育出我国第二代绿色荧光蛋白转基因克隆猪。研究人员是先从一种特殊水母中提取绿色荧光蛋白基
- 将阻值为20Ω的电阻丝接在电压为10V的电源两端,通电10s,产生的热量为______J。
- 有如图所示的装置,当电流表中产生持续电流时,下列说法正确的是 ()A.Cu是原电池的负极 B.Al是原电池的负极 C.电
- 阅读下面一首宋诗,然后回答问题。村 行① 王禹稱马穿山径菊初黄,信马悠悠野兴长。万壑有声含晚籁,数峰无语
- 我国面积最大的省级行政单位是:( ) A 四川 B 新疆 C 西藏
- Brandon worked for hours after school________money for her e
- 16、孟德尔的豌豆杂交试验中,将纯种的黄色圆粒(YYRR)与纯种的绿色皱粒(yyrr)豌豆杂交。F2种子为556粒(以5
- ,西北望,射天狼。(苏轼《江城子》)



