有关燃烧热的计算 知识点题库
在燃烧2.24L(标准状况)CO与O2的混合气体时,放出11.32kJ的热量,最后产物的密度为原来气体密度的1.25倍,则CO的燃烧热为( )
A . 283 kJ·mol-1
B . -283 kJ·mol-1
C . -566 kJ·mol-1
D . 566kJ·mol-1
在36 g碳不完全燃烧所得气体中,CO占 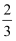 体积,CO2占
体积,CO2占  体积,且C(s)+
体积,且C(s)+  O2(g) = CO(g) ΔH=-110.5 kJ/mol;CO(g)+
O2(g) = CO(g) ΔH=-110.5 kJ/mol;CO(g)+  O2(g) = CO2(g) ΔH=-283 kJ/mol。与这些碳完全燃烧相比,损失的热量是 ( )
O2(g) = CO2(g) ΔH=-283 kJ/mol。与这些碳完全燃烧相比,损失的热量是 ( )
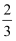 体积,CO2占
体积,CO2占  体积,且C(s)+
体积,且C(s)+  O2(g) = CO(g) ΔH=-110.5 kJ/mol;CO(g)+
O2(g) = CO(g) ΔH=-110.5 kJ/mol;CO(g)+  O2(g) = CO2(g) ΔH=-283 kJ/mol。与这些碳完全燃烧相比,损失的热量是 ( )
O2(g) = CO2(g) ΔH=-283 kJ/mol。与这些碳完全燃烧相比,损失的热量是 ( )
A . 172.5 kJ
B . 110.5 kJ
C . 283 kJ
D . 566 kJ
下列各组物质的燃烧热相等的是( )
A . 碳和二氧化碳
B . 1mol碳和3mol碳
C . 3mol乙炔(C2H2)和1mol苯(C6H6)
D . 天然气和酒精
汽车尾气中排放的NOx和CO污染环境,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
-
(1) Ⅰ.已知:①2CO(g)+O2(g)=2CO2(g) ΔH1=-566.0 kJ·mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+180.5 kJ·mol-1
③2NO(g)+O2(g)=2NO2(g) ΔH3=-116.5 kJ·mol-1
CO的燃烧热为。
-
(2) 若1 mol N2(g)、1 mol O2(g)分子中化学键断裂时分别需要吸收946 kJ、498 kJ的能量,则1 mol NO(g)分子中化学键断裂时需吸收的能量为。
-
(3) Ⅱ.利用水煤气合成二甲醚的总反应为:
3CO(g)+3H2(g)=CH3OCH3(g)+CO2(g) ΔH=-246.4 kJ·mol-1
它可以分为两步,反应分别如下:
①2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g) ΔH1=-205.1 kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=。
-
(4) 已知CH3OCH3(g)的燃烧热为1455 kJ·mol-1 , 写出表示其燃烧热的热化学方程式:。若二甲醚燃烧生成的CO2恰好能被100 mL 0.2 mol·L-1 NaOH溶液吸收生成Na2CO3 , 则燃烧过程中放出的热量为。
一些烷烃的燃烧热如下表:
| 化合物 | 燃烧热(kJ·mol-1) | 化合物 | 燃烧热(kJ·mol-1) |
| 甲烷 | 890.3 | 正丁烷 | 2 878.0 |
| 乙烷 | 1 560.8 | 异丁烷 | 2 869.6 |
| 丙烷 | 2 221.5 | 2-甲基丁烷 | 3 531.3 |
下列说法正确的是( )
A . 正戊烷的燃烧热大约是3 540 kJ·mol-1
B . 热稳定性:正丁烷>异丁烷
C . 乙烷燃烧的热化学方程式为2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g) ΔH=-1560.8 kJ·mol-1
D . 相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多
下列四幅图所表示的信息与对应的叙述相符的是( )
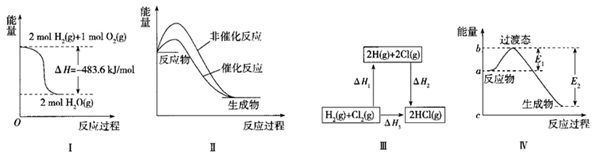
A . 图Ⅰ表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8kJ·mol-1
B . 图Ⅱ表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
C . 图Ⅲ表示一定条件下H2与Cl2生成HCl的反应热与途径无关,则△H2<△H3
D . 由图Ⅳ可知该反应△H =(E2 - E1)kJ·mol-1
石墨燃烧过程中的能量变化可用下图表示。下列说法正确的是( )
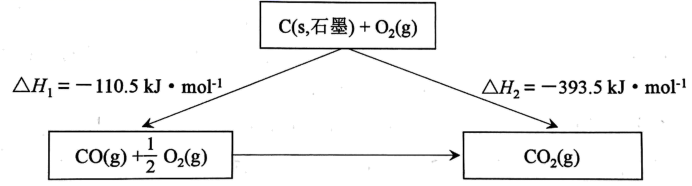
A . 石墨的燃烧热为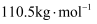 B . 反应C(s,石墨)
B . 反应C(s,石墨)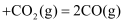 在任何温度下均能自发进行
C . 由图可知:
在任何温度下均能自发进行
C . 由图可知:
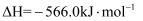 D . 已知C(s,金刚石)=C(s,石墨)
D . 已知C(s,金刚石)=C(s,石墨)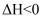 , 则金刚石比石墨稳定
, 则金刚石比石墨稳定
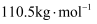 B . 反应C(s,石墨)
B . 反应C(s,石墨)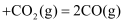 在任何温度下均能自发进行
C . 由图可知:
在任何温度下均能自发进行
C . 由图可知:
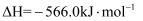 D . 已知C(s,金刚石)=C(s,石墨)
D . 已知C(s,金刚石)=C(s,石墨)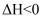 , 则金刚石比石墨稳定
, 则金刚石比石墨稳定
下列关于分子组成为 的烷烃、烯烃、炔烃的说法正确的是( )
的烷烃、烯烃、炔烃的说法正确的是( )
 的烷烃、烯烃、炔烃的说法正确的是( )
的烷烃、烯烃、炔烃的说法正确的是( )
A . 当x≤4时,常温常压下不一定均为气体
B . 燃烧时,火焰均为明亮火焰,并伴有黑烟
C . 当x<10,y=2x+2时, 的一氯代物只有一种的烃有4种
D . 分别完全燃烧1mol
的一氯代物只有一种的烃有4种
D . 分别完全燃烧1mol 时,消耗氧气为
时,消耗氧气为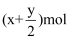
 的一氯代物只有一种的烃有4种
D . 分别完全燃烧1mol
的一氯代物只有一种的烃有4种
D . 分别完全燃烧1mol 时,消耗氧气为
时,消耗氧气为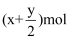
某有机物X6.0g在足量氧气中完全燃烧,生成8.8gCO2和3.6g水。下列说法错误的是( )
A . X分子中一定含有氧元素
B . X的分子式可能为CH2O
C . 若X为最简单的醛糖,则X分子中至少有6个碳原子
D . 若X与乙醇、乙酸都能发生酯化反应,则X分子中至少有3个碳原子
最近更新
- 3.一质量为m的物体放在光滑水平面上.今以恒力F沿水平方向推该物体,在相同的时间间隔内,下列说法正确的是 (A)物体
- 在“美馆美名”活动中,大家给上海世博会的许多场馆起了一个美丽的名字,如英国馆的“蒲公英”,黑龙江馆的“冰点诱惑”,都极富
- 空气中含量最多的气体是()A.氧气 B.二氧化碳 C.氮气 D.稀有气体
- 下列不平等条约中,严重损害中国关税自主权的是 A.《南京条约》 B.《黄埔条约》 C.《望厦条约》 D.《马关条
- 下列词语中加点的字,每对读音都不相同的一组是 A.阡陌/纤毫毕见 曝光/一曝十寒 嗔怪/瞋目而视 B.罢黜/相形见绌 折
- (08年长春外国语学校期中)(5分)使用中值电阻为(×1档)的多用电表测量两个定值电阻和,(已知和的阻值分别约为和,在下
- 在探究“滑动摩擦力的大小与什么有关”实验中,小聪以相同方式拉着同一个物体分别在水平地面和水平冰面上缓慢滑行,感觉在冰面上
- 明代沉船“南澳一号”发掘引起社会关注,学术以此为题进行研究性学习,搜集的一条史料是:“(明中后期,有大臣)请开市舶,易私
- 如下图所示,坐标纸上的每个单元格的边长为,由下往上的六个点:,,,,,的横、纵坐标分别对应数列()的前项,如下表所示:
- 自1998年至今,根据国内外经济形势的变化情况,我国的倾向政策经历了从“稳健”到“从紧”再到“适应宽松”的变化过程。这一
- 下列句子中加点的词语使用不恰当的一项是:( )A.不久前,中央电视台举办了“隆力奇杯”全国青年歌手电视大奖赛,选手们的表
- 如图所示,已知AB为⊙O的直径,CD是弦,且ABCD于点E. 连接AC、OC、BC。 (1)求证:ACO=BCD. (
- 某化工厂排放的污水中含有Al3+、Fe3+、Hg2+、Cu2+四种离子。甲、乙、丙三位同学设计的从该污水中回收金属铜的方
- 要测量河两岸相对的两点的距离,先在的垂线上取两点,使,再作出的垂线,使在一条直线上(如图所示),可以说明△≌△,得,因此
- 综合性学习水平考查( 7分)。 (1)节约是中华民族的传统美德,也是现代社会发展的需要。然而随着生活水平的提高,消费现象
- 正方形ABCD的边长为1,=a,=b,=c,则|a+b+c|等于( ) A.0 B.3
- 下列各组词语中,没有错别字的一组是A.庾毙 箫条 熟谙 狼籍 毛骨悚然B.丛冢 惫懒
- 光耀千古的唐朝文学,最为光彩夺目的是 A.散文 B.传奇 C.戏剧
- 阅读下面的文字,完成1-3题。 作为符号的丧家狗(节选) 陈壁生 北大教授李零评孔子为“丧家狗”,这一惹眼词
- 关于x的一元二次方程有两个不相等的实数根,则m的取值范围是A. B.



