溶液中溶质的质量分数及相关计算 知识点题库
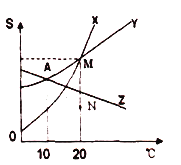
图是X、Y、Z三种物质的溶解度曲线,
(1)20℃时,X、Y、Z三种物质溶解度大小顺序是 ;
(2)20℃时,N点处物质X的溶液呈 (填“饱和”或“不饱和”);
(3)若X、Y、Z三种物质中,有一种是气态物质,则该物质是 .
-
(1) 30%的H2SO4和50%的H2SO4等质量混合后,所得溶液的质量分数(填“大于”、“小于”或“等于”)40%,如果等体积混合,混合后溶液的质量分数(填“大于”、“小于”或“等于”)40%.
-
(2) 已知98%的浓H2SO4的物质的量浓度为18.4mol•L﹣1 , 试判断49%的H2SO4的物质的量浓度(填“大于”、“小于”或“等于”)9.2mol•L﹣1 .
-
(1) 该盐酸的质量分数是多少?
-
(2) 取这种盐酸100.00mL,稀释到500.00mL,所得的稀盐酸的物质的量浓度为多少?
-
(1) 混合后溶液的质量分数.
-
(2) 混合后溶液的物质的量浓度.
-
(3) 在1 000g水中需溶解多少摩尔KNO3才能使其浓度恰好与上述混合后溶液的浓度相等?
-
(1) 原NaOH溶液的质量分数为.
-
(2) 所得溶液中Cl﹣的物质的量为mol.
-
(3) 所用氯气和参加反应的氢气的物质的量之比n(Cl2):n(H2)=.


-
(1) 该浓盐酸中HCl的物质的量浓度为。
-
(2) 某学生欲用上述浓盐酸和蒸馏水配制480 mL物质的量浓度为0.400 mol·L-1的稀盐酸。
可供选用的仪器有:①胶头滴管;②玻璃棒;③烧杯;④药匙;⑤量筒;⑥托盘天平。
请回答下列问题:
① 配制稀盐酸时,还缺少的仪器有 (写仪器名称);该仪器上标有以下五项中的;
A.温度 B.浓度 C.容量 D.压强 E.刻度线
②该学生需要量取 mL上述浓盐酸进行配制。
③在配制过程中,下列实验操作对所配制的稀盐酸物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面。()
b.量筒量取浓盐酸后又用蒸馏水洗涤2~3次,并将洗涤液移入容量瓶中。()
-
(3) ①假设该同学成功配制了0.400 mol·L-1的盐酸,他又用该盐酸中和含0.4 g NaOH的溶液,则该同学需取mL盐酸。
②假设该同学用新配制的盐酸中和含0.4 g NaOH的溶液,发现比①中所求体积偏小,则可能的原因是。
A.浓盐酸挥发,浓度不足 B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
-
(1) 该溶液中NaOH的物质的量浓度为。
-
(2) 该溶液中NaOH的质量分数为。
-
(3) 从该溶液中取出10mL,其中含NaOH的质量为。
-
(4) 将取出的10mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为。
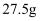 水中溶解
水中溶解 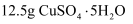 ,恰好达到饱和,该溶液密度为
,恰好达到饱和,该溶液密度为 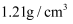 ,求:(要求有计算过程)
,求:(要求有计算过程)
-
(1) 该溶液中
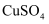 的质量分数是
的质量分数是
-
(2) 该溶液中
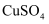 的物质的量浓度是(计算结果保留到小数点后两位)
的物质的量浓度是(计算结果保留到小数点后两位)
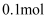 的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100mL水,搅拌,使固体全溶解,有甲、乙、丙、丁内溶液的溶质质量分数大小的顺序为( )
的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100mL水,搅拌,使固体全溶解,有甲、乙、丙、丁内溶液的溶质质量分数大小的顺序为( )
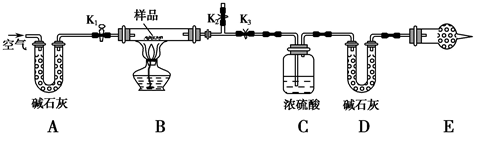
-
(1) 实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,检查气密性
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③关闭活塞K1、K2 , 打开K3 , 缓缓鼓入空气数分钟,目的是。
④关闭活塞K1、K2 , 打开K3 , 点燃酒精灯加热至不再产生气体。装置B中发生了能使装置D质量增加的化学方程式为。
⑤打开活塞K1 , 缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
-
(2) 关于该实验方案,请回答下列问题。
①E处干燥管中盛放的药品是,如果实验中没有该装置,则可能导致测量结果NaHCO3的质量分数(填“偏大”“偏小”或“无影响”)。
②有同学认为采用滴定法可以测得其中NaHCO3的质量分数,因此提出了以下方案:
准确称取纯碱样品Wg,放入锥形瓶中加蒸馏水溶解,加1~2滴酚酞指示剂,用物质的量浓度为c(mol/L)的HCl溶液滴至终点,所用HCl溶液体积为V1mL,再加1~2滴甲基橙指示剂,继续用HCl溶液滴至终点,所用HCl溶液体积为V2mL。写出该样品中NaHCO3质量分数的计算式:NaHCO3(%)=。
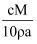 B . S=
B . S= 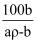 C . b=
C . b= 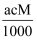 D . c=
D . c= 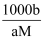
-
(1) 原22.4g混合物中CuSO4的质量
-
(2) 乙烧杯溶液中FeSO4的质量分数。
- 物块与竖直轻弹簧相连,放在水平地面上,一个物块由距弹簧上端点高处自由落下,落到弹簧上端后将弹簧压缩.为了研究物块下落的速
- 变形虫在细胞核被移除之后仍能消化已吞噬的食物,但不能摄取食物、也不能对外界刺激发生反应,电镜下观察到退化的高尔基体等细胞
- .已知m是8的相反数,n比m的相反数小2,求n比m大多少?
- 下列图示与对应的叙述不相符的是 选项 A. B. C. D. 图示 叙述 探究双氧水制氧气中MnO2的作用 将水通电电解
- 原子从a能级状态跃迁到b能级状态时发射波长为λ1的光子;原子从b能级状态跃迁到c能级状态时吸收波长为λ2的光子,已知λ1
- All these experiences have taught me a great deal about life
- 经济发展、劳动生产率的提高,会引导劳动力由第一产业向第二产业转移,再向第三产业梯次转移,出现劳动力在第一产业减少,在二三
- 1920年冬,列宁发现“广大农民群众不是自觉地而是本能地在情绪上反对我们”。后来列宁为此采取的措施是 A.采用余粮收集制
- There are a number of different ways to study a language, ea
- ---Was Tom in the chemistry lab when you arrived there? ---Y
- punish, approach, represent, nod, express, yawn,introduce, a
- 25℃时,在pH=13的溶液中可以大量共存的离子组是 A.K+、Na+、HC
- 如图,对称轴平行于y轴的抛物线与x轴交于(1,0),(3,0)两点,則它的对称轴为 .
- 下列关于基因工程的叙述,正确的是 A.基因工程经常以抗生素抗性基因为目的基因 B.细菌质粒是基因工程常用的运载体 C.通
- 下列各图反映的重大历史活动,哪些是专制决策的结果( ) ①长城 ②大运河 ③十三行④票号A.①②③
- 今年“两会”期间,网络媒体开通了“我有问题问总理”、“我向总理献一策”等栏目,上百万网民踊跃参与,各种提问和建言多达数万
- 下表为地球在公转轨道不同位置时公转速度的变化资料,据此比较北极和南极极夜持续天数( ) 时间 日地距离 角速度 线速度
- 当欧洲资产阶级革命以排山倒海之势冲击封建统治时,亚洲主要封建国家正在 A.日益觉醒,并掀起亚洲革命风暴 B.
- 北方民族尊唐太宗为“天可汗”的直接原因是( ) A.与吐蕃建立和亲关系 B.在西突厥故地设北庭都护府
- RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池,RFC工作原理见图.下列有关说法正确的是()A.转移0.1



