质量守恒定律 知识点题库
200℃时,11.6克CO2和水蒸气的混合气体与足量的Na2O2充分反应后,固体的质量增加了 3. 6克。从以上信息中,我们得出的下列结论中不正确的是( )
A . 可以计算出混合气体中CO2和水蒸气的质量
B . 可以判断出混合气体的平均摩尔质量
C . 可以计算出该反应中转移的电子数
D . 可以总结出Na2O2任何反应中既作氧化剂也作还原剂
某反应的微观示意图如下(一种小球代表一种元素的原子),下列说法错误的是( )
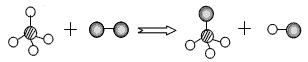
A . 该反应中共有三种元素
B . 图中反应物都是化合物
C . 该反应的本质是原子的重新组合
D . 该反应前后分子的种类发生改变
在化学反应中,反应前与反应后相比较,肯定不变的是( )
①元素的种类 ②如果在水溶液中反应,反应前与反应后阳离子所带的正电荷总数
③分子的数目 ④原子的数目 ⑤反应前物质的质量总和与反应后物质的质量总和.
A . ①③④
B . ②③⑤
C . ①④⑤
D . ②④⑤
在一个密闭的容器内有四种物质,高温下发生反应,一段时间后测得反应前后各物质的质量如下:
a | b | c | d | |
反应前质量(g) | 8 | 10 | 1 | 25 |
反应后质量(g) | 未测 | 24 | 2 | 16 |
若a的相对分子质量为2n,d的相对分子质量为3n,则该反应的化学方程式中a与d的化学计量数比为( )
A . 1:1
B . 1:2
C . 1:3
D . 2:3
美国”9.11”恐怖袭击事件中,毁坏的建筑物散发出大量的石棉,人吸入石棉纤维易患肺癌,石棉是硅酸盐矿物,某种石棉的化学式为:Ca2MgxSiyO22(OH)2 , 该化学式中的x,y的值分别是( )
A . 5,
B . 8,3
C . 3,8
D . 8,5
物质发生化学反应时,下列量值在反应前后肯定不发生变化的是( )
①电子总数; ②原子总数; ③分子总数; ④物质的种类;⑤物质的总质量;⑥物质所具有的总能量.
A . ①②⑤
B . ②⑤⑥
C . ①②③⑤
D . ①②⑤⑥
已知15gA物质和10.5gB物质恰好完全反应生成7.2gC、1.8gD和0.3molE,则E物质的摩尔质量是( )
A . 110g
B . 110g/mol
C . 55g/mol
D . 55
如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图.下列有关说法正确的是( )
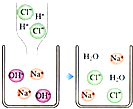
A . 反应前后,溶液的pH不变
B . 反应前后,Na+和Cl﹣的数目不变
C . 反应前后,H+和OH﹣的数目不变
D . 反应前后,H2O的数目不变
化学家李比希最早提出关于有机化合物中元素定量分析方法:用CuO作氧化剂(在氧气流中)将有机物氧化,再对产物进行分析,从而确定有机物的实验式.现取m g某种氨基酸(CxHyOzNp)在纯氧中完全燃烧,生成CO2、H2O和N2 . 实验在如图装置中进行:
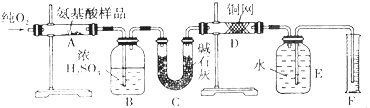
请回答下列问题:
-
(1) 实验开始时,先要通一段时间的氧气,其理由是.
-
(2) 装置图中需要加热的仪器有(用字母填空,下同),操作时应先点燃处的酒精灯.
-
(3) A装置中发生反应的化学方程式是.
-
(4) D装置的作用是.
-
(5) 读取N2的体积时,应注意:①;②.
-
(6) 实验中测得N2的体积为V mL(已折算成标准状况下).为确定此氨基酸的分子式,还需要的有关数据有 .A . 生成二氧化碳气体质量 B . 生成水的质量 C . 通入氧气的体积 D . 氨基酸的相对分子质量.
在反应式:a FeCl2 + b KNO3 + c HCl = d FeCl3 + e KCl + f X + g H2O中,若b=1,d=3,则X的分子式为( )
A . NO
B . N2
C . NO2
D . NH4Cl
将mg含氧化铁、氧化铜或氧化亚铁的样品投入物质的量浓度为1 mol/L的2 L盐酸中恰好完全反应,若向等质量的该样品中通入足量的氢气并加热,充分反应后所得金属的质量是 ( )
A . (m-16)g
B . (m+16)g
C . (m-32)g
D . 16g
下列说法正确的是( )
A . 1L0.1mol·L-1的氨水中含有的NH3与NH4+之和为0.1NA
B . 标准状况下,2.24LCCl4中含有的C—Cl键数为0.4NA
C . l0.0mL18 mol·L-1浓硫酸与足量铜反应,生成SO2的分子数为0.09NA
D . 标准状况下,Na2O2与足量CO2反应生成2.24LO2 , 转移电子数为0.2NA
标准状况下,a L氢气在过量的bL氯气中燃烧,所得混合物用100mL3.00mol·L-1的NaOH溶液恰好完全吸收,则氯气的体积b为( )
A . 2.24L
B . 4.48L
C . 3.36L
D . 1.12L
有两份质量相同的NaHCO3 , 向第一份中加入盐酸使其充分反应;将第二份加热使其完全分解,冷却至原温度再加入相同浓度的盐酸充分反应,则它们所耗用的盐酸的质量比为( )
A . 1∶1
B . 2∶1
C . 1∶2
D . 4∶1
中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃时反应制造出纳米级金刚石粉末和另一种化合物。该成果发表在世界权威的《科学》杂志上,被科学家们高度评价为“稻草变黄金"。下列有关说法中,你认为错误的是( )
A . Na的还原性强于金刚石
B . 另一种化合物是NaCl
C . 纳米级金刚石粉末属于胶体
D . 这个反应是置换反应
假设某化学反应的反应过程如图所示,观察分析,符合图中变化的化学反应为( )
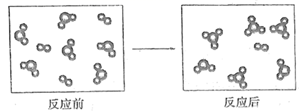
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取其工艺流程如图所示。
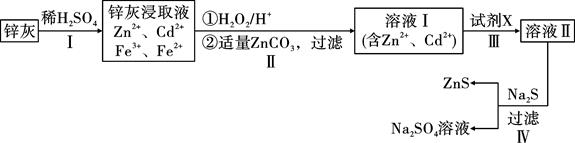
-
(1) 为提高锌灰的浸取率,可采用的方法是。
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
-
(2) 步骤Ⅱ所得滤渣中的物质是(写化学式)。
-
(3) 步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂X应为。
-
(4) 步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是;
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取,化学反应方程式为;
③已知Na2SO4·10H2O及Na2SO4的溶解度随温度变化的曲线如图,从滤液中得到Na2SO4·10H2O的操作方法是。
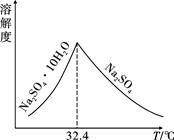
-
(5) 若步骤Ⅱ加入的ZnCO3为bmol,步骤Ⅲ所得Cd为dmol,最后得到VL、物质的量浓度为cmol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为。
(NH4)2Fe(SO4)2•6H2O俗称“摩尔盐”,是一种重要的化学试剂。当隔绝空气加热至500℃时,摩尔盐可完全分解,某小组欲探究其分解产物,设计实验如下,请回答:
-
(1) 该小组认为分解产物可能有以下几种情况:A . Fe2O3、SO3、NH3、H2O B . FeO、SO3、NH3、H2O C . FeO、SO2、NH3、H2O D . Fe2O3、SO2、SO3、NH3、H2O
经认真分析,确定猜想___________不成立(填序号);
-
(2) 为进一步确认分解产物,该小组设计了如下实验装置探究:
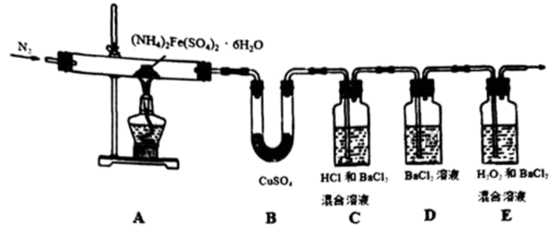 ①仪器B的名称为;
①仪器B的名称为;②加热前先通一段时间N2 , 加热至完全分解后再通入过量N2 , 实验过程中观察到装置D始终无明显现象,装置C和E均产生白色沉淀。
ⅰ.下列判断错误的是
A.C中的沉淀一定有BaSO4
B.C中的沉淀不可能含有BaSO3
C.加热至完全分解后再通入过量N2的目的是将分解产生的气体全部排到B、C装置中使其全部被吸收
D.D中无明显现象是因为SO2不能与BaCl2反应
ⅱ.写出E中所发生反应的化学方程式;
-
(3) 实验结束后,A中的固体变为红棕色,某同学猜测可能还有FeO,并设计实验验证:
第一步:该红色固体用溶解(填“盐酸”或“稀硫酸”);
第二步:为了检验是否存在Fe2+ , 向所得溶液中滴加试剂,观察是否褪色。
我国古代有“银针验毒”的记载。“银针验毒”的反应原理之一是:4Ag+2H2S+O2=2X+2H2O,下列有关该反应的说法正确的是( )
A . Ag得到电子
B . X为AgS
C . H2O是还原产物
D . 每生成1molX转移电子数4NA
工业上利用粗硅制备高纯硅可通过如下反应实现(反应均已配平),①Si+3HCl SiHCl3+X②SiHCl3+Y
SiHCl3+X②SiHCl3+Y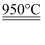 Si+3HCl,下列说法错误的是( )
Si+3HCl,下列说法错误的是( )
 SiHCl3+X②SiHCl3+Y
SiHCl3+X②SiHCl3+Y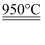 Si+3HCl,下列说法错误的是( )
Si+3HCl,下列说法错误的是( )
A . X、Y为同一种物质
B . 反应①②均为置换反应
C . 由反应①②可知单质硅和单质氢还原性相同
D . 反应①②均为氧化还原反应
最近更新
- 下列是我们日常生活中接触到的物质,其中属于纯净物的是( ) A.碘酒 B.蒸馏水 C.可
- 下列史书记载与秦始皇有关的是( ) ①“以法为教”,“以吏为师”,“严禁私学”②规定“统一车轨,修驰道”③“廿六年,皇
- 如图1-3-4所示为物体分子势能与分子间距离之间的关系.下列判断正确 的是( )图1-3-4 A.当r<r0
- _____ private cars are bringing us convenience, they may als
- 图中的外圆圈表示30°纬线圈,O为海洋,∠AOD=75°,读图回答下题。若劣弧AD表示2007年3月1日的范围,其余为2
- 下列物质基本组成单位相同的一组是 ( )
- 有一只粗细均匀、直径为d、电阻为r的光滑金属圆环水平放置在磁感应强度大小为B、方向竖直向下的匀强磁场中,其俯视图如图所
- 下列关于人体内环境的说法不正确的是() A.葡萄糖氧化分解不可能发生在人体内环境中 B.内环境稳态是指内环境的成分和理化
- 下列关于有机化合物的叙述不正确的是( ) A.三氯甲烷可以做麻醉剂,它和四氯化碳都是重要的有机溶剂 B.根据金属
- 下列燃料中属于可再生资源的是 A、煤 B、石油 C、天然气 D、
- 如图:P是∠的边OA上一点,且P点的坐标为(3,4),则sin=_____________.
- 如图所示,宽h=2cm的有界匀强磁场,纵向范围足够大,磁感应强度的方向垂直纸面向内,现有一群正粒子从O点以相同的速率沿纸
- 椭圆=1(a>b>0)与x轴正向交于A,若这个椭圆上总存在点P,使OP⊥AP(O为原点),求椭圆离心率的取值范围.
- 打气筒能将空气压入自行车胎内,主要是由于( ) A. 气体分子的大,易被压缩 B.分
- 研究甲状腺激素对小鼠的新陈代谢的影响(实验装置足以维持实验过程中小鼠的生命活动,瓶口密封,忽略水蒸气变化对实验结果的影响
- 用杂合子(DdEe)种子获得纯合子(ddee),最简捷的方法是( ) A.种植→F1→选双隐性者→纯合体
- 下表是某中年男子血液化验单中的部分数据:请根据所学知识判断下列叙述正确的是( ) A.该男子可能患有糖尿病,可服
- 读以北极为中心的地球部分示意图(AB为晨昏线,阴影部分为气压带),完成18~20题。18.图中甲所在地的气压带名称应该是
- 成年人体内,终生具有造血功能的红骨髓位于( ) A.骨膜 B.骨密质 C.骨松质
- I was in a rush as always, but this time it was for an impor



