化合价与化学式 知识点题库
XY2 是离子化合物,X和Y的离子的电子层结构与氖原子的相同,则X、Y为( )
A . Na和Cl
B . K和S
C . Ca和F
D . Mg和F
净水丸能对饮用水进行快速的杀菌消毒,药丸通常分内外两层.外层的优氯净 Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去;优氯净中氯元素的化合价为;无水亚硫酸钠隔绝空气加热到600℃便开始分解,分解产物是硫化钠和另一固体.请写出无水亚硫酸钠受热分解的反应方程式.
(1)将下列物质进行分类:①正丁烷与异丁烷、②红磷与白磷、③乙醇(CH3CH2OH)与二甲醚(CH3OCH3)
④金刚石和石墨、⑤冰与水、⑥16O与18O、⑦干冰与二氧化碳,用数字序号回答下列问题:
A.互为同素异形体的是
B.互为同分异构体的是
C.属于同位素的是
D.属于同一种化合物的是
(2)某元素最高正化合价为+6,其最低负价为 .某元素R与氢形成的气态氢化物的化学式为RH3 , 其最高价氧化物的化学式为 .
(3)试判断:①SiO2②CO2③KCl晶体的熔点由高到低排列的顺序: (填相应物质的编号).
铜在一定条件下也会生锈,其主要成分是铜绿,化学式为Cu2(OH)nCO3 , 式中n等于( )
A . 1
B . 2
C . 3
D . 4
X元素最高氧化物对应的水化物为H2XO3 , 则它对应的气态氢化物为( )
A . HX
B . H2X
C . XH3
D . XH4
某混合物甲中含有明矾[KAl(SO4)2·12H2O]、Al2O3和Fe2O3在一定条件下由甲可实现下图所示的物质之间的转化:
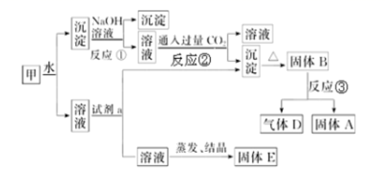
请回答下列问题:
-
(1) 写出A、B、D的化学式:A、B、D。
-
(2) 试剂a最好选用______(填字母)A . NaOH溶液 B . 稀盐酸 C . 二氧化碳 D . 氨水
-
(3) 写出反应①的离子方程式:
-
(4) 写出反应②中生成沉淀的化学方程式:。
-
(5) 固体E可以作为复合性的化学肥料,E所含物质的化学式为。
下列说法正确的是( )
A . MgO和Al2O3都属于两性氧化物
B . 悬浊液和乳浊液的分散质均为液态
C . Fe3O4和Pb3O4中的金属都呈现两种价态
D . 葡萄糖和淀粉都属于还原性糖
我们的生活离不开化学。化学物质在不同的领域发挥着重要的作用。
-
(1) 明矾是常用的一种净水剂,用离子方程式和相应的文字叙述解释其净水的原理:。
-
(2) 化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时发生如下分解反应:
2Mg5Al3(OH)19(H2O)4
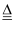 27H2O+10MgO+3Al2O3
27H2O+10MgO+3Al2O3写出该化合物作阻燃剂的两条依据:、。
-
(3) 焦亚硫酸钠(Na2S2O5)是一种常见的食品抗氧化剂,焦亚硫酸钠中硫元素的化合价为。
-
(4) 铵盐是重要的化肥,NH4Cl溶液中离子浓度大小顺序是。
-
(5) NaHCO3可以中和胃酸又是常用的食品添加剂,室温下pH=8的NaHCO3溶液中水电离出的OH-浓度为。
-
(1) 处于下列状态的物质中:①氯化钠晶体 ②干冰 ③HCl气体 ④铜 ⑤硫酸钡晶体 ⑥蔗糖 ⑦酒精 ⑧熔融的硝酸钾 ⑨NaCl溶液
能导电的是(填标号,下同);
属于电解质的是;
属于非电解质的是;
-
(2) 在一定条件下,RO
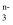 和I-可以发生反应,离子方程式为RO
和I-可以发生反应,离子方程式为RO 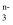 +6I-+6H+=R-+3I2+3H2O根据计算回答:
+6I-+6H+=R-+3I2+3H2O根据计算回答: ①RO
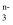 中n值为;
中n值为;②RO
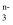 中元素R的化合价为。
中元素R的化合价为。③若R为氯元素,写出R的原子结构示意图
-
(3) 写出下列物质的电离方程式
H2SO4 :,
NaHCO3 :
KOH:
以物质的类别为横坐标,化合价为纵坐标绘制的图象叫价类图。如图是铁的价类图,Y物质为( )

A . FeO
B . Fe(OH)2
C . Fe3O4
D . FeSO4
如果用0.3 mol·L−1的亚硫酸钠溶液16mL,恰好将3.2×10−3mol的强氧化剂[RO(OH)2]2+溶液的溶质还原到较低价态。则反应后R的最终价态为( )
A . 0
B . +1
C . +2
D . +3
某元素X最高价含氧酸的化学式为HnXO2n-2 , 则在其气态氢化物中X元素的化合价为( )
A . 5n-2
B . 3n-12
C . 3n-6
D . n-10
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
-
(1) 写出化合物AC2的电子式;一种由B、C组成的化合物与AC2互为等电子体,其化学式为。
-
(2) E的核外电子排布式是,ECl3形成的配合物的化学式为。
-
(3)
 与
与 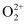 互为等电子体,1mol
互为等电子体,1mol 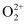 中含有的
中含有的  键数目为。
键数目为。
某元素的最高价含氧酸的阴离子符号是  ,则该元素的气态氢化物的化学式是( )
,则该元素的气态氢化物的化学式是( )
 ,则该元素的气态氢化物的化学式是( )
,则该元素的气态氢化物的化学式是( )
A . HR
B .  C .
C .  D . 不能确定
D . 不能确定
 C .
C .  D . 不能确定
D . 不能确定
铅丹能直接杀灭细菌、寄生虫,并有制止粘液分泌的作用,铅丹的主要成分中铅元素以不同的化合价存在,其化学式应为( )
A . PbO
B . Pb3O4
C . PbCl2
D . PbO2
某盐 A是由三种元素组成的化合物,某研究小组按如图流程探究其组成:
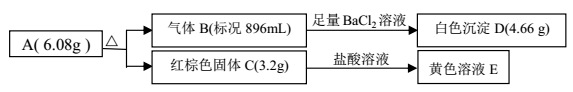
请回答:
-
(1) 写出红棕色固体 C 的化学式。
-
(2) 写出 A 受热分解反应的化学方程式。
-
(3) 写出气体 B 与溶液 E 反应的离子方程式。
镓与第VA 族元素形成的化合物是重要的半导体材料,应用最广泛的是砷化镓。
-
(1) 基态镓原子的核外电子排布简式为
-
(2) 镓失去电子的逐级电离能(kJ·mol-1)数值依次为577、1984.5、2961.8和 6192,由此可推知镓的主要化合价为 和+3价。砷的电负性比镓(填“大”成或”小”)。
-
(3) ①比较下列镓的卤化物的熔点和沸点,分析其变化规律及原因
镓的卤化物
GaCl3
GaBr3
GaI3
熔点/℃
77.75
122.3
211.5
沸点/℃
201.2
279
346
②GaF3的熔点超过1000℃,可能的原因是
A、B、C三种元素原子的最外层电子排布分别为3s1、2s22p3和2s22p4 , 由这三种元素组成的化合物的化学式可能是( )
A . ABC3
B . A2BC4
C . ABC2
D . A2BC3
氢化钠(NaH)可在野外用作生氢剂,有关的化学反应原理为NaH+H2O=NaOH+H2↑。下列关于该反应的说法中正确的是( )
A . NaH中H的化合价为+1
B . H2O是氧化剂,其中的氧元素被还原
C . NaH是还原剂,失去电子
D . 转移1mol电子时生成11.2L(标况)H2
-
(1) I.实验室常用浓盐酸与高锰酸钾发生反应快速制备少量氯气,该反应的化学方程式为:2KMnO4+16HCl(浓)=2MnCl2 + 2KCl + 5Cl2↑ + 8H2O,请回答以下问题:
上述化学反应方程式改写为离子方程式
-
(2) 该反应中氧化剂为(填化学式)。起酸作用的HCl与起还原作用的HCl的质量之比
-
(3) 已知在碱性溶液中可发生如下反应2R(OH)3+3ClO-+4OH-=2RO
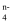 +3Cl-+5H2O,则RO
+3Cl-+5H2O,则RO 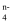 中R的化合价是___________
A . +3 B . +4 C . +5 D . +6
中R的化合价是___________
A . +3 B . +4 C . +5 D . +6 -
(4) II.我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质己略去)
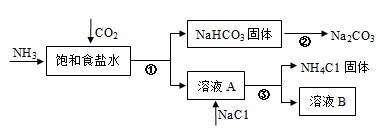
①②③所涉及的操作方法中,包含过滤的是(填序号)
-
(5) 根据上图,写出①中发生反应的化学方程式
-
(6) 煅烧NaHCO3固体的化学方程式是
最近更新
- 19.填入下面空白处的词语,最恰当的一组是(3分) 科学家有国籍,①科学无国界,让国籍不成为科学的羁绊,②不能成为科学家
- 当前,文化市场在满足人民日益增长的文化需要的同时,也出现了“娱乐化”“低俗化”的倾向。针对这种现象,在文化消费时我们应当
- 金属的下列性质,不能用金属晶体结构加以解释的是( ) A.易导电 B.易导热
- “送您一枝鲜花,请把火种留下。”2008年清明节,许多地方的市民以鲜花和植树等文明祭奠方式.取代了上坟烧纸.烧香烧花圈
- A Race Against Death It was a cold January in 1925 in Nome,
- The new comer is shy and never speaks until __________. A. a
- 下图甲表示某日昼长状况,乙是某地等高线示意图。读图完成下列问题。 甲
- 阅读下面这首唐诗,然后回答问题。 送友人入蜀 李白 见说蚕丛路,崎岖不易行。山从人面起,云傍
- 下列说法中,正确的是() A.家用电器着火,立即用水泼灭 B.日常生活中,用生石灰做干燥剂 C.发令枪中红磷燃烧时产生大
- 认为国家的主权属于人民,统治者的权力来自于人民,人民有权推翻那些违反民意,践踏公共意志的统治者的启蒙思想家是() A.卢
- 由细胞质核糖体合成的DNA聚合酶要进入细胞核内参与DNA的复制,其进入方式是( ) A.非跨膜运输
- 一根长为0.2m,电流为2A的通电导线,放在磁感应强度为0.5T的匀强磁场中,受到磁场力的大小不可能是() A.0.4N
- 已知,之间的一组数据:则与的回归方程必经过点 () A.(2,2) B.(1,3) C.(1.5
- 如果有,则.
- 用分子的性质解释下列生活中的现象,其中不正确的是() A.墙内开花墙外可嗅到花香,说明分子在不停地运动 B.湿衣服在阳光
- His winning the competition has ____ his confidence of himse
- 据最新研究发现,内皮素在皮肤中分布不均,是造成色斑的主要原因.内皮素拮抗剂进入皮肤,可以和黑色素细胞膜的受体结合,使内皮
- .抛物线如图所示,则它关于轴对称的抛物线的解析式是 .
- ......
- 用NA表示阿伏加德罗常数。下列叙述正确的是 ( ) A.2.0 g重水(2H2O)中含有的质子



