乙炔炔烃 知识点题库
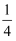 )mol
D . 在密闭容器中完全燃烧,150℃时测得的压强一定比燃烧前增加
)mol
D . 在密闭容器中完全燃烧,150℃时测得的压强一定比燃烧前增加
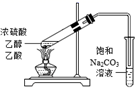
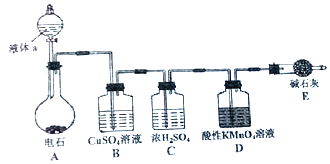
如图是某课外小组制取乙炔并测定乙炔的某些性质的实验.
-
(1) 写出实验室制取乙炔的化学方程式:
-
(2) 实验室制取乙炔时,分液漏斗中的液体a通常是
-
(3) CuSO4溶液的作用是
-
(4) 装置D中的现象是:
-
(5) 乙炔点燃之前必须进行的操作是
某化学兴趣
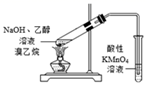
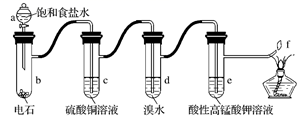
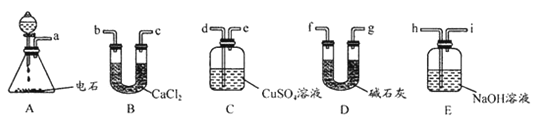 小组欲选用下列装置和药品制取纯净乙炔并进行有关乙炔性质的探究,试回答下列问题
小组欲选用下列装置和药品制取纯净乙炔并进行有关乙炔性质的探究,试回答下列问题
-
(1) (1)A中制取乙炔的化学反应方程式为: .
(2)制乙炔时,旋开分液漏斗活塞,使水缓慢滴下的原因是
(3)用电石制的乙炔中常含有H2S、PH3等杂质,除去杂质应选用 (填序号,下同)装置,气体应从 进;干燥乙炔最好选用 装置.(提示:PH3与CuSO4反应可生成Cu3P沉淀)
-
(2)
. 为了探究乙炔与HBr发生加成反应后的有关产物,进行以下实验:
纯净乙炔气
 混合液
混合液 有机混合物Ⅰ
有机混合物Ⅰ 混合液
混合液 有机混合物Ⅱ
有机混合物Ⅱ(1)操作b的名称是 ;
(2)有机混合物I可能含有的物质是 (写结构简式).
(3)最后得到的有机混合物Ⅱ中含两种有机物,其中一种是饱和一元醛,其结构简式为
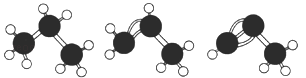
B . 相同物质的量的三种物质完全燃烧,生成的气体在标准状态下,体积比3:2:1
C . 丙烷、丙烯、丙炔三种物质的熔沸点逐渐升高,相同条件下密度逐渐增大
D . 丙炔的碳原予空间结构呈线性排列
B . 相同物质的量的三种物质完全燃烧,生成的气体在标准状态下,体积比3:2:1
C . 丙烷、丙烯、丙炔三种物质的熔沸点逐渐升高,相同条件下密度逐渐增大
D . 丙炔的碳原予空间结构呈线性排列
-
(1)
、第一种方案:请从图中选用适当的装置,设计一个实验,测定CaC2试样的纯度.
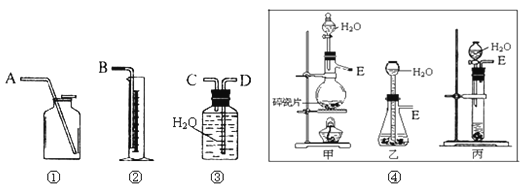
(1)制取C2H2最好选④中的 .所选用装置的连接顺序是(填各接口A~E的顺序): .
(2)若实验时称取的试样为1.4g,产生的乙炔在标准状况下的体积为448mL,此试样中CaC2的质量分数为
-
(2) 第二种方案:根据试样和水在锥形瓶中反应前后质量的变化,测定CaC2的质量分数.先称取试样1.6g、锥形瓶和水的质量为195.0g , 再将试样加入锥形瓶中,反应过程中每隔相同时间测得的数据如下表:
读数次数
质量/g
锥形瓶十水十试样
第1次
196.4
第2次
196.2
第3次
196.1
第4次
196.0
第5次
196.0
(3)计算CaC2的质量分数时,必需用的数据是 . 不必作第6次读数的原因是
-
(3)
第三种方案:称取一定质量的试样(1.6g),操作流程如下:
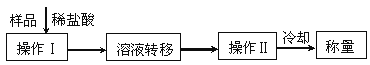
(4)操作Ⅱ的名称是 .
(5)要测定CaC2试样的纯度,还需知道的数据是 .
(6)在转移溶液时,如溶液转移不完全,则CaC2质量分数的测定结果 (填“偏大”、“偏小”或“不变”).
-
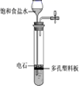
(1) 为了控制水与电石的反应速率并得到平稳气流,采取的措施是.
-
(2) 用试管制取少量乙炔时,在试管上部放置一团疏松的棉花,其作用是.
-
(3) 实验室制取下列气体时,不能使用启普发生器的是 .A . 用大理石和盐酸反应制CO2 B . 用电石与水反应制C2H2 C . 用锌粒和稀硫酸制H2 D . 用亚硫酸钠和硫酸制SO2 .
-
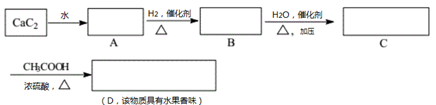
(1) 写出A,B,C,D的结构简式:A: B:C: D:
-
(2) A→B的化学反应方程式是,反应类型是。
-
(3) C→D的化学反应方程式是,反应类型是。
-
(4) B在一定条件下可生成聚合物,其化学方程式是,反应类型是。这种塑料会造成白色污染的原因是。
-
(5) A在一定条件下也可生成聚合物
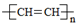 ,人们发现这种聚合物可以导电,从而具有巨大的应用前景。这一发现在思想观念上给我们的启示是。
,人们发现这种聚合物可以导电,从而具有巨大的应用前景。这一发现在思想观念上给我们的启示是。
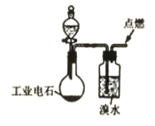
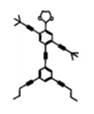
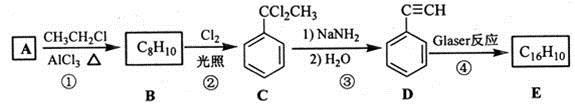
回答下列问题:
-
(1) B的结构简式为,D 的化学名称为。
-
(2) ①和③的反应类型分别为、。
-
(3) E的结构简式为。用1 mol E合成1,4−二苯基丁烷,理论上需要消耗氢气mol。
-
(4) 化合物(
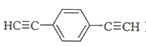 )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为。
-
(5) 芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中3种的结构简式。
-
(6) 写出用2−苯基乙醇为原料(其他无机试剂任选)制备化合物D的合成路线。
| | | | |
| A.制备并收集乙酸乙酯 | B.验证溴乙烷的消去产物是乙烯 | C.实验室制乙炔 | D.除去甲烷中的乙烯 |
-
(1) 乙炔水化法:在75℃左右,用
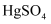 做催化剂,乙炔可水化为乙醛,但
做催化剂,乙炔可水化为乙醛,但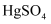 遇到某些特定物质常会发生催化剂中毒而失去催化作用,
遇到某些特定物质常会发生催化剂中毒而失去催化作用, 就是其中一种。实验装置如图所示
就是其中一种。实验装置如图所示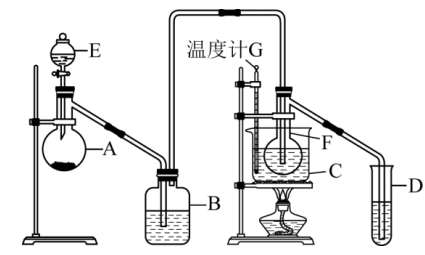
已知:F装置中已按顺序加入了氧化汞、水、浓硫酸。
①实验开始时,仪器A中盛放电石,B中应装。
②仪器D中盛放水,作用是,进一步提纯乙醛的操作是。
③装置图中,所选用温度计G的量程为(填标号)。
A.0~50℃ B.0~100℃ C.0~200℃
④请用化学方程式表示出装置F中的反应:。
-
(2) 乙烯氧化法:将乙烯、氧气和催化剂(
 和盐酸的混合溶液),在温度120~130℃,压力0.3MPa条件下,直接反应生成乙醛。下表是这两种方法的部分数据
和盐酸的混合溶液),在温度120~130℃,压力0.3MPa条件下,直接反应生成乙醛。下表是这两种方法的部分数据物质/项目
乙炔水化法
乙烯氧化法
平衡转化率
乙炔平衡转化率90%左右
乙烯平衡转化率80%左右
日产量
2.5吨(某设备条件下)
3.6吨(相同设备条件下)
从化学反应速率角度分析,在相同设备条件下,选用法制取乙醛快。
A | B | C |
①球棍模型为 ②能和Cl2在光照条件下反应生成多种氯代物 | ①能使溴水褪色 ②标准状况下,气体密度为1.25g•L-1 | ①能使溴水褐色 ②1molC能和2molH2发生加成反应 ③空间充填模型为 |
-
(1) 烃分子C的空间结构为。
-
(2) 三种烃中,和甲烷互为同系物的是(填结构简式,下同);完全燃绕,生成CO2和H2O的物质的量之比为1:1的是。
-
(3) 烃B能使溴水褪色,其原因为(用化学方程式表示),反应类型为。
-
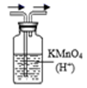
(4) 已知B和C具有相似的化学性质,将烃C通入少量酸性KMnO4溶液中的现象是。
- 下列有关基因工程的正确叙述是( ) A.重组DNA技术所用的工具酶是限制酶、DNA连接酶和运载体 B.所
- 如图5,斜面与质量为m的木块一起以加速度a竖直向上加速运动,斜面倾角为θ,重力加速度为g,求物体对斜面M的压力.
- 阅读下面这首唐诗,完成后面题。 白 帝 杜 甫 白帝城中云出门,白帝城下雨翻盆。 高江急峡雷霆斗,古木苍藤日月昏。 戎马
- 依次填入下列各句横线处的词语,恰当的一组是( ) (1)天地境界的人,其最高成就,是自己与宇宙__________
- 某块地在施用了含硼的微肥后,其增产效果显著,这是因为含硼的微肥有利于植物的( )A .受精作用 B .光合作
- 分解因式:2m3﹣8m= .
- 下列属于受非生物因素影响的是() A.螳螂捕蝉 B.秋风扫落叶 C.草盛豆苗稀 D.狐假虎威
- 阅读下面这首诗歌,回答后面的问题。 雨中同孟原佥宪登嘉鱼亭① 明蓝智 高阁流莺外,荒城驻马前。 江寒三月雨,春老百蛮②天
- 如图表示某一健康人注射疫苗前后、不同时间采血所测得的抗体水平(箭头表示疫苗注射时间)。下列叙述错误的是 ()。A.b段各
- ----I can’t find Mr.Brown.Where did you meet him this mornin
- 下图是氮循环以及氮在生物体内的转化过程示意图,下列说法错误的是A.完成⑦⑧过程的生物在生态系统的成分中属于分解者 B.完
- 太傅袁隗欲以女妻范,范辞不受。 译文:_________________________________
- 下列句子中,没有语病的一项是()A.作为一种新兴的教育模式,跨文化、体验式游学已经成为一种时尚,受到学生和家长的普遍欢迎
- 如图,正四棱柱中,底面边长为,侧棱长为4,点分别为棱的中点,,求点到平面的距离.
- 向20g氯化钡溶液中,逐滴加入一定量9.8%的硫酸溶液至恰好完全反应,生成沉淀质量为2.33g。请计算: (1)欲配制1
- 一射击运动员一次射击练习的成绩是(单位:环):7,10,9,9,10,这位运动员这次射击成绩的平均数是
- 如图所示,图线a是线圈在匀强磁场中匀速转动时所产生正弦交流电的图象,当调整线圈转速后,所产生正弦交流电的图象如图线b
- 白血病是由于造血干细胞增殖分化异常而引起的恶性增殖疾病。目前治疗白血病的主要方法是骨髓移植,但骨髓配型的成功率较低,大大
- 下列关于几种运输方式速度的叙述,正确的是 ( ) A.空运最快、水运最慢
- 从下面两个作文题中,任选其一,按要求作文。 题目一:请以“感谢一路有你”为题写一篇文章。 题目二:美无处不有,美无时不在