分子间作用力与物质的性质 知识点题库
将下列晶体熔化:NaOH、SiO2、CaO、CCl4 , 需要克服的微粒间的相互作用①共价键②离子键③分子间作用力,正确的顺序是( )
A . ②①②③
B . ①②②③
C . ②③②①
D . ①①②③
下列变化需克服相同类型作用力的是( )
A . 碘和干冰的升华
B . 硅和C60的熔化
C . 氯化氢和氯化钠的溶解
D . 液溴和液汞的汽化
下列说法中,不正确的是( )
A . 干冰升华,克服的是CO2的分子间作用力
B . 碳原子间连接方式的多样性,是含碳化合物种类繁多的原因之一
C . 在N2、CO2和SiO2物质中,都存在共价键,它们都是由分子构成
D . NH4Cl属于离子化合物,该物质中存在离子键和共价键
下列说法正确的是( )
A . 金属与非金属元素形成的化合物一定是离子化合物
B . 干冰气化过程中只需克服分子间作用力
C . HF的热稳定性很好,是因为HF分子间存在氢键
D . 常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构
下列物质发生变化时,所克服的粒子间相互作用属于分子间作用力的是( )
A . 酒精受热变为气体
B . 氯化铵受热变为气体
C . 二氧化硅受热熔化
D . 食盐溶解在水中
一种芳纶纤维的拉伸强度比钢丝还高,广泛用作防护材料。其结构片段如下图
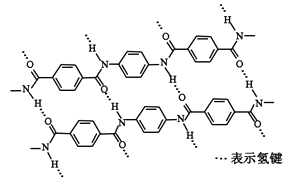
下列关于该高分子的说法正确的是( )
A . 完全水解产物的单个分子中,苯环上的氢原子具有不同的化学环境
B . 完全水解产物的单个分子中,含有官能团一COOH或一NH2
C . 氢键对该高分子的性能没有影响
D . 结构简式为: 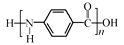
短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数是次外层的2倍,Y的氟化物YF3分子中各原子均达到8电子稳定结构,Z是同周期中原子半径最大的元素,W的最高正价为+7价。下列说法正确的是()
A . XH4的沸点比YH3高
B . X与W形成的化合物和Z与W形成的化合物的化学键类型相同
C . 元素W的最高价氧化物对应水化物的酸性比Y的弱
D . X与Y形成的化合物的熔点可能比金刚石高
下列说法正确的是( )
A . 碘晶体受热变成蒸汽,吸收的热量用于克服碘原子间的作用力
B . 金刚石、富勒烯、干冰都是由共价键形成的原子晶体
C . HCl溶于水后,化学键被破坏,形成水合离子
D . CH4、PCl3分子中各原子均达到8电子稳定结构
铁氮化合物(  )在磁记录材料领域有着广泛的应用前景。某
)在磁记录材料领域有着广泛的应用前景。某  的制备需铁、氮气、丙酮和乙醇参与。
的制备需铁、氮气、丙酮和乙醇参与。
 )在磁记录材料领域有着广泛的应用前景。某
)在磁记录材料领域有着广泛的应用前景。某  的制备需铁、氮气、丙酮和乙醇参与。
的制备需铁、氮气、丙酮和乙醇参与。
-
(1)
 基态核外电子排布式为。
基态核外电子排布式为。
-
(2) 丙酮(
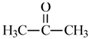 )分子中碳原子轨道的杂化类型是,1mol丙酮分子中含有σ键的数目为。
)分子中碳原子轨道的杂化类型是,1mol丙酮分子中含有σ键的数目为。
-
(3) C,H,O三种元素的电负性由小到大的顺序为。
-
(4) 乙醇的沸点高于丙酮,这是因为。
-
(1) 比较相同条件下微粒得到电子的能力Fe3+Cu2+(填“>” 、“<”或“=”)
-
(2) 已知Mg3N2遇水会剧烈反应生成白色沉淀和有刺激性气味的气体,写出Mg3N2与足量稀盐酸反应的化学方程式。
-
(3) 相同条件下冰的密度比水小,主要原因是 。
下列说法错误的是( )
A . 华为“麒麟990”手机芯片的主要成分是晶体硅
B . 新冠病毒DNA分子内存在氢键,氢键具有方向性和饱和性
C . 血红蛋白的载氧能力是通过分子中的Fe2+与O2形成离子键来实现的
D . 紫外线能使蛋白质分子中的C-C、C-N等化学键断裂,从而损伤皮肤
下列对分子结构及其性质的解释中,错误的是( )
A . 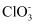 与
与  中心原子的价层电子对数相同
B . 液态氟化氢的化学式有时写成(HF)n的形式与氢键有关
C . 碘易溶于四氯化碳、甲烷难溶于水都可用相似相溶原理解释
D . 酸性:H3PO4>HClO,是因为H3PO4分子中氢原子数比HClO的多
中心原子的价层电子对数相同
B . 液态氟化氢的化学式有时写成(HF)n的形式与氢键有关
C . 碘易溶于四氯化碳、甲烷难溶于水都可用相似相溶原理解释
D . 酸性:H3PO4>HClO,是因为H3PO4分子中氢原子数比HClO的多
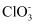 与
与  中心原子的价层电子对数相同
B . 液态氟化氢的化学式有时写成(HF)n的形式与氢键有关
C . 碘易溶于四氯化碳、甲烷难溶于水都可用相似相溶原理解释
D . 酸性:H3PO4>HClO,是因为H3PO4分子中氢原子数比HClO的多
中心原子的价层电子对数相同
B . 液态氟化氢的化学式有时写成(HF)n的形式与氢键有关
C . 碘易溶于四氯化碳、甲烷难溶于水都可用相似相溶原理解释
D . 酸性:H3PO4>HClO,是因为H3PO4分子中氢原子数比HClO的多
铜是人类最早发现并广泛使用的一种金属。回答下列问题:
-
(1) 黄铜矿(CuFeS2)是其中铜的主要存在形式。CuFeS2中存在的化学键类型是。试比较组成黄铁矿的三种组成元素的电负性的相对强弱。
-
(2) 在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①则X是(填名称),X分子的立体构型是,中心原子杂化类型为。
②X的沸点比水的沸点(填“高”、“低"),主要原因是。
-
(3) [Cu(NH3)4]2+中,提供孤对电子的是。Cu(NH3)2Cl2有两种同分异构体,其中种可溶于水,则此种化合物是(填“极性"或“非极性")分子,由此推知[Cu(NH3)4]2+的空间构型是。
-
(4) 某镍白铜合金的立方品胞结构如图所示:
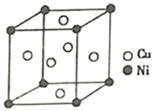
①晶胞中铜原子与镍原子的数量比为。
②若合金的密度为d g/cm3 , 品胞参数a=nm。(设NA代表阿伏加德罗常数)
下列有机物相关说法正确的是( )
A . 氨基酸和蛋白质分子中均含有酰胺键
B . 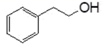 与
与 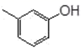 互为同系物
C . 按系统命名法,化合物
互为同系物
C . 按系统命名法,化合物  的名称是2,3,3,5,5-五甲基-4-乙基己烷
D .
的名称是2,3,3,5,5-五甲基-4-乙基己烷
D . 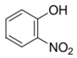 比
比 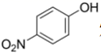 熔沸点低,是因为前者形成分子内氢键
熔沸点低,是因为前者形成分子内氢键
 的名称是2,3,3,5,5-五甲基-4-乙基己烷
D .
的名称是2,3,3,5,5-五甲基-4-乙基己烷
D .  比
比  熔沸点低,是因为前者形成分子内氢键
熔沸点低,是因为前者形成分子内氢键
教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
-
(1) 第三周期的某主族元素,其第一至第五电离能数据如图所示,则该元素对应的原子有种不同空间运动状态的电子。
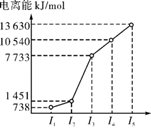
-
(2) 如图所示,每条折线表示周期表ⅣA ~ⅦA 中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中 a 点代表的是。判断依据是。
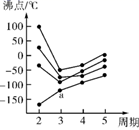
-
(3) CO2 在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于晶体。
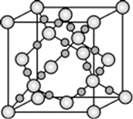
-
(4) 第一电离能介于 Al、P 之间的第三周期元素有种。 GaCl3 中中心原子的杂化方式为,写出与 GaCl3 结构相同的一种离子。
-
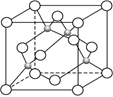
(5) 下图是碳化硅的晶胞结构 。若碳化硅晶胞边长为 apm,阿伏加德罗常数为 NA ,则碳化硅晶体的密度为g/cm3.(列出计算式即可)
德国科学家发现新配方:他使用了远古地球上存在的  、
、  、
、  、
、  、
、  和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法错误的是( )
和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法错误的是( )
 、
、  、
、  、
、  、
、  和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法错误的是( )
和HCN,再使用硫醇和铁盐等物质合成RNA的四种基本碱基。下列说法错误的是( )
A . 基态  价电子排布为
价电子排布为  B .
B .  、
、  、
、  分子间均存在氢键
C .
分子间均存在氢键
C .  、
、  、HCN中均存在
、HCN中均存在  键和
键和  键
D . 沸点:
键
D . 沸点:  (乙硫醇)>
(乙硫醇)> 
 价电子排布为
价电子排布为  B .
B .  、
、  、
、  分子间均存在氢键
C .
分子间均存在氢键
C .  、
、  、HCN中均存在
、HCN中均存在  键和
键和  键
D . 沸点:
键
D . 沸点:  (乙硫醇)>
(乙硫醇)> 
近年来,科学家研究的以复合过渡金属镍的氢氧化物为催化剂、三乙醇胺为电子给体以及  为光敏剂的催化体系,在可见光驱动下可高效催化还原
为光敏剂的催化体系,在可见光驱动下可高效催化还原  。
。
 为光敏剂的催化体系,在可见光驱动下可高效催化还原
为光敏剂的催化体系,在可见光驱动下可高效催化还原  。
。
-
(1) 下列有关
 原子的叙述正确的是___________ (填标号)。
A . 第一电离能比钙的大 B . 基态
原子的叙述正确的是___________ (填标号)。
A . 第一电离能比钙的大 B . 基态 原子的核外价电子排布式为
原子的核外价电子排布式为 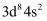 C . 基态
C . 基态 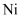 原子形成基态
原子形成基态 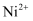 时,先失去
时,先失去 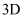 轨道上的电子
轨道上的电子
-
(2) 三乙醇胺的制备:3

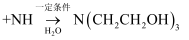 。
。 ①三乙醇胺所含的元素中,电负性由小到大的顺序为。
②
 的空间结构为。
的空间结构为。③键角:
 (填“
(填“ 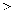 ”、“
”、“ 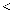 ”或“
”或“  ”)
”)  。
。 -
(3)
 能转化为高价值化学品,如
能转化为高价值化学品,如  、
、  、
、 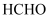 。上述3种物质中,沸点最高的是
。上述3种物质中,沸点最高的是  ,原因是。
,原因是。
-
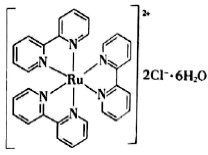
(4)
 的结构如图所示。
的结构如图所示。 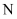 原子的杂化类型为,
原子的杂化类型为, 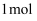 配体
配体 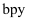 分子中含有
分子中含有  键的数目为
键的数目为  。
。 
-
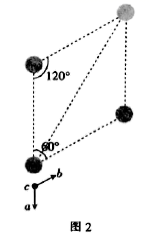
(5)
 的晶胞结构如图1(氧、氢原子均位于晶胞内部)所示,图2是晶胞正上方的俯视投影图,请在图2中用空心球(○)表示氧原子的位置。已知晶胞的底边长为
的晶胞结构如图1(氧、氢原子均位于晶胞内部)所示,图2是晶胞正上方的俯视投影图,请在图2中用空心球(○)表示氧原子的位置。已知晶胞的底边长为 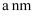 ,高为
,高为 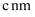 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为  ,则该晶胞的密度为
,则该晶胞的密度为 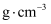 (列出表达式)。
(列出表达式)。 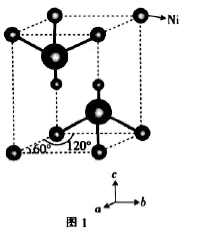
-
(1) 铜与类卤素(SCN)2反应生成Cu(SCN)2 , 1mol(SCN)2中含有π键的数目为; 类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H-S-C
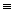 N)的沸点低于异硫氰酸(H-N=C=S)的沸点,其原因是 。
N)的沸点低于异硫氰酸(H-N=C=S)的沸点,其原因是 。
-
(2) H2O2与H2O可以以任意比例互溶,除因为它们都是极性分子外,还因为。
-
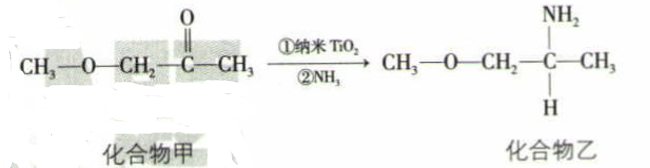
(3) 纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如图所示,化合物甲中碳原子的杂化方式为,组成化合物乙的所有元素的第一电离能由大到小的顺序为。化合物乙的沸点明显高于化合物甲,主要原因是。
化合物Z是一种具有广谱抗菌活性的药物,其合成反应如图。下列说法错误的是( )
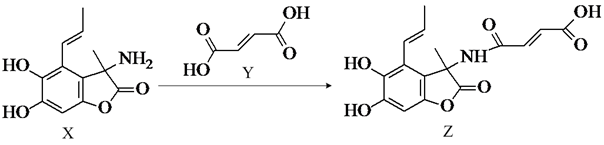
A . X分子间只能形成下列氢键:O-H…O、N-H…N
B . 1molZ最多能与6molNaOH反应
C . Z分子中含2个手性碳原子
D . X、Y、Z三种分子均存在顺反异构体
下列两组命题中,M组命题能用N组命题加以解释的是( )
选项 | M组 | N组 |
A | 酸性强弱:三氟乙酸>三氯乙酸 | F的电负性大于Cl的电负性,导致三氟乙酸羧基中的羟基的极性更大 |
B |
| 因为 |
C |
|
|
D | HI的沸点比HCl的高 | H-I键的键能大于H-Cl键的键能 |
A . A
B . B
C . C
D . D
最近更新
- 玉米和蝗虫个体发育的起点分别是( ) A.受精卵、受精卵 B.精子、受精卵 C.卵细胞、受精卵 D.
- .That’s such a good radio _____ almost every one wants to bu
- 一长直铁芯上绕有一固定线圈M,铁芯右端与一木质圆柱密接,木质圆柱上套有一闭合金属环N,N可在木质圆柱上无摩擦移动。M连接
- 单项选择 —I have never been to Tibet. What about you, Tina?—Me .
- 下列关于植物组织培养的叙述中,正确的是 ( ) A.培养基中添加蔗糖的目的是提供营养和
- (8分)PtCl2(NH3)2可以形成两种固体,一种为淡黄色,在水中的溶解度小,另一种为黄绿色,在水中的溶解度较大,请回
- Everybody has one of those days when everything goes wrong.
- 下图表示的是在最适温度下,反应物浓度对唾液淀粉酶所催化的化学反应速率的影响。下列有关说法正确的是( )A.若在A
- 元素性质呈周期性变化的决定因素是() A.元素原子半径大小呈周期性变化 B.元素相对原子质量依次递增 C.元素原子最外层
- --Mary knows the city quite well. --She______ well have been
- 2006年4月26日是前苏联切尔诺贝利核泄漏事故20周年纪念日。20年前,切尔诺贝利核电站4号反应堆发生爆炸,大量强辐射
- 我市在各校推广大阅读活动,初二(1)班为了解2月份全班学生课外阅读的情况,调查了全班学生2月份读书的册数,并根据调查结果
- 在原子反应堆中抽动液态金属或在医疗器械中抽动血液等导电液体时,常使用电磁泵.某种电磁泵的结构如图6-1-4所示,把装有液
- We usually go to school on weekdays, and sometimes g
- 如图是细胞中多聚核糖体合成多肽链的过程.对此过程的理解错误的是() A. 合成过程的模板是脱氧核糖核酸,原料
- 已知函数f(x)=x+2x,g(x)=x+lnx,h(x)=x--1的零点分别为x1,x2,x3,则x1,x2,x3的大
- —I think students should have mobile phones to call their pa
- 依法执政和依法治国的联系是() A. 都是党领导人民治理国家的基本方略 B. 本质都是保证人民当家作主 C. 本质
- 有六张完全相同的卡片,其正面分别标有数字:﹣2,,π,0,,3.,将它们背面朝上洗匀后,从中随机抽取一张卡片,则其正面的
- 致富是令人神往的,但通向致富的道路是坎坷的。纵观古今中外的致富者,哪一个不是历尽磨难?如果致富的路上都是一帆风顺,都能一
 的稳定性大于
的稳定性大于



