超分子 知识点
超分子: 超分子通常是指由两种或两种以上分子依靠分子间相互作用结合在一起,组成复杂的、有组织的聚集体,并保持一定的完整性使其具有明确的微观结构和宏观特性。
超分子 知识点题库
2016年诺贝尔化学奖授予在合成分子机器领域做出贡献的三位科学家。分子机器是一种特殊的超分子体系,当体系受到外在刺激(如pH变化、吸收光子、电子得失等)时,分子组分间原有作用被破坏,各组分间发生类似于机械运动的某种热运动。下列说法错误的是( )
A . 驱动分子机器时,需要对体系输入一定的能量
B . 分子状态的改变会伴随能量变化,属于化学变化
C . 氧化还原反应有可能是刺激分子机器体系的因素之一
D . 光照有可能使分子产生类似于机械运动的某种热运动
下列说法错误的是( )
A . 气态和液态物质都是由分子构成的
B . 超分子的重要特征是分子识别和自组装
C . 大多数晶体都是四种典型晶体之间的过渡晶体
D . 石墨晶体中既有共价键和范德华力又有类似金属的导电性属于混合型晶体
下列关于物质特殊聚集状态的叙述中,不正确的是( )
A . 在电场存在的情况下,液晶分子沿着电场方向有序排列
B . 非晶体的内部原子或分子的排列杂乱无章
C . 液晶最重要的用途是制造液晶显示器
D . 由纳米粒子构成的纳米陶瓷有极高的硬度,但低温下不具有优良的延展性
下列说法不正确的是( )
A . 纳米颗粒界面通常为无序结构,但内部具有晶状结构
B . 利用红外光谱实验可确定青蒿素分子中含有的部分基团
C . 超分子内部分子之间通过氢键、弱配位键等相结合
D . 电子表液晶显示器在施加电场时,液晶分子沿垂直于电场方向排列
某课题组设计合成的双(β-二酮)钛(Ⅳ)配合具有抗肿瘤作用,合成路线如下:
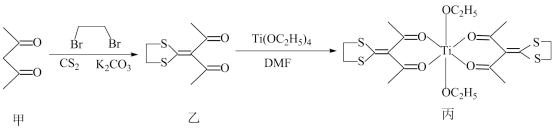
下列说法正确的是( )
A . 乙的分子式为C8H8O2S2
B . K2CO3中阴离子的VSEPR模型为正四面体形
C . 物质甲中含σ键和Π键的数目之比为7:1
D . 丙中Ti的配位数为4
下列说法正确的是( )
A . 破损的晶体能够在固态时自动变成规则的多面体
B . 利用超分子的分子识别特征,可以分离 和
和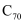 C . 金属晶体能导电的原因是金属阳离子在外加电场作用下可发生定向移动
D . 在沸水中配制明矾饱和溶液,然后急速冷却,可得到较大颗粒明矾晶体
C . 金属晶体能导电的原因是金属阳离子在外加电场作用下可发生定向移动
D . 在沸水中配制明矾饱和溶液,然后急速冷却,可得到较大颗粒明矾晶体
 和
和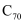 C . 金属晶体能导电的原因是金属阳离子在外加电场作用下可发生定向移动
D . 在沸水中配制明矾饱和溶液,然后急速冷却,可得到较大颗粒明矾晶体
C . 金属晶体能导电的原因是金属阳离子在外加电场作用下可发生定向移动
D . 在沸水中配制明矾饱和溶液,然后急速冷却,可得到较大颗粒明矾晶体
科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种具有高效催化性能的超分子,其分子结构示意图如图所示(注:实线代表共价键,其他重复单元的W、X未标注)。W、X、Z分别位于不同周期,Z的原子半径在同周期元素中最大。下列说法不正确的是( )
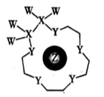
A . Y的单质的氧化性在同主族中最强
B . 简单离子半径: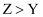 C . Z与Y可形成多种离子化合物
D . 简单氢化物的热稳定性;
C . Z与Y可形成多种离子化合物
D . 简单氢化物的热稳定性;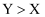
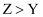 C . Z与Y可形成多种离子化合物
D . 简单氢化物的热稳定性;
C . Z与Y可形成多种离子化合物
D . 简单氢化物的热稳定性;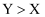
科学家预言超级原子的发现将会重建周期表,2005年1月美国科学家在《Science》上发表论文,宣布发现Al的超原子结构Al13和Al14 , Al13、Al14的性质很像现行周期表中的某主族元素,已知这类超原子当具有40个价电子时最稳定。下列说法正确的是( )
A . Al13、Al14互为同位素
B . All4与ⅡA族元素性质相似
C . Al13和Al14都具有强还原性,容易失去电子生成阳离子
D . Al13超原子中Al原子间是通过离子键结合的
美国《Science》上发表论文,宣布发现了一种 Al 的超原子结构,这种超原子(Al13)是以 1 个 Al 原子 在中心,12 个 Al 原子在表面形成的三角二十面体结构。这种超原子具有 40 个价电 子(价电 子即主族元 素的最外层电子数)时最稳定。请预测稳定的 Al13 所带的电荷为( )
A . -1
B . +2
C . +3
D . 0
在10﹣9m~10﹣7m范围内,对原子、分子进行操纵的纳米超分子技术往往能实现意想不到的变化。纳米铜颗粒一遇到空气就会剧烈燃烧,甚至发生爆炸,下列说法正确的是( )
A . 纳米铜是一种新型胶体
B . 纳米铜颗粒比普通铜更易与氧气发生反应
C . 纳米铜与普通铜所含铜原子的种类不同
D . 纳米铜无需密封保存
下列说法不正确的是( )
A . 离子液体有难挥发的特点,常被用于有机合成的溶剂
B . 冠醚与碱金属离子通过离子键形成超分子
C . 等离子体是一种特殊的气体,由带电的阳离子、电子及电中性粒子组成
D . 液晶既具有液体的流动性,又具有类似晶体的各向异性
超分子化学已逐渐扩展到化学的各个分支,还扩展到生命科学和物理学等领域。由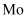 将2个
将2个 分子、2个
分子、2个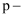 甲酸丁酯吡啶分子及2个
甲酸丁酯吡啶分子及2个 分子利用配位键自组装的超分子结构如图所示。
分子利用配位键自组装的超分子结构如图所示。
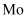 将2个
将2个 分子、2个
分子、2个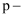 甲酸丁酯吡啶分子及2个
甲酸丁酯吡啶分子及2个 分子利用配位键自组装的超分子结构如图所示。
分子利用配位键自组装的超分子结构如图所示。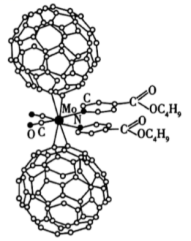
-
(1)
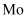 位于第5周期ⅥB族,基态原子核外电子排布与
位于第5周期ⅥB族,基态原子核外电子排布与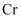 相似,则基态
相似,则基态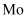 原子的价电子排布式为;核外未成对电子数为。
原子的价电子排布式为;核外未成对电子数为。
-
(2) 该超分子中存在的化学键类型有____(填字母)。A .
 键
B . π键
C . 离子键
D . 氢键
键
B . π键
C . 离子键
D . 氢键
-
(3) 配体
 中提供孤电子对的原子是(填元素符号);
中提供孤电子对的原子是(填元素符号);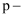 甲酸丁酯吡啶配体中C原子的杂化方式有。
甲酸丁酯吡啶配体中C原子的杂化方式有。
-
(4) 从电负性角度解释
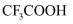 的酸性强于
的酸性强于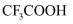 的。
的。
-
(5)
 与金刚石互为同素异形体,从结构与性质的关系角度解释
与金刚石互为同素异形体,从结构与性质的关系角度解释 的熔点远低于金刚石的原因。
的熔点远低于金刚石的原因。
下列有关超分子的说法错误的是( )
A . 超分子是由两种或多种分子形成的聚集体
B . 分子形成超分子的作用可能是分子间作用力
C . 超分子具有分子识别的特性
D . 分子以共价键聚合形成超分子
-
(1) I.超分子化学已逐渐扩展到化学的各个分支,还扩展到生命科学和物理学等领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。
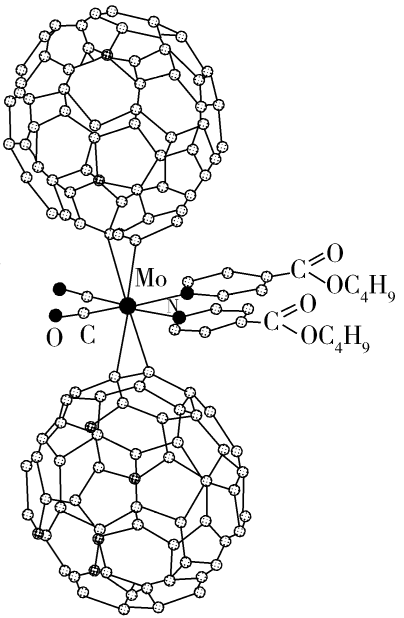
Mo处于第五周期第VIB族,核外电子排布与Cr相似,它的基态价电子排布式是;核外未成对电子数是个。
-
(2) 该超分子中存在的化学键类型有____。A . σ键 B . π键 C . 离子键 D . 氢键
-
(3) 该超分子中配体CO提供孤电子对的原子是(填元素符号)。
-
(4) C60与金刚石互为同素异形体,从结构与性质之间的关系解释C60的熔点远低于金刚石的原因是。
-
(5) II.开发新型储氢材料是氢能利用的重要研究方向。
Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。基态原子Ti有种能量不同的电子。Li、B、H元素的电负性由大到小排列顺序为。
-
(6) NaH具有NaCl型晶体结构。已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H-的半径为,NaH的理论密度是g·cm-3(只列算式,不必计算出数值,阿伏加德罗常数的值为NA)。
下列关于物质特殊聚集状态结构的叙述中,错误的是( )
A . 超分子是由两个或多个分子相互“组合”在一起形成具有特定结构和功能的聚集体,能表现出不同于单个分子的性质
B . 非晶体基本构成微粒的排列是长程无序和短程有序的
C . 液晶内部分子沿分子长轴方向有序排列,使液晶具有各向异性
D . 纳米晶体具有不同于大块晶体特性的原因是晶体的表面积减小
下列关于物质特殊聚集状态结构的叙述中,错误的是( )
A . 等离子体的基本构成微粒是带电的离子和电子及不带电的分子或原子
B . 超分子内部分子之间可以通过非共价键结合
C . 液晶内部分子沿分子长轴方向有序排列,使液晶具有各向异性
D . 纳米材料包括纳米颗粒与颗粒间的界面两部分,两部分都是长程有序
下列说法错误的是( )
A . 某些金属盐灼烧呈现不同焰色是因为电子从高能轨道跃迁至低能轨道释放不同波长的光
B . 超分子具有分子识别和自组装的特征
C .  右上角的3表示该能级有3个轨道
D .
右上角的3表示该能级有3个轨道
D .  的VSEPR模型和离子的空间构型一致
的VSEPR模型和离子的空间构型一致
 右上角的3表示该能级有3个轨道
D .
右上角的3表示该能级有3个轨道
D .  的VSEPR模型和离子的空间构型一致
的VSEPR模型和离子的空间构型一致
下列说法错误的是( )
A . 利用超分子的分子识别特征,可以用“杯酚”和甲苯、氯仿等分离 和
和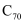 B . 某元素气态基态原子的逐级电离能(
B . 某元素气态基态原子的逐级电离能(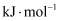 )分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是
)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是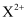 C . 晶体与非晶体的本质区别是有无固定熔点
D .
C . 晶体与非晶体的本质区别是有无固定熔点
D .  的分子立体构型为
的分子立体构型为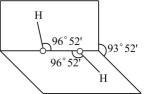 , 由此可知
, 由此可知 为极性分子
为极性分子
 和
和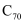 B . 某元素气态基态原子的逐级电离能(
B . 某元素气态基态原子的逐级电离能(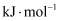 )分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是
)分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是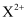 C . 晶体与非晶体的本质区别是有无固定熔点
D .
C . 晶体与非晶体的本质区别是有无固定熔点
D .  的分子立体构型为
的分子立体构型为 , 由此可知
, 由此可知 为极性分子
为极性分子
下列有关物质结构与性质的叙述正确的是( )
A . 等离子体是只由离子组成的具有带电性的气态物质
B . 1molCo3+的八面体配合物[CoClx(NH3)y]Clz与足量AgNO3溶液作用生成2molAgCl沉淀,则x、y、z的值分别为2、4、2
C . 若MgO的化学键中离子键的百分数为50%,则MgO可看作离子晶体与共价晶体之间的过渡晶体
D . 利用超分子的自组装特征,可以分离C60和C70
科学家利用四种原子序数依次增大的短周期主族元素W、X、Y、Z“组合”成一种超分子,该超分子具有高效的催化性能,其分子结构示意图如下(注:实线代表共价键,其他重复单元的W、X未标注)。已知X、Y位于同一周期,基态Z原子中只有两种形状的电子云,最外层只有一种自旋方向的电子,下列说法正确的是( )
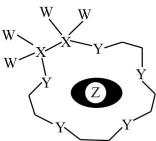
A . 氢化物的沸点: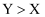 B . Y与Z形成的化合物中只含离子键
C . 由X、Y、Z形成的单质分别为共价晶体、分子晶体和金属晶体
D . 该超分子反映了超分子“分子识别”的特性
B . Y与Z形成的化合物中只含离子键
C . 由X、Y、Z形成的单质分别为共价晶体、分子晶体和金属晶体
D . 该超分子反映了超分子“分子识别”的特性
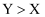 B . Y与Z形成的化合物中只含离子键
C . 由X、Y、Z形成的单质分别为共价晶体、分子晶体和金属晶体
D . 该超分子反映了超分子“分子识别”的特性
B . Y与Z形成的化合物中只含离子键
C . 由X、Y、Z形成的单质分别为共价晶体、分子晶体和金属晶体
D . 该超分子反映了超分子“分子识别”的特性
最近更新
- 在翻译的过程中,碱基互补配对发生于哪两者之间 A.氨基酸与转运RNA
- 直流电路如图所示,在滑动变阻器的滑片P向右移动时,电源的() A.总功率一定减小 B.效率一定增大 C.内部损耗功率一定
- —What sports do you play after school, Jim? —_____.A. I play
- 制约环境承载力的主要因素是( )A.科技水平 B.人均物质消费量 C.资源总量 D.人均精神消费量
- 下列叙述中不正确的是() A.动物体内癌细胞一般能不断合成蛋白质和产生中心粒 B.生物的卵细胞虽然分化程度很高,但仍然具
- 下图中实线是沿x轴传播的一列简谐横波在t=0时刻的波形图,虚线是这列波在t=0.05s时刻的波形图。已知该波的波速是80
- 引领20世纪初期中国社会前进的旗帜,并推动了资产阶级民主革命发展的是( ) A.资产阶级维新思想 B.三民主义思想
- 下列各式成立的是( ) A.22=(﹣2)2 B.23=(﹣2)3 C.﹣23=4 D.(﹣
- (13分)设函数 (I)k为何值时,f(x)在R上是减函数; (II)试确定实数k的值,使的极小值为0.
- We tried tofind a table for seven, but they were all
- 据宁波市统计局公布的第六次人口普查数据,本市常住人口760.57万人,其中760.57万人用科学记数法表示为( )
- 下列事例中,属于利用声传递能量的是( )A.用声呐探测海底深度B.用超声波清洗眼镜C.医生用听诊器为病人检查身体D
- 已知两个圆锥,底面重合在一起,其中一个圆锥顶点到底面的距离为2cm,另一个圆锥顶点到底面的距离为3cm,则其直观图中这两
- AnEnglishman was showing a foreign visitor around London. “W
- 下列函数中,( ) 、
- 词汇运用 56. Put the vegetables into the fridge so that they can
- 不畏浮云遮望眼, 。(王安石《登飞来峰》)
- 阅读下面的小说,完成小题。 品质 (英)约翰·高尔斯华绥 格斯拉先生的店房朴素安静,橱窗里陈列的几双靴子太美观了,是
- 2008年5月12日的汶川大地震,牵动了亿万中国人的心。在震后的救灾工作中,科学的搜救方法非常重要。有一种被称为“气垫”
- 在水平放置的两块金属板AB上加上不同电压,可以使从炽热的灯丝释放的电子以不同速度沿直线穿过B板中心的小孔O进入宽度为L的



