分子晶体 知识点题库
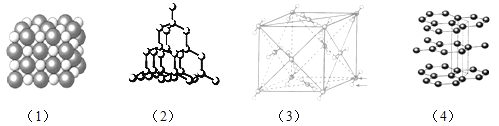
下列6种物质:A.P4(白磷),B.SiO2 , C.CaCl2 , D.Ca(OH)2 , E.NaF,F.CO2 , 固态下都为晶体,回答下列问题:(填字母编号)
(1)熔化时与破坏(1)晶体类型相同化学键的有 ;
(2)其中与(2)晶体类型相同的有 ,它们属于 晶体.
(3)与(3)晶体类型相同的有 ,熔化时需要破坏 作用力.
(4)分析对比(2)(4)晶体,硬度较大的是 .
(5)上述(1)﹣(3)三种晶体通常熔点由高到低的排列顺序为(填数字编号)
-
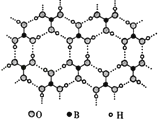
(1) 硼酸晶体属于 (填“离子晶体”、“分子晶 体”或“原子晶体”),B元素的电负性 O元素(填“>”或“<”).
-
(2) 硼酸晶体中,B的杂化轨道类型是
-
(3) 硼酸晶体中,微粒间的作用力类型有
-
(4) 硼酸是一元弱酸,其呈酸性的机理是:硼酸与水作用时,硼原子与水电离产生的OH﹣以配位键结合形成Y﹣离子,导致溶液中c(H+)>c(OH﹣).Y﹣的结构简式是 硼酸与水作用时,每生成一个Y﹣ , 断裂 个σ键.
-
(5) 三氟化硼水解生成硼酸和氟硼酸(H[BF4]),BF4﹣的空间结构与CH4相似.BF4﹣和BF3中硼氟键的键长如表所示.
BF4﹣
BF3
键长/pm
152
130
从表中数据可以看出,BF3中硼氟键的键长比BF4﹣的B﹣F键的键长短,原因可能是
-
(1) 水分子中氧原子在基态时核外电子排布式为
-
(2) H2O分子中氧原子采取的是 杂化.写出与H2O分子互为等电子体的微粒 .(写一个即可)
-
(3) 水分子容易得到一个H+形成水合氢离子(H3O+).对上述过程的下列描述不合理的是 .
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.水分子仍保留它的化学性质 D.微粒中的键角发生了改变
-
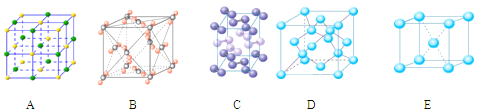
(4) 下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序).与冰的晶体
类型相同的是 (请用相应的编号填写)
-
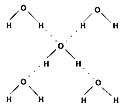
(5) 在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51kJ/mol,除氢键外,水分子间还存在范德华力(11kJ/mol),则冰晶体中氢键的“键能”是 kJ/mol;
-
(6) 将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子.请写出生成此配合离子的离子方程式:
-
(7) 已知下列元素的电负性数据:H:2.1,O:3.5,F:4.0.OF2与水的立体结构相似,但水分子的极性比OF2强得多,其原因有:①OF2中氧原子上有两对孤对电子,抵消了F一O键中共用电子对偏向F而产生的极性;②从电负性上看,
-
(8) 分析下表数据,请写出你的最具概括性的结论:
键型
键能
(kJ/mol)
键长
(pm)
分子
键角
物质
熔点(℃)
沸点(℃)
H﹣C
413
109
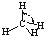
109.5°
甲烷
﹣183.7
﹣128.0
H﹣N
391
101
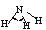
107°
氨
﹣77.7
﹣33.3
H﹣O
467
96
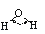
104.5°
水
0.0
100.0
① ;②
①晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性
②含有金属阳离子的晶体一定是离子晶体
③共价键可决定分子晶体的熔、沸点
④MgO的晶格能远比NaCl大,这是因为前者离子所带的电荷数多,离子半径小
⑤晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列
⑥晶体尽可能采取紧密堆积方式,以使其变得比较稳定
⑦干冰晶体中,一个CO2分子周围有12个CO2分子紧邻;CsCl和NaCl晶体中阴、阳离子的配位数都为6.
①原子晶体中只存在非极性共价键
②稀有气体形成的晶体属于原子晶体
③干冰晶体升华时,分子内共价键会发生断裂
④金属元素和非金属元素形成的化合物一定是离子化合物
⑤分子晶体的堆积均为分子密堆积
⑥离子晶体和金属晶体中均存在阳离子,但金属晶体中却不存在离子键
⑦金属晶体和离子晶体都能导电
⑧依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体
-
(1) C60分子形成的晶体中,在晶胞的顶点和面心均含有一个C60分子,则一个C60晶胞的质量为。
-
(2) 干冰和冰是两种常见的分子晶体,下列关于两种晶体的比较中正确的是(填字母代号)。
a.晶体的密度:干冰>冰
b.晶体的熔点:干冰>冰
c.晶体中的空间利用率:干冰>冰
d.晶体中分子间相互作用力类型相同
-
(3) 金刚石和石墨是碳元素形成的两种常见单质,下列关于这两种单质的叙述中正确的有。
a.金刚石中碳原子的杂化类型为sp3杂化,石墨中碳原子的杂化类型为sp2杂化
b.晶体中共价键的键长:金刚石中C—C<石墨中C—C
c.晶体的熔点:金刚石>石墨
d.晶体中共价键的键角:金刚石>石墨
e.金刚石晶体中只存在共价键,石墨晶体中则存在共价键、金属键和范德华力
f.金刚石和石墨的熔点都很高,所以金刚石和石墨都是原子晶体
-
(4) 金刚石晶胞结构如图所示,立方BN结构与金刚石相似,在BN晶体中,B原子周围最近的N原子所构成的立体图形为,一个晶胞中N原子数目为。
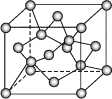
-
(5) C与孔雀石共热可以得到金属铜,铜原子的原子结构示意图为,金属铜采用面心立方最密堆积(在晶胞的顶点和面心均含有一个Cu原子),则Cu的晶体中Cu原子的配位数为。
晶体 | NaCl | MgO | SiCl4 | AlCl3 | 晶体硼 |
熔点/℃ | 801 | 2 800 | -70 | 180 | 2 500 |
①H2O汽化成水蒸气破坏分子间作用力、H2O分解为H2和O2 , 需要破坏共价键
②C4H10的两种同分异构体因为分子间作用力大小不同,因而沸点不同
③因为晶体硅的摩尔质量比金刚石的摩尔质量大,所以晶体硅的熔点比金刚石的高
④SiO2与CO2的分子结构类似,所以化学性质类似
⑤分子晶体中,共价键键能越大,该分子晶体的熔、沸点越高
-
(1) 根据要求回答下列问题:
①干冰与 CO2;②白磷与红磷;③3517Cl 与3717Cl;④液氯与氯水;⑤
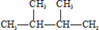 与
与 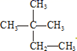 。 在上述各组物质中:
。 在上述各组物质中:互为同位素的是;
互为同素异形体的是;
互为同分异构体的是;
属于同种物质的是。(填序号,下同)
-
(2) 现有以下六种物质形成的晶体:a.NH4Cl;b.SiO2;c.Na2O2;d.干冰;e.C60;f.Ne 请用相应字母填空:
属于分子晶体的是; 属于共价化合物的是;属于离子化合物的是;熔化时只需要破坏共价键的是; 既含有离子键又含有非极性共价键的是; 不存在化学键的是。
①冰 ②二氧化硅 ③碘 ④铜 ⑤固态的氩
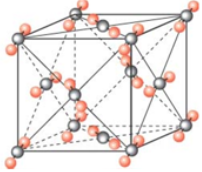
 分子
C . 每个
分子
C . 每个 分子周围有12个紧邻的
分子周围有12个紧邻的 分子
D . 干冰升华时需克服分子间作用力
分子
D . 干冰升华时需克服分子间作用力
- 自选一位历史名人,写一段赞誉性文字,要求内容符合人物特点,语言有文采,至少运用两种修辞手法。可以从下面提供的人物中选取,
- 根据拼音在田字格内写出相应的汉字。(4分) 微笑是人生一道亮丽的风景线,一种不会diāo xiè的花朵。无论生活多么匆忙
- 已知两个分式,,其中。则下面三个结论正确的是 ( ) A.A=B
- 如图所示,在△ABC中,∠B=40°,将△ABC绕点A逆时针旋转至在△ADE处,使点B落在BC的延长线上的D点处,则∠B
- 过双曲线()的右焦点作直线的垂线,垂足为,交双曲线的左支于点,若,则该双曲线的离心率为( ▲ ) (A)
- 若︱a-5︱+=0,则a-b的立方根是________
- 2010年5月13日,河南省高级人民法院宣布:给予因错案冤枉服刑10多年的赵作海国家赔偿金及生活困难补助费共计65万元,
- “全民大炼钢铁”“大办公共食堂,吃饭不要钱”。与这样的事情相关联的是( )A.第一个五年计划
- 中国的抗战对世界反法西斯战争胜利的贡献突出表现在
- 《应诏统筹全局折》与《五条誓文》 A.都是改革的施政纲领 B.都提出了比较具体的变化措施并得到了贯彻执行
- It was said _____ was all ______ he said. A. that that; that
- 27.Shanghai Expo has been building an Expo Village for the p
- 下图是洋务运动时期创办的最大的军事工业,创办者是( )A.李鸿章 B.左宗棠
- 观察下列不等式:,,,,,,由此猜想第个不等式为 .
- 某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一
- 函数y=(m+1)x|m|+1+4x﹣5是二次函数,则m=.
- 标签:系统默认该标签表示题目的开始。
- 200件产品中有3件次品,任意抽取5件,其中至少有2件次品的抽法有( ) A.种
- I had been told that she was really nice but she was ______
- 16.下图是中国人民抗日战争暨世界反法西斯战争胜利70周年纪念活动标识,请写出构图要素,并阐述其寓意。



