用晶格能的大小衡量离子晶体中离子键的强弱 知识点题库
-
(1) 科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
晶体
NaCl
KCl
CaO
晶格能/(kJ•mol﹣1)
786
715
3 401
四种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是
-
(2) 科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图1,其中配位键和氢键均采用虚线表示.
①写出基态Cu原子的核外电子排布式 ;
金属铜采用图2中 (填字母代号)堆积方式.
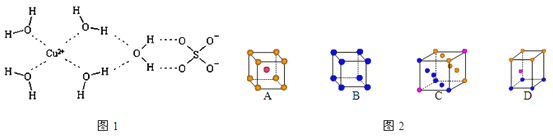
②水分子间存在氢键,请你列举两点事实说明氢键对水的性质的影响:
③SO42﹣的空间构型是
-
(3) 下列哪个系列的排列顺序正好是电负性减小的顺序?
A.K、Na、Li B.O、Cl、H C.As、P、H D.三者都是.
①共价键可决定分子晶体的熔、沸点【
②含有金属阳离子的晶体一定是离子晶体
③晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性
④MgO的晶格能远比NaCl大,这是因为前者离子所带的电荷数多,离子半径小
⑤晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列
⑥干冰晶体中,一个CO2分子周围有12个CO2分子紧邻;CsCl和NaCl晶体中阴、阳离子的配位数都为6
⑦晶体尽可能采取紧密堆积方式,以使其变得比较稳定.
-
(1) 黄铜矿的主要成分为二硫化亚铁铜(CuFeS2),基态Cu2+的外围电子排布图为 ,Fe2+含有 个未成对电子。
-
(2) Mn的第三电离能比Fe的第三电离能大的原因为 。
-
(3) 煤化工可得氨气、苯、甲苯等产品,氨的空间构型为 ,甲苯分子上甲基的碳原子的杂化方式为;氨硼烷化合物(NH3▪BH3)是一种新型化学氢化物储氢材料,氨硼烷的结构式为(配位键用“→”表示),与氨硼烷互为等电子体的有机小分子为写名称)。
-
(4) 碲化锌的晶胞结构如图1所示。
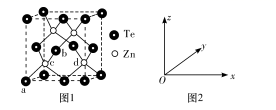
①碲化锌的化学式为。
②图2可表示晶胞内部各原子的相对位置,已知a、b、c的原子坐标参数分别为(0,0,0)、(
 ,0,
,0,  )、(
)、( 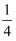 ,
, 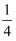 ,
, 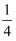 ),则d的原子坐标参数为
),则d的原子坐标参数为③若两个距离最近的Te原子间距离为apm,阿伏加德罗常数值为NA , 则晶体密度为g/cm3(用含有NA、a的代数式表示,不必化简)。
 、
、  、
、 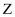 、
、 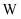 ,原子序数依次增大,X原子基态时
,原子序数依次增大,X原子基态时 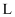 层中
层中 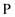 轨道电子数与s轨道电子数相同;
轨道电子数与s轨道电子数相同;  原子基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧化物可作涂料;
原子基态时2p原子轨道上有3个未成对的电子;Z有多种氧化物,其中一种红棕色氧化物可作涂料; 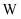 位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
位于第四周期,其原子最外层只有1个电子,且内层都处于全充满状态。回答下列问题:
-
(1) X位于周期表的第周期,第族。
-
(2) 元素的第一电离能:XY(填“>”或“<”,下同);原子半径:XY。
-
(3)
 的最高价氧化物对应水化物中酸根离子的空间构型是(用文字描述)。
的最高价氧化物对应水化物中酸根离子的空间构型是(用文字描述)。
-
(4)
 基态核外电子排布式为,用铁氰化钾溶液检验
基态核外电子排布式为,用铁氰化钾溶液检验 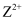 的离子方程式为。
的离子方程式为。
-
(5) 元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是,它可与浓盐酸发生非氧化还原反应,生成配合物
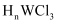 ,反应的化学方程式:。
,反应的化学方程式:。 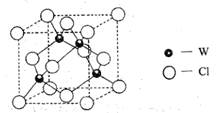
-
(1) ①为了纪念元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。Fe在元素周期表中的位置为。科学家在研究金属矿物质组分的过程中。发现了Cu-Ni-Fe等多种金属互化物。确定某种金属互化物是晶体还是非晶体的方法是。
②已知:r(Fe2+)为61 pm,r(Co2+)为65 pm。在隔绝空气条件下分别加热FeCO3和CoCO3 , 实验测得FeCO3的分解温度低于CoCO3 , 原因是。
③下表是Fe和Cu的部分电离能数据,请解释I2(Cu)大于I2(Fe)的主要原因是。
元素
Fe
Cu
第一电离能I1/kJ·mol-1
759
746
第一电离能I2/kJ·mol-1
1561
1958
-
(2) 原子序数依次增大的五种元素A、B、C、D、E分别处于第一至第四周期,A是前四周期中原子半径最小的元素,B原子核外电子有6种不同的运动状态,常温下C的单质是空气中含量最多的成分,D最高价氧化物对应水化物的酸性最强,E的基态原子的最外能层只有一个电子,其他能层均已充满电子。请回答下列问题:
①B2A2的电子式是,D所在主族的前四种元素分别与A形成的化合物,其共价键的极性由强到弱的顺序是(填化学式)。
②A和C形成的简单化合物遇到D单质出现白烟现象,写出有关反应的化学方程式为。
③向E的硫酸盐溶液中滴加过量氨水,观察到的现象是首先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液,请写出最后-步得到深蓝色透明溶液对应的离子方程式。
-
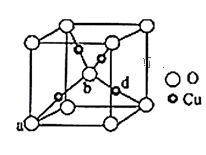
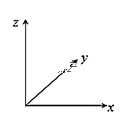
(3) 铜与氧元素可形成如图所示的晶胞结构,其中Cu均匀地分散在立方体内部,a、b的坐标参数依次为(0,0,0)、(
 ,
,  ,
,  ),则d的坐标参数为,已知该品体的密度为ρg/cm3 , NA是阿伏加德罗常数值,则晶胞参数(晶胞棱长)为cm(列出计算式即可)。
),则d的坐标参数为,已知该品体的密度为ρg/cm3 , NA是阿伏加德罗常数值,则晶胞参数(晶胞棱长)为cm(列出计算式即可)。
-
(1) 元素N 的价层电子排布式为3d2 4s2 ,其氯化物 NCl4 和LiBH4 反应可制得储氢材料N(BH4)3 。元素 N 在周期表中的位置为,该原子具有种不同运动状态的电子。 B 原子的轨道表示式为。
-
(2) 金属氢化物是具有良好发展前景的储氢材料。
① LiH 中,离子半径: Li+ (填“>”“=”或“<”) H- 。
②某储氢材料是短周期金属元素M 的氢化物。 M 的部分电离能(单位: kJ· mol-1 )如下表所示:
I1
I2
I3
I4
I5
738
1451
7733
10540
13630
M 的最高正价是价。
-
(3) AlF3 具有较高的熔点(1040℃),属于(填晶体类型)晶体;AlCl3 在 178℃时升华,写出 AlF3 、AlCl3晶体类型不同的原因(从原子结构与元素性质的角度作答)。
 )破坏臭氧层的反应过程示意图,下列说法错误的是( )
)破坏臭氧层的反应过程示意图,下列说法错误的是( )
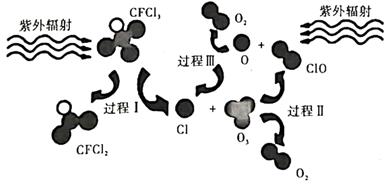
 )只有一种结构
B . 过程Ⅱ可表示为
)只有一种结构
B . 过程Ⅱ可表示为 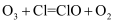 C . 过程Ⅲ中
C . 过程Ⅲ中 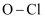 键断裂是放热过程,
键断裂是放热过程, 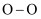 键形成是吸热过程
D . 上述过程说明氟利昂中氯原子是破坏
键形成是吸热过程
D . 上述过程说明氟利昂中氯原子是破坏  的催化剂
的催化剂
 B . 沸点:
B . 沸点: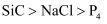 C . 晶格能:
C . 晶格能: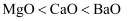 D . 共价键的健能:
D . 共价键的健能: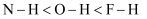
 (含
(含 、
、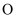 、
、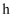 三种元素)的球棍模型如图所示,下列叙述正确的是( )
三种元素)的球棍模型如图所示,下列叙述正确的是( )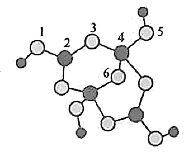
 的化学式为
的化学式为 B . 硼原子轨道的杂化类型有
B . 硼原子轨道的杂化类型有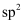 、
、 C . 配位键存在于
C . 配位键存在于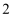 、
、 原子之间
D . 硼砂晶体中的化学键只有离子键和配位键
原子之间
D . 硼砂晶体中的化学键只有离子键和配位键
- 物体做匀加速直线运动,加速度为3 m/s2,下列说法正确的是() A.物体的末速度一定比初速度大3 m/s B.物体在每
- (09年天门中学月考理)(12分)已知平面上三个向量的模均为1,它们相互之间的夹角均为.(1) 求的值; (2)
- 解放后我国的农业生产发生了翻天覆地的变化,图12中A、B、C三地的农业也得到了快速的发展。阅读下图回答有关问题。1..从
- 下列各句中,加点的词语解释不完全正确的一项是 A.项为之强(通“僵”,僵硬) 惩(苦于)山北之塞 B
- 1912年元旦,《申报》刊登了这样一条庆贺标语:“中华民万岁”。《申报》把“国”字改写为“”主要是表达( ) A.“三
- 某种商品的标价为200元,按标价的八折出售,这时仍可盈利25%,则这种商品的进价是元.
- 洪仁玕《资政新编》中提出:“用人不当,足以坏法;设法不当,足以害人。只有二者兼顾,才能权归于一”。这种主张体现的法制思想
- 如图所示光学显微镜下观察到的根尖分生区的细胞,视野内看到最多的细胞是 ( )
- 下列各组词语中加点字的读音,与所给注音全都相同的一组是( ) A.假jiǎ 暑假 假嗓子
- 公元前452—450年间,罗马先后铸造十二块铜牌,详细列出民法、刑法、诉讼程序等许多方面的内容,公布于罗马广场,史称“十
- 下列句子中加点的词语解释有误的一项是 ( ) A、立春过后,大地渐渐从沉睡中苏
- 把ag Na2O和a1 g Na2O2分别加入等质量的水中(水足量),结果得到同浓度的溶液,则a和a1的关系正确的是(
- 下列函数解析式中,一定为二次函数的是() A.y=3x﹣1 B.y=ax2+bx+c C.s=2t2﹣2t
- 下列离子在指定溶液中能大量共存的是( )。 ①pH=11的溶液中:CO3 2-、Na+、AlO2-、NO3-;②无
- Millions of people visit Yosemite National Park every year t
- 读“我国大陆部分地壳厚度的等厚度线分布图”,回答下列说法中,正确的是() A.图中“40”等厚度线大约为我国季风区与非
- 世界区域经济集团化和经济全球化趋势迅速加强的根本原因是( ) A.两极格局的解体
- 圆上的动点到直线的最小距离为( ) A. B. C. D.
- 如图4所示的电路中,不计温度对灯丝电阻的影响,电源电压保持不变。当在a、b间接“6V 6W”的灯泡时,闭合开关,灯L恰
- 下列词语中没有错别字的一组是A.肇事 擀面杖 旁证博引 弃之如敝履B.诡秘 吊书袋 煞有介



