用晶格能的大小衡量离子晶体中离子键的强弱 知识点
用晶格能的大小衡量离子晶体中离子键的强弱 知识点题库
-
(1) 基态氮原子价层电子排布图为,其中电子能量最高的能级是。
-
(2) HOCH2CH2NH2所含非金属元素电负性由大到小顺序为,其中C和N的杂化方式均为HOCH2CH2NH2中∠HOC小于∠HNC,其原因是。
-
(3) HOCH2CH2NH2是一种常见的二齿配体,能和Co2+形成环状配离子。Co位于元素周期表中区,该环状配离子的配位原子为。
-
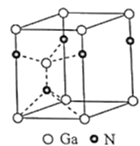
(4) 氮化镓为六方晶胞,其结构如图,其中Ga作六方最密堆积。Ga填充在N围成的(选填:八面体空隙、正四面体空隙、立方体空隙或三角形空隙);已知该晶胞底边边长为apm,高为cpm,阿伏加德罗常数的值为NA , 则该晶体的密度为g•cm-3(列出计算式即可)。
-
(1) 基态Zn原子的价电子排布式为,在周期表中位置为。
-
(2) 硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①组成[Zn(NH3)4]SO4的元素中,除H外其余元素的第一电离能由大到小排序为。
②在[Zn(NH3)4]SO4溶液中滴加NaOH溶液,未出现浑浊,其原因是。
③已知[Zn(NH3)4]2+的空间构型与SO42-相同,则在[Zn(NH3)4]2+中Zn2+的杂化类型为。
④以下作用力在[Zn(NH3)4]SO4晶体中存在的有。
A.离子键 B.极性共价键 C.非极性共价键
D.配位键 E.范德华力 F.金属键
-
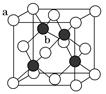
(3) ZnS晶胞结构如图(已知a为硫离子,b为锌离子)所示,ZnS晶体的熔点约为1 700 ℃。
①已知晶体密度为ρ g·cm-3 , NA为阿伏加德罗常数的值。则1个ZnS晶胞的体积为cm3。
②ZnO与ZnS结构相似,熔点为1 975 ℃,其熔点较高的原因是。
|
A组 |
B组 |
C组 |
D组 |
|
金刚石:3550 ℃ |
Li:181 ℃ |
HF:-83 ℃ |
NaCl:801 ℃ |
|
硅晶体:1410 ℃ |
Na:98 ℃ |
HCl:-115 ℃ |
KCl:776 ℃ |
|
硼晶体:2300 ℃ |
K:64 ℃ |
HBr:-89 ℃ |
RbCl:718 ℃ |
|
二氧化硅:1723 ℃ |
Rb:39 ℃ |
HI:-51 ℃ |
CsCl:645 ℃ |
据此回答下列问题:
-
(1) A组属于晶体。
-
(2) B组晶体共同的物理性质是(填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
-
(3) C组中HF熔点反常是由于。
-
(4) D组晶体可能具有的性质是(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
-
(5) D组晶体的熔点由高到低的顺序为NaCl>KCl>RbCl>CsCl,其原因为。
①含有离子的晶体一定是离子晶体 ②分子晶体若采取密堆积方式,其配位数是12 ③含有共价键的晶体一定是原子晶体 ④分子晶体的熔点一定比金属晶体的低 ⑤MgO远比NaCl的晶格能大 ⑥共价键的强弱决定分子晶体熔、沸点的高低
-
(1) 基态
 原子的核外电子排布式为。
原子的核外电子排布式为。
-
(2) 一种香豆素衍生物(
 )可作为测定
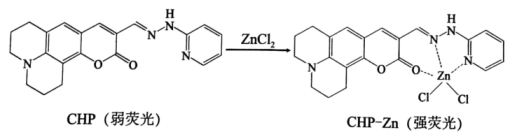
)可作为测定 的荧光探针,其原理如下图所示。已知
的荧光探针,其原理如下图所示。已知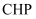 中
中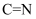 结构的异构化和旋转会导致荧光减弱。
结构的异构化和旋转会导致荧光减弱。
①
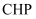 所含元素(C、H、O、N)电负性从大到小的顺序为;
所含元素(C、H、O、N)电负性从大到小的顺序为;②
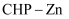 中N原子的杂化类型为;
中N原子的杂化类型为;③加入
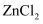 后,体系荧光增强的原因是。
后,体系荧光增强的原因是。 -
(3)
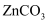 可用于配制炉甘石洗剂,具有收敛和保护皮肤的作用。
可用于配制炉甘石洗剂,具有收敛和保护皮肤的作用。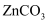 中阴离子
中阴离子 的空间构型为,与
的空间构型为,与 互为等电子体的分子有(任写一种)。
互为等电子体的分子有(任写一种)。
-
(4)
 水溶液可作为工业零件淬火的冷却介质。已知
水溶液可作为工业零件淬火的冷却介质。已知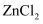 的熔点为275℃,而
的熔点为275℃,而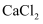 的熔点为782℃,两者熔点相差较大,其原因是。
的熔点为782℃,两者熔点相差较大,其原因是。
-
(5)
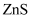 是一种性能优异的荧光材料,在自然界中有立方
是一种性能优异的荧光材料,在自然界中有立方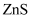 和六方
和六方 两种晶型,其晶胞结构如下图所示:
两种晶型,其晶胞结构如下图所示:
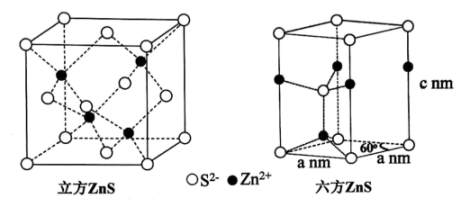
①立方
 中,
中, 填充在
填充在 形成的空隙中;
形成的空隙中;②六方
 的晶体密度为
的晶体密度为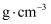 (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 、
、 、
、 、
、 、
、 为短周期主族元素,
为短周期主族元素,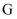 、
、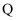 为第四周期元素,它们的原子序数依次增大。
为第四周期元素,它们的原子序数依次增大。 元素原子核外电子数和电子层数相同;
元素原子核外电子数和电子层数相同; 的价电子层中未成对电子有
的价电子层中未成对电子有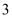 个;
个;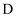 元素为最活泼非金属元素;
元素为最活泼非金属元素;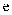 的最高价氧化物对应的水化物既能与酸又能与强碱反应;
的最高价氧化物对应的水化物既能与酸又能与强碱反应;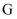 元素正三价离子的
元素正三价离子的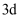 轨道上填充了
轨道上填充了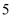 个电子;
个电子;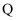 元素基态原子的
元素基态原子的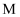 层全充满,
层全充满,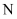 层只有
层只有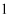 个电子。
个电子。
-
(1)
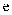 元素在元素周期表中的位置是,
元素在元素周期表中的位置是,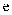 元素基态原子中填有电子的能量最高的能级符号是。
元素基态原子中填有电子的能量最高的能级符号是。
-
(2)
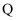 元素基态原子的价电子排布式为,
元素基态原子的价电子排布式为, 为离子化合物,写出其阴离子的电子式(用化学符号表示)。
为离子化合物,写出其阴离子的电子式(用化学符号表示)。
-
(3)
 元素的第一电高能
元素的第一电高能 元素的第一电离能(填“
元素的第一电离能(填“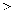 ”“
”“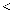 ”或“
”或“ ”),
”), 、
、 、
、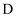 三种元素的电负性由大到小的顺序是(用化学符号表示),
三种元素的电负性由大到小的顺序是(用化学符号表示), 、
、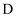 、
、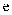 元素形成的简单离子中半径最大的是(用化学符号表示)。
元素形成的简单离子中半径最大的是(用化学符号表示)。
-
(4)
 元素正三价离子比正二价离子稳定的原因是。
元素正三价离子比正二价离子稳定的原因是。
-
(5) 向盛有
 的硫酸盐溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解并得到深蓝色的透明液体;若向试管中加入一定量乙醇,析出深蓝色晶体。蓝色沉淀溶解时发生反应的离子方程式是,深蓝色晶体中不存在的化学键有(填字母序号)。
的硫酸盐溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解并得到深蓝色的透明液体;若向试管中加入一定量乙醇,析出深蓝色晶体。蓝色沉淀溶解时发生反应的离子方程式是,深蓝色晶体中不存在的化学键有(填字母序号)。a.离子键 b.极性健 c.非极性键 d.配位键
-
(1) 已知Sn和Si同族,基态Sn原子价层电子的空间运动状态有种,基态氧原子的价层电子排布式不能表示为2s22p
 2p
2p , 因为这违背了(填选项)。
, 因为这违背了(填选项)。A.泡利原理 B.洪特规则 C.能量最低原理
-
(2) [B(OH)4]-中硼原子的杂化轨道类型为,[B(OH)4]-的空间构型为。[Sn(OH)6] 2-中,Sn与O之间的化学键不可能是(填选项)。
A.π键 B.σ键 C.配位键 D.极性键
-
(3) 碳酸钡、碳酸镁分解温度较低的是,分解得到的金属氧化物中,熔点较低的是BaO,其原因是。
-
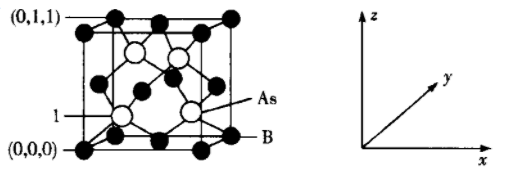
(4) 超高热导率半导体材料-砷化硼(BAs)的晶胞结构如图所示,则1号砷原子的坐标为。已知阿伏加德罗常数的值为NA , 若晶胞中As原子到B原子最近距离为a pm,则该晶体的密度为g·cm-3(列出含a、NA的计算式即可)。
-
(1) 硫原子的价电子轨道表示式为。
-
(2) 硫化钠的熔点 (填“大于”“小于”或“等于”)硫化钾的熔点,原因是。
-
(3) 硫酸根和硫代硫酸根的结构如下图所示:
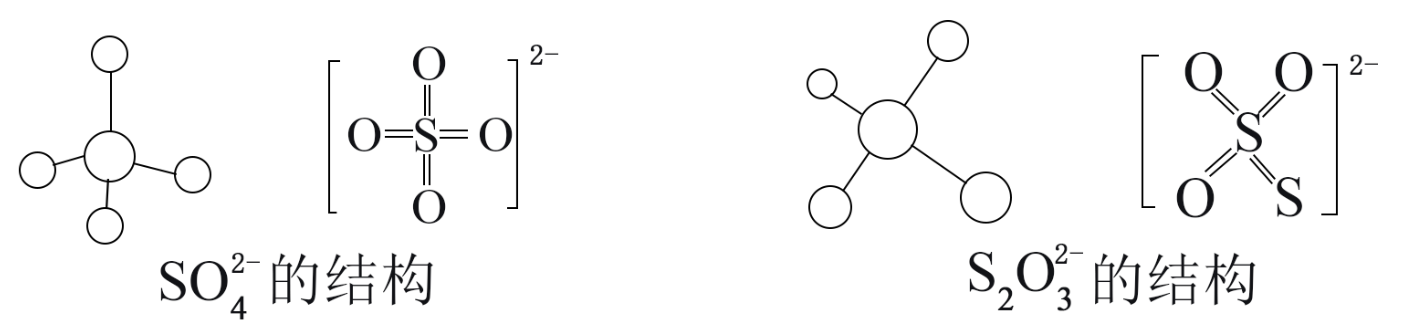
S2O
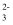 的空间构型为, 中心硫原子的杂化轨道类型为。
的空间构型为, 中心硫原子的杂化轨道类型为。 -
(4) 硫原子和氧原子可形成多种链式硫酸根离子,连二硫酸根离子、连三硫酸根离子如下图所示:
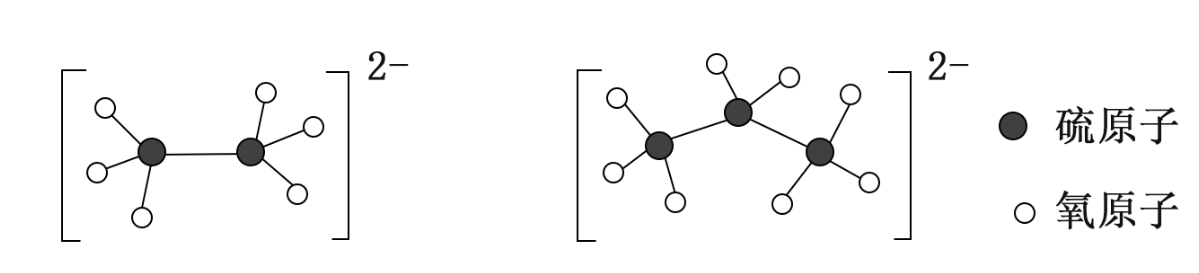
这类硫原子数可变的多硫氧合阴离子的化学式可用通式表示为(用n代表硫原子数)。
-
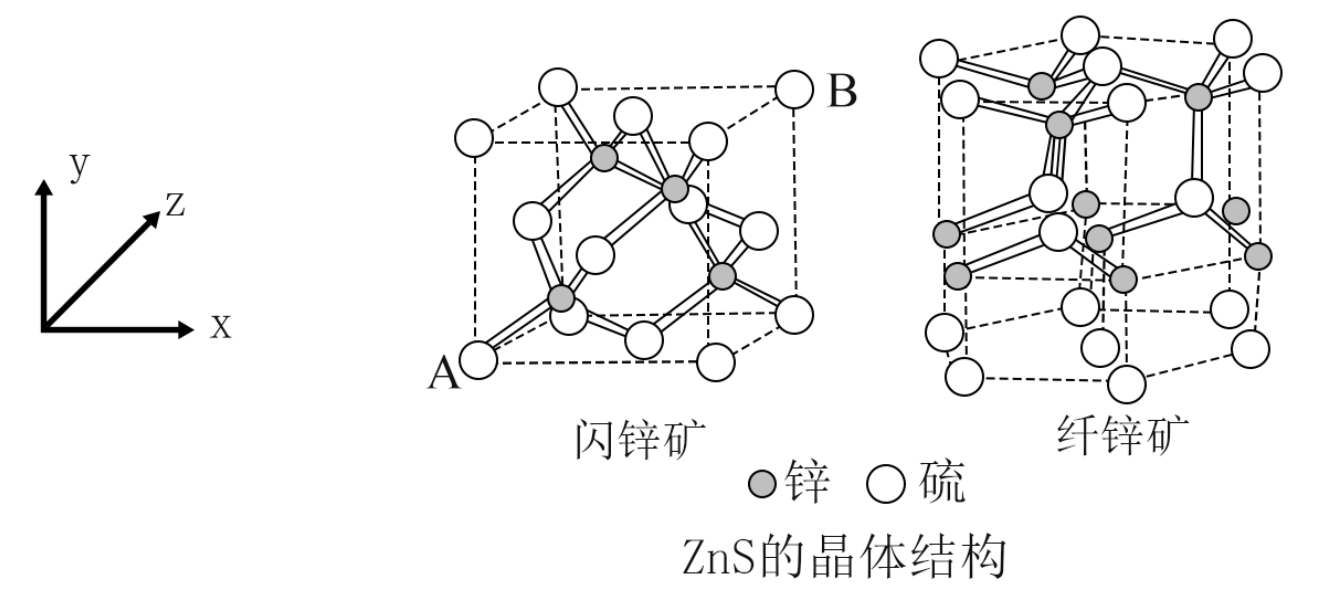
(5) 天然硫化锌以闪锌矿和纤锌矿存在,ZnS的晶体结构如下图所示,闪锌矿中Zn2+的配位数为,已知原子A、B的分数坐标为(0, 0, 0)和(1, 1, 1),原子C的分数坐标为。 纤锌矿晶体堆积模型为。
-
(6) 闪锌矿中,设晶胞边长为a, Zn2+和 S2-的离子半径分别为
 和
和 , 则Zn2+和S2-离子的空间占有率为% (列出计算表达式)。
, 则Zn2+和S2-离子的空间占有率为% (列出计算表达式)。
 的沸点低于
的沸点低于 , 是由于C=O键的键能比C=S键的大
D . 因金属性:K>Na>Mg,所以熔点:
, 是由于C=O键的键能比C=S键的大
D . 因金属性:K>Na>Mg,所以熔点: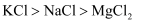
- 下列对物理现象、概念认识正确的是:A.由于地球大气阻力作用,从高空下落的大雨滴落地速度大于小雨滴落地速度B.以匀加速运动
- 在1200℃时,天然气脱硫工艺中会发生下列反应 ①H2S(g)+ 3/2 O2(g)=SO2(g)+H2O(g) △
- We must face the fact __________ our time is limited and we
- 在配制一定物质的量浓度的盐酸溶液时,下列错误操作可使所配制溶液浓度偏高的是( ) A.用量筒量取浓盐酸俯视读数
- 如图所示,表示的是化合反应和氧化反应之间的关系,按示例填空按示例填空: A部分:是化合反应,不是氧化反应,例:二氧化碳+
- 下列铁路不属于山西省煤炭外运干线的是 A.胶济线 B.大秦线 C.神黄线 D.太焦线
- 唐代中枢机构中书省、尚书省和门下省的精细分工体现了( )A.施政观念上的民主追求
- 有n=10匝的矩形线圈,每匝都是长50cm,宽20cm,线圈总电阻10Ω,在B=2T的匀强磁场中以角速度ω=50rad/
- 关于我国国情的叙述正确的是( )①中国是世界国力最强的国家 ②中国地大物博,人均资源丰富③中国耕地面积居世界第
- 如图所示电路为“用电流表、电压表测电阻”的实验电路,请填写空格处的内容。 ① 实验目的:伏安法测电阻,要求(13),求电
- 下列是“探究某种加酶洗衣粉使用的最适温度”的实验设计,最合理的是( )A.加酶洗衣粉在 30 ℃的水中洗涤效果没有 4
- 4.下列各句中,没有语病的一项是。 A.这是一个可以将相亲、求职等社会传统话题搬上电视荧幕并对其进行娱乐化改造的时代,在
- 某同学用量筒取液体,量筒平稳且面向刻度线,初次平视液面,读数为19mL,倾倒出部分液体后,俯视液面,读数是11mL,则实
- 法国哲学家爱尔维修有句名言:“人是环境的产物”,某论坛上,主持人让听众写下与自己关系最密切的6个朋友,并指出他们月收入的
- 在基因指导某种蛋白质的合成过程中,细胞中的哪些“措施”有利于保证或提高“翻译”的速率( ) ①一条mRNA上结
- 下列可以使光合作用加强的一项是( )A.增加氧气的浓度 B.增加
- 完成句子 1.西蒙认为丝绸制造的白衬衣将与任何其他颜色很相配。 Simon thinks white shirts __
- 根据句子意思和所给首字母或中文提示,在标有题号的横线上写出一个英语单词的完整、正确形式,使句意通顺。 81. The d
- 干轰轰烈烈的大事才可以体现人生价值。
- 2006年10月19日,2000余名海内外彭氏宗亲汇聚江苏徐州彭祖园,举行“祭拜彭祖大典”仪式。中华民族这种尊祖敬宗的习



