水的电离 知识点题库
常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A . 使酚酞变红色的溶液中:Na+、Al3+、SO42﹣、Cl﹣
B .  =1×10﹣13mol•L﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C . 与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
D . 水电离的c(H+)=1×10﹣13mol•L﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
=1×10﹣13mol•L﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C . 与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
D . 水电离的c(H+)=1×10﹣13mol•L﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
 =1×10﹣13mol•L﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C . 与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
D . 水电离的c(H+)=1×10﹣13mol•L﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
=1×10﹣13mol•L﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C . 与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
D . 水电离的c(H+)=1×10﹣13mol•L﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
25℃时,水中存在平衡:H2O⇌H++OH﹣△H>0,下列叙述正确的是( )
A . 加入稀氨水,平衡逆向移动,c(OH﹣)降低,Kw不变
B . 加入少量固体CuSO4 , c (H+)增大,Kw不变
C . 加入少量固体CH3COONa,平衡逆向移动,c (H+)降低,Kw不变
D . 加热到90℃,Kw增大,溶液仍呈中性,pH不变
25℃时,水的电离达到平衡: H2O  H++ OH-ΔH > 0 ,下列叙述正确的是( )
H++ OH-ΔH > 0 ,下列叙述正确的是( )
 H++ OH-ΔH > 0 ,下列叙述正确的是( )
H++ OH-ΔH > 0 ,下列叙述正确的是( )
A . 将水加热,Kw增大,pH不变
B . 向水中加入少量盐酸,c(H+)增大,Kw不变
C . 向水中加入NaOH固体,平衡逆向移动,c(OH-) 降低
D . 向水中加入AlCl3固体,平衡逆向移动,c(OH-) 增大
下列各种离子一定能大量共存的是( )
A . 强碱性溶液中:Na+、K+、AlO2-、CO32-
B . 含有大量Fe3+的溶液中:NH4+、SCN-、Cl-、K+
C . pH=7的溶液中:NH4+、Al3+、SO42-、CO32-
D . c(OH-)=1×10-13mol/L的溶液中:K+、Fe2+、Cl-、NO3-
25℃时,部分物质的电离平衡常数如表所示:
|
化学式 |
CH3COOH |
NH3·H2O |
H2CO3 |
H2SO3 |
|
电离平衡常数 |
1.7×10-5 |
1.7×10-5 |
K1=4.3×10-7 K2=5.6×10-11 |
K1=1.3×10-2 K2=6.3×10-8 |
请回答下列问题:
-
(1) H2CO3的第二级电离平衡常数的表达式K2=。
-
(2) 相同温度下,等pH的CH3COONa溶液、Na2CO3溶液和Na2SO3溶液,三种溶液的物质的量浓度c(CH3COONa)、c(Na2CO3)、c(Na2SO3)由大到小排序为。
-
(3) 用足量Na2CO3溶液吸收工业尾气中少量SO2气体,发生反应的离子方程式为。
-
(4) 25℃时,向0.1 mol•L-1的氨水中缓缓少量CO2气体的过程中(忽略溶液体积的变化),下列表达式的数值变小的是______。A .
 B .
B .  C .
C .  D .
D . 
-
(5) 能证明醋酸是弱酸的实验事实是(填写序号)。
① 相同条件下,浓度均为0.1 mol•L-1的盐酸和醋酸,醋酸的导电能力更弱
② 25℃时,一定浓度的CH3COOH、CH3COONa混合溶液的pH等于7
③ CH3COOH溶液能与NaHCO3反应生成CO2
④ 0.1mol•L-1 CH3COOH溶液可使紫色石蕊试液变红
-
(6) 向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如图所示。
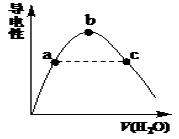
① a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是。
② a、c两点对应的溶液分别吸收氨气,若两溶液最终pH均为7(25℃时),则a点溶液中的c(CH3COO-)c点溶液中的c(NH4+)。(填“<”、“>”或“=”)
在常温下,某无色溶液中,由水电离出的c(H+)=1×10-14mol·L-1 , 则该溶液中,一定能大量共存的离子是( )
A . K+、Na+、MnO4-、SO42-
B . Na+、CO32-、AlO2-、Cl-
C . K+、Na+、Cl-、Br-
D . K+、Cl-、Ba2+、HCO3-
常温下将pH=8的NaOH溶液稀释1000倍,稀释后溶液中c(Na+)与c(OH-)之比接近( )
A . 1:1
B . 1:102
C . 102:1
D . 1:103
下列溶液中的离子关系正确的是( )
A . 相同温度下,0.2 mol·L-1的醋酸溶液与0.1mol·L-1的醋酸溶液中c(H+)之比大于2 : 1
B . pH=3的醋酸和pH=3的FeCl3溶液中,由水电离出的c(H+)相等
C . 0.1 mol﹒L-1NaHSO4溶液中:c(H+)=c(SO 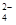 ) +c(OH-)
D . pH=4、浓度均为0.1 mol·L-1的CH3COOH、CH3COONa 混合溶液中:c(CH3COO-)-c(CH3COOH)=10-4-10-10mol/L
) +c(OH-)
D . pH=4、浓度均为0.1 mol·L-1的CH3COOH、CH3COONa 混合溶液中:c(CH3COO-)-c(CH3COOH)=10-4-10-10mol/L
25℃时,某稀溶液中由水电离产生的c(H+)为1×10-10 , 下列说法错误的是( )
A . 该溶液一定不是中性
B . NH4+、Na+、Cl-、HCO3- 在该溶液不能共存
C . 该溶液的pH一定是10
D . 该溶液中水的电离受到抑制
下列操作会使H2O的电离平衡向正方向移动,且所得溶液呈酸性的是( )
A . 向水中加入少量的CH3COONa
B . 向水中加入少量的NaHSO4
C . 加热水至100 ℃,pH=6
D . 向水中加少量的CuSO4
将1 mL 0.1 mol·L-1的H2SO4溶液加入纯水中制成200 mL溶液,该溶液中由水自身电离产生的c(H+)最接近于( )
A . 1×10-3 mol·L-1
B . 1×10-11 mol·L-1
C . 1×10-7 mol·L-1
D . 1×10-13 mol·L-1
弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb),请回答下面问题:
|
酸或碱 |
电离平衡常数(Ka或Kb) |
|
CH3COOH |
1.8×10-5 |
|
HNO2 |
4.6×10-4 |
|
HCN |
5×10-10 |
|
HClO |
3×10-8 |
|
NH3•H2O |
1.8×10-5 |
-
(1) CH3COONH4的水溶液呈(选填“酸性”、“中性”或“碱性”)。理由是。溶液中各离子浓度大小关系是。
温度t℃时,某NaOH稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,请回答下列问题:
-
(2) 该温度下水的离子积常数Kw=。
-
(3) 该NaOH溶液中由水电离出的c(OH-)是mol/L。
-
(4) 给该NaOH溶液加热(水不挥发),pH=。(填变大、变小或不变)
下列说法错误的是( )
A . 常温下,pH=5的氯化铵溶液中由水电离出的c(H+)=1×10-5mol·L-1
B . 将Na2CO3溶液从常温加热至80℃,溶液的碱性增强
C . 常温下,0.1mol·L-1CH3COOH溶液pH=3,说明CH3COOH是弱电解质
D . 常温下,pH为11的氨水溶液中加入氯化铵固体,溶液pH增大
下列说法错误的是( )
A . 0.1mol/L 的硫酸铵溶液中:C(NH  )>C(SO
)>C(SO  )
B . 25℃ 时 pH=2 的醋酸溶液中水电离出的 C(H+)=10-12mol/L
C . 配制 FeCl3溶液,应加少量盐酸
D . 将 Al2(SO4)3溶液蒸干,灼烧得 Al2O3
)
B . 25℃ 时 pH=2 的醋酸溶液中水电离出的 C(H+)=10-12mol/L
C . 配制 FeCl3溶液,应加少量盐酸
D . 将 Al2(SO4)3溶液蒸干,灼烧得 Al2O3
 )>C(SO
)>C(SO  )
B . 25℃ 时 pH=2 的醋酸溶液中水电离出的 C(H+)=10-12mol/L
C . 配制 FeCl3溶液,应加少量盐酸
D . 将 Al2(SO4)3溶液蒸干,灼烧得 Al2O3
)
B . 25℃ 时 pH=2 的醋酸溶液中水电离出的 C(H+)=10-12mol/L
C . 配制 FeCl3溶液,应加少量盐酸
D . 将 Al2(SO4)3溶液蒸干,灼烧得 Al2O3
下列有关水的叙述正确的是( )
A . 水是一种非电解质
B . 纯水中c(H+)随着温度的升高而降低
C . 由液态水结成冰的过程是一个熵增的过程
D . 25℃时浓度相同的氢氧化钠溶液与醋酸钠溶液,水的电离度前者小于后者
常温下,向20 mL 0.1 mol·L-1 NaHC2O4溶液中缓慢滴加等浓度的NaOH溶液,混合溶液的温度与滴加NaOH溶液体积的关系如图所示,下列说法错误的是( )
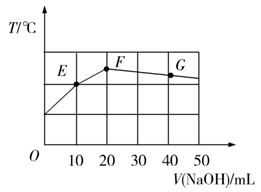
A . E点存在:2c(Na+)=3c(H2C2O4)+3c(HC2O  )+3c(C2O
)+3c(C2O  )
B . F点存在:c(OH-)>c(H+)+c(HC2O
)
B . F点存在:c(OH-)>c(H+)+c(HC2O  )+c(H2C2O4)
C . G点存在:c(Na+)>c(C2O
)+c(H2C2O4)
C . G点存在:c(Na+)>c(C2O  )>c(OH-)>c(HC2O
)>c(OH-)>c(HC2O  )
D . 滴加过程中,水的电离程度先变大,后变小
)
D . 滴加过程中,水的电离程度先变大,后变小
 )+3c(C2O
)+3c(C2O  )
B . F点存在:c(OH-)>c(H+)+c(HC2O
)
B . F点存在:c(OH-)>c(H+)+c(HC2O  )+c(H2C2O4)
C . G点存在:c(Na+)>c(C2O
)+c(H2C2O4)
C . G点存在:c(Na+)>c(C2O  )>c(OH-)>c(HC2O
)>c(OH-)>c(HC2O  )
D . 滴加过程中,水的电离程度先变大,后变小
)
D . 滴加过程中,水的电离程度先变大,后变小
下列有关电解质溶液的说法正确的是( )
A . 向0.1mol•L-1氨水中滴加等浓度的CH3COOH溶液至过量,水的电离程度一直增大
B . 常温下,pH=2的某酸HA与pH=12的某碱BOH等体积混合溶液呈酸性,则HA为强酸,BOH为弱碱
C . 0.2mol•L-1CH3COOH溶液中的c(H+)是0.1mol•L-1CH3COOH溶液中的c(H+)的2倍
D . 浓度均为0.1mol•L-1的NH4HSO4溶液与NaOH溶液等体积混合后:c(SO  )=c(Na+)>c(NH
)=c(Na+)>c(NH  )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
 )=c(Na+)>c(NH
)=c(Na+)>c(NH  )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
常温下,向20mL浓度均为0.1mol·L-1的HA与NaA的混合溶液中,分别滴加浓度均为0.1mol·L-1的HCl、NaOH两种溶液,混合溶液的pH变化情况如图所示。已知Ka(HA)=10-4.76。下列说法正确的是( )
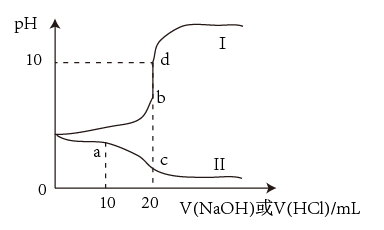
A . 滴加HCl溶液的曲线为Ⅰ
B . 水的电离程度:b>a>c
C . d点时,lg  =5.24
D . b点溶液中存在:c(Na+)=2[c(A-)+c(HA)]
=5.24
D . b点溶液中存在:c(Na+)=2[c(A-)+c(HA)]
 =5.24
D . b点溶液中存在:c(Na+)=2[c(A-)+c(HA)]
=5.24
D . b点溶液中存在:c(Na+)=2[c(A-)+c(HA)]
25℃时,向25mL0.1mol·L-1邻苯二甲酸(H2A)溶液中加入KOH固体,混合溶液的pH随-lgc(HA-)以及-lgc(A2-)的关系如图所示(忽略溶液体积变化和邻苯二甲酸的挥发)。下列有关叙述错误的是( )
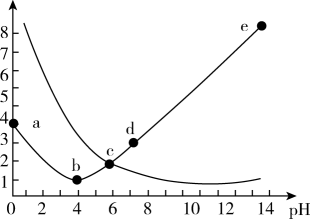
A . 邻苯二甲酸的Ka1约为1.0×10-3
B . b点有关微粒浓度大小关系为(HA-)>c(A2-)>c(H2A)
C . 从b点到e点,水电离产生的c(H+)先增大后减小
D . c点c(K+)>3c(A2-)
甘氨酸盐酸盐 的水溶液呈酸性,溶液中存在以下平衡:
的水溶液呈酸性,溶液中存在以下平衡:
 的水溶液呈酸性,溶液中存在以下平衡:
的水溶液呈酸性,溶液中存在以下平衡: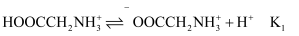
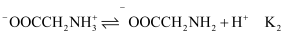
常温时,向10mL一定浓度的 的水溶液中滴入同浓度的NaOH溶液。混合溶液pH随加入NaOH溶液体积的变化如图所示。下列说法正确的是( )
的水溶液中滴入同浓度的NaOH溶液。混合溶液pH随加入NaOH溶液体积的变化如图所示。下列说法正确的是( )
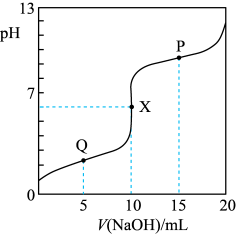
A . 水的电离程度:Q>X
B . X→P过程中: 逐渐增大
C . P点的溶液中:
逐渐增大
C . P点的溶液中: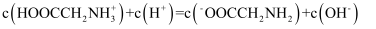 D . 当
D . 当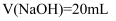 时,混合溶液中的溶质主要为
时,混合溶液中的溶质主要为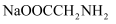 和NaCl
和NaCl
 逐渐增大
C . P点的溶液中:
逐渐增大
C . P点的溶液中: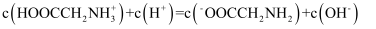 D . 当
D . 当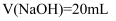 时,混合溶液中的溶质主要为
时,混合溶液中的溶质主要为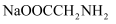 和NaCl
和NaCl
最近更新
- “奏国歌,升国旗”是进行爱国主义教育的内容,你知道《中华人民共和国国歌》源自下列哪一部电影的插曲吗? A.《渔光曲》B.
- 普通小麦中有高秆抗病(TTRR)和矮秆易感病(ttrr)两个品种,控制两对性状的基因分别位于两对同源染色体上。实验小组利
- 已知函数f(x)=2x-.(1)若f(x)=2,求x的值;(2)若2tf(2t)+mf(t)≥0对于t∈[1,2]恒成立
- We _____ very glad if what he told us ______ true. A. shall
- 设函数f(x)=2x,若f(x0)>1,则x0的取值范围是A.(0,2)∪(3,+∞)
- 如图所示,MN是纸面内的一条直线,其所在空间充满与纸面平行的匀强电场或与纸面垂直的匀强磁场(场区都足够大),现有一个重力
- 现有浓盐酸、浓硫酸、氢氧化钠、石灰水四种溶液,将其长期露放在空气中,溶液质量因发生物理变化而减少的是,而增大的是.因发生
- 已知∠α是它的余角的2倍,则∠α=________.
- 假定债券市场上一年期债券的利率有2.25%、2.50%和3.0%三档。一般来讲,与此三档利率水平相对应的债券的发行主体分
- This kind of cloth _______ well. I think it is worthy ______
- 下列关于生物膜结构和功能的叙述正确的是 A、肌细胞的细胞膜上有协助葡萄糖跨膜运输的载体 B、细胞膜上的受体是细胞间信息交
- 阅读《人的头发为什么会变白》一文 ①我们的毛发为什么会有颜色呢?毛发的色调主要由两种黑色素构成:真黑色素和类黑色素。真黑
- 2009年3月26日,某市委学习实践科学发展观活动领导小组办公室与该市晚报联合推出“市民QQ议政”活动,为改市的科学发展
- 下列溶液蒸干后,能得到溶质固体的是( ) A.AlCl3 B.KHCO3 C.Fe2(SO4)3
- Every morning,manygirls in the African country of Zimbabwe r
- 下图中甲国铁矿、森林、渔业资源丰富,历史上航海业发达。目前拥有50多家具有国际领先水平的造船厂,对外贸易发达,读图回答下
- 在舞台上喷洒干冰(固态二氧化碳)可以产生白雾,形成所需的效果。这种雾气是: A.二氧化碳气体迅速液化而形成的小液滴
- 在炼铁、制玻璃、制水泥三种工业生产中,都需要的原料是:A.纯碱 B.石灰石 C.石英
- 如图,,,,.求证.
- The books in the largest library of the city could _____ all



