等效平衡 知识点题库
现有反应:CO(g)+H2O(g)  CO2(g)+H2(g) ΔH=-43kJ/mol,在850℃时,K=1,今在某密闭容器中充入1.0molCO、3.0molH2O、1.0molCO2、xmolH2 , 下列说法不正确的是( )
CO2(g)+H2(g) ΔH=-43kJ/mol,在850℃时,K=1,今在某密闭容器中充入1.0molCO、3.0molH2O、1.0molCO2、xmolH2 , 下列说法不正确的是( )
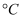 , 该反应的平衡常数K<1
B . 850
, 该反应的平衡常数K<1
B . 850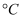 达到平衡时,通入CO,CO转化率将增大
C . 850
达到平衡时,通入CO,CO转化率将增大
C . 850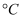 时,若x=5.0,则起始时平衡向逆反应方向移动
D . 850
时,若x=5.0,则起始时平衡向逆反应方向移动
D . 850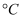 时,若要使上述反应开始时向正反应方向进行,则
时,若要使上述反应开始时向正反应方向进行,则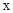 应满足
应满足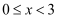
(1)恒温恒容条件下,若HBr的物质的量为n,则上述配比在平衡时HBr的物质的量仍为n的是 (填序号);若HBr体积分数为a%,则上述配比在平衡时仍为a%的是(填序号)。
(2)恒温恒压条件下,若HBr的物质的量为n,则上述配比在平衡时HBr的物质的量仍为n是(填序号);若HBr体积分数为a%,则上述配比在平衡时仍为a%的是 (填序号)。
容器 | 温度/℃ | 物质的起始浓度/mol•L﹣1 | 物质的平衡浓度/mol•L﹣1 | ||
c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
Ⅱ | 400 | 0.40 | 0.20 | 0 | |
Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
3A(g)+B(g)⇌2C(g)+D(g)
-
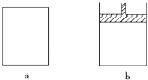
(1) 达平衡时,a中A的浓度为M mol・L﹣1 , C的浓度为N mol・L﹣1 , b中A的浓度为m mol・L﹣1 , C的浓度为n mol・L﹣1 , 则Mm;Nn; (填“>”或“<”或“=”或“无法比较”)
-
(2) 保持温度不变,按下列配比分别充入 a、b 两容器,达平衡后a中C的浓度为N mol・L﹣1的是,b中C的浓度为n mol・L﹣1的是
A.6molA+2molB B.3molA+2molC C.2molC+1molB+1mol D
D.2molC+1molD E.1.5molA+0.5molB+1molC+0.5molD
-
(3) 若将2molC和2molD充入a中,保持温度不变,平衡时A的浓度为Wmol・L﹣1 , C的浓度为Ymol・L﹣1 , 则W和M,Y和N之间的关系为WM、YN. (填>、<、=、无法比较)
-
(4) 保持温度不变,若将4molC和2molD充入a中,平衡时A的浓度为R mol・L﹣1 , 则关系式正确的是A . R=2M B . R<M C . M<R<2M D . R>2M
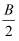 D . m<3
D . m<3
 2NH3(g),若开始时只充入2 mol NH3 (g),达平衡时,混合气体的平均摩尔质量等于10. 625g/moL;若开始时只充入3mol H2和1 mol N2的混合气体,达平衡时H2的转化率为( )
2NH3(g),若开始时只充入2 mol NH3 (g),达平衡时,混合气体的平均摩尔质量等于10. 625g/moL;若开始时只充入3mol H2和1 mol N2的混合气体,达平衡时H2的转化率为( )
 2NH3(g) ΔH= -92.4kJ/mol,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
2NH3(g) ΔH= -92.4kJ/mol,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下: 容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 |
NH3的浓度(mol/L) | c1 | c2 | c3 |
反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
体系压强 | P1 | P2 | P3 |
反应物转化率 | α1 | α2 | α3 |
下列说法正确的是( )
时间/s 浓度/mol·L-1 | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4) | 0.100 | c1 | 0.050 | c3 | a | b |
c(NO2) | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试填空:
-
(1) 该反应的化学方程式为;达到平衡时四氧化二氮的转化率为% ;表中 c2c3ab(选填“ > ”、“ < ”、“ = ”)。
-
(2) 20s时四氧化二氮的浓度 c1=mol·L-1 , 在0s~20s内四氧化二氮的平均反应速率为mol·(L·s)-1;
-
(3) 若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是mol·L-1。
 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( ) 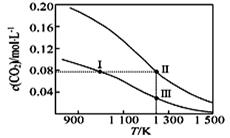
 2CO(g)的 ΔS>0、ΔH<0
B . 体系的总压强p总:p总(状态Ⅱ)<2p总(状态Ⅰ)
C . 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D . 逆反应速率v逆:v逆(状态Ⅰ)>v逆(状态Ⅲ)
2CO(g)的 ΔS>0、ΔH<0
B . 体系的总压强p总:p总(状态Ⅱ)<2p总(状态Ⅰ)
C . 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D . 逆反应速率v逆:v逆(状态Ⅰ)>v逆(状态Ⅲ)
 2SO3(g) ΔH<0,达到平衡时,下列说法不正确的是( )
2SO3(g) ΔH<0,达到平衡时,下列说法不正确的是( ) | 容器 编号 | 容器类型 | 起始物质的量 / mol | 平衡时SO3的物质的量 / mol | ||
| SO2 | O2 | SO3 | |||
| I | 恒温恒容 | 2 | 1 | 0 | 1.8 |
| II | 恒温恒压 | 2 | 1 | 0 | a |
| III | 绝热恒容 | 0 | 0 | 2 | b |
 2HI(g);ΔH= -14.9kJ·mol-1。某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008mol·L-1。下列判断正确的( )
2HI(g);ΔH= -14.9kJ·mol-1。某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008mol·L-1。下列判断正确的( ) | 起始浓度 | c(H2)/(mol·L-1) | c(I2)/(mol·L-1) | c(HI)(mol·L-1) |
| 甲 | 0.01 | 0.01 | 0 |
| 乙 | 0.02 | 0.02 | 0 |
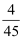 B . 图中c点所示条件下,v(正)>v(逆)
C . 向a点平衡体系中充入一定量的NO2 , 达到平衡时,NO2的转化率比原平衡大
D . 容器内的压强:Pa:Pb>6:7
B . 图中c点所示条件下,v(正)>v(逆)
C . 向a点平衡体系中充入一定量的NO2 , 达到平衡时,NO2的转化率比原平衡大
D . 容器内的压强:Pa:Pb>6:7
 2SO3(g);△H=-akJ·mo1-1 在相同条件下要想得到2akJ热量,加入各物质的物质的量可能是( )
2SO3(g);△H=-akJ·mo1-1 在相同条件下要想得到2akJ热量,加入各物质的物质的量可能是( )
 2E(g),若开始时只充入2mol E(g),达平衡时,E的转化率为40%;若开始时充入2mol M和1mol N的混合气体,达平衡时混合气体的压强比起始时减少了( )
2E(g),若开始时只充入2mol E(g),达平衡时,E的转化率为40%;若开始时充入2mol M和1mol N的混合气体,达平衡时混合气体的压强比起始时减少了( )
 ,反应过程中测定的部分数据见下表(表中t1<t2),下列说法错误的是( )
,反应过程中测定的部分数据见下表(表中t1<t2),下列说法错误的是( ) | 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
 mol/(L·min)
B . 保持其他条件不变,若起始时向容器中充入0.60 molCO和1.20 mol H2O (g),则到达平衡时n(CO2)=0.40 mol
C . 保持其他条件不变,若平衡后向容器中再充入0.40 mol CO和0.40 mol CO2 , 则平衡将向正反应方向移动
D . 温度升至800℃,上述反应的平衡常数为0.64,则该反应的正反应为放热反应
mol/(L·min)
B . 保持其他条件不变,若起始时向容器中充入0.60 molCO和1.20 mol H2O (g),则到达平衡时n(CO2)=0.40 mol
C . 保持其他条件不变,若平衡后向容器中再充入0.40 mol CO和0.40 mol CO2 , 则平衡将向正反应方向移动
D . 温度升至800℃,上述反应的平衡常数为0.64,则该反应的正反应为放热反应
 B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1阶段的 c(B)变化未画出]。
B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1阶段的 c(B)变化未画出]。 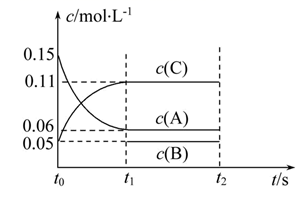
-
(1) 若 t1=15 s,用 A 的浓度变化表示 t0~t1阶段的平均反应速率为mol·L-1·s-1 , t1时A的转化率为。
-
(2) 由图可知t0时,加入B的物质的量为mol,若在t1时,将容器体积变为1 L,则此时c(A)=mol/L
-
(3) 若在相同体积的容器中,加入0.14 mol B和0.3 mol C,在相同的条件下发生反应,达平衡后A的物质的量浓度为mol/L。
-
(4) 若在同条件,同体积容器中加入a mol A、0.08 mol B和0.18 mol C,平衡后A的物质的量浓度与(3)相同,则a=
- 在大熊猫和大肠杆菌体内,最基本的化学元素和含量最多的化学元素分别是: A.C和O B.C和H
- 王谠在《唐语林》中写到“开元初,上留心理道,革去弊讹,不六七年,天下大理。河清海晏,物殷俗阜”。“留心理道”的皇帝是:
- 为虚数单位,则复数( )
- 依次填入下面各句横线处的词语,最恰当的一项是 ①森林的光合作用能够 大气中的氧气和二氧化碳的平衡,森林的蒸腾
- 【地理—环境保护】阅读图文材料,回答问题。 材料一 山东某地煤矿示意图材料二 据不完全统计,我国建筑物下压煤超过48
- 下图甲、乙分别是两类高等生物细胞的亚显微结构模式图。请据图回答: (1)请写出标号①结构的组成元素是
- 下列计算错误的是() A.(﹣2x)3=﹣2x3 B.﹣a2•a=﹣a3 C.(﹣x)9+(﹣x)9=
- 月球轨道呈椭圆形,近地点平均距离为363300千米,远地点平均距离为405500千米 , 用科学记数法表示 : 近地点平
- 已知苯和一卤代烷在催化剂的作用下可生成 在催化剂的作用下,由苯和下列各组物质合成乙苯(
- 如图在△ABC中,AB=AC=9,∠BAD=120°,AD是△ABC的中线,AE是∠BAD的角平分线,DF∥AB交AE的
- 2010年4月14日青海玉树发生7.1级地震,灾区饮用水安全备受关注。 (1)除去水中难溶性固体杂质的操作时
- . 第三节:书面表达(满分30分) 观察下面的一幅漫画,用英语写一篇100—120左右题为“Birds with Wea
- 某核素A ZX的氯化物XCl2 1.11 g配成溶液后,需用1mol·L-1的硝酸银溶液20 ml才能把氯离子完全沉淀下
- 用NA表示阿伏加德罗常数的值,下列说法正确的是() A.1mol N2所含有的原子数为NA B.标准状况下,22.4 L
- Aturning point of the continuously high housing price
- 如图,甲转盘被分成3个面积相等的扇形,乙转盘被分成4个面积相等的扇形,每一个扇形都标有相应的数字.同时转动两个转盘,当转
- 第二节:完形填空 (共15小题;每小题2分,满分30分) 阅读下面短文,掌握其大意,然后从41~55各题所给的四个
- 某动物的精子细胞中有染色体16条,则在该动物的初级精母细胞中存在染色体数、四分体数、染色单体数、DNA分子数分别是 A.
- 下列各组关联词填写在句中正确的一项是( ) ①我所说的是否与《礼记》《老子》原意相合,不必深求;____我确信“敬业
- 1.在下面一段话空缺处依次填入词语,最恰当的一组是( ) 书是整个人类的记忆。没有书,也许历史还在混沌未开的蒙昧中



