合成氨条件的选择 知识点
合成氨条件的选择 知识点题库
 2NH3 , 是工业上制造氮肥的重要反应.下列关于该反应的说法正确的是( )
2NH3 , 是工业上制造氮肥的重要反应.下列关于该反应的说法正确的是( )(1)向合成塔中按1:4的物质的量之比充入N2、H2进行氨的合成,图A为T℃时平衡混合物中氨气的体积分数与压强(P)的关系图.
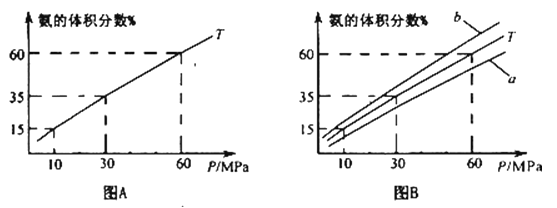
①写出工业上合成氨的化学方程式
②图A中氨气的体积分数为15.00%时,H2的转化率=
③图B中T=500℃,温度为450℃对应的曲线是 (选填字母“a“或“b”),选择的理由是
④由图象知,增大压强可提高原料的利用率,从生产实际考虑增大压强需解决的问题是 (写出一条即可).
(2)合成氨所需的氢气可由甲烷与水反应制得,反应的热化学方程式为:
CH4(g)+H2O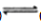 CO(g)+3H2(g);△H=+QkJ/mol(Q>0)
CO(g)+3H2(g);△H=+QkJ/mol(Q>0)
(3)一定温度下,在2L容器中发生上述反应,各物质的物质的量变化如下表
|
时间/min |
CH4(mol) |
H20( mol) |
CO (mol) |
H2 (mol) |
|
0 |
0.40 |
1.00 |
0 |
0 |
|
5 |
X1 |
X2 |
X3 |
0.60 |
|
7 |
Y1 |
Y2 |
0.20 |
Y3 |
|
10 |
0.21 |
0.81 |
0.19 |
0.62 |
①分析表中数据,判断5〜7min之间反应是否处于平衡状态 (填“是”或“否”),
前5min平均反应速率v(CH4)=
②反应在7~10min之间,CO的物质的量减少的原因可能是 (填字母).
a·减少CH4 b·降低温度c·增大压强d·充入H2
③若保持温度不变,向1L容器中起始充入0.15mol CH4.0.45mol H2O. mol CO、 mol H2 , 达到平衡时CH4的体积百分含量与第一次投料相同.
-
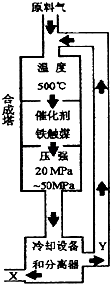
(1) X的化学式为;X的状态为态.
-
(2) 据图分析,下列说法正确的是(填写编号).
a.在此温度下,有利于平衡正向移动,可提高氨的产量
b.铁触媒的使用有利于平衡正向移动
c.工业生产受动力、材料、设备等条件的限制,选择此压强
d.为提高原料的转化率,采用循环操作
-
(3) 常温下氨气极易溶于水,其水溶液可以导电.
①氨水中水的离子积常数的数值是;
②将相同体积、相同物质的量浓度的氨水和盐酸混合后,溶液中离子浓度由大到小依次为.
 2NH3 , 回答下列问题:
2NH3 , 回答下列问题:
-
(1) 反应过程中拆开的化学键是;
-
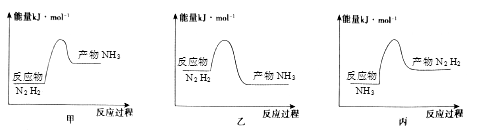
(2) 反应放热,从价键角度分析,反应放热的原因是,下列图像正确的是。
-
(3) 在体积是2L的密闭容器中开始加入1molN2 , 3molH2 , 反应过程浓度中,物质的浓度与时间的关系如图所示。
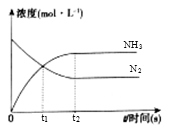
①t1时生成NH3的物质的量是;用H2表示的化学反应速率υ(H2)=。
②下列各项能表明反应达到化学平衡状态的是。
A.容器中气体的密度保持不变
B.容器中气体的压强不变
C.氨气的含量不变
D.拆开3molH-H键同时形成6molN-H键
-
(4) 下列措施中能提高合成氨反应化学反应速率的是。
A.使用高效催化剂
B.恒温恒容再充入氢气
C.降低反应温度
D.扩大容器体积
-
(1) 为了提高农作物的产量,德国化学家哈伯、波施等科学家成功地开发了将氮气转化为氨气的生产工艺,请用化学方程式表示工业合成氨的反应原理;为什么选择20~50Mpa的高压?说明理由。
-
(2) 氨气通入水中可制得氨水,氨水能使无色的酚酞变红,请用电离方程式表示其原因:。
-
(1) 制硫酸的三种原料是、、,三个生产过程是①,写出反应方程式,②,写出反应方程式,③,写出反应方程式,三废指的是、、。
-
(2) 合成氨的反应原理工业合成氨的反应条件为浓度使用过量的、温度℃、高压MPa、。
 2NH3(g),该反应一定条件下自发。下列有关说法正确的是( )
2NH3(g),该反应一定条件下自发。下列有关说法正确的是( )
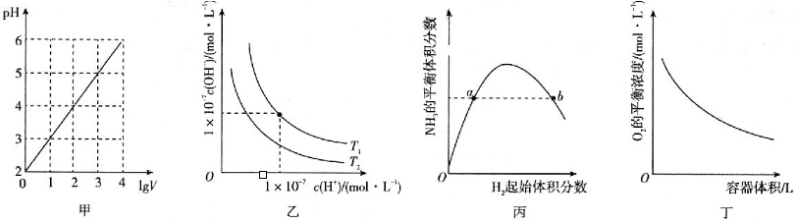
 溶液加水稀释至V L,pH随lg V的变化
B . 图乙表示不同温度下水溶液中H+和OH-浓度的变化的曲线,图中温度
溶液加水稀释至V L,pH随lg V的变化
B . 图乙表示不同温度下水溶液中H+和OH-浓度的变化的曲线,图中温度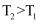 C . 图丙表示一定条件下的合成氨反应中,NH3平衡体积分数随H2始体积分数(N2起始量恒定)的变化,图中a点N2转化率小于b点
D . 图丁表示同一温度下,在不同容积的容器中进行反应
C . 图丙表示一定条件下的合成氨反应中,NH3平衡体积分数随H2始体积分数(N2起始量恒定)的变化,图中a点N2转化率小于b点
D . 图丁表示同一温度下,在不同容积的容器中进行反应
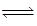
 , O2的平衡浓度与容器容积的关系
, O2的平衡浓度与容器容积的关系
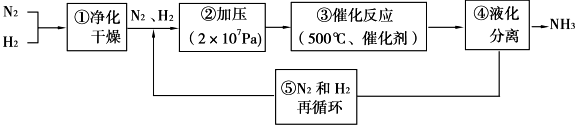
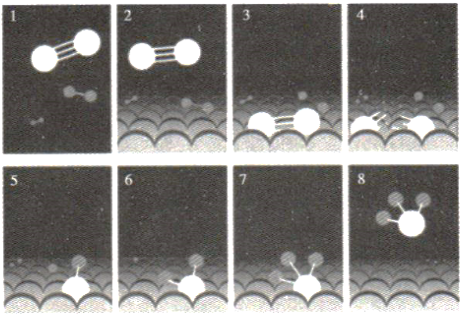
 键
C . NH3分子中的N—H键不是同时形成的
D . Fe催化剂可以有效提高反应物的平衡转化率
键
C . NH3分子中的N—H键不是同时形成的
D . Fe催化剂可以有效提高反应物的平衡转化率
 2NH3(g)ΔH= -92.4 kJ·mol-1的说法正确的是( )
2NH3(g)ΔH= -92.4 kJ·mol-1的说法正确的是( )
 的值可增大N2的转化率
D . 可以使用酶作该反应的催化剂
的值可增大N2的转化率
D . 可以使用酶作该反应的催化剂
 2NH3(g) △H<0,则下列说法错误的是( )
2NH3(g) △H<0,则下列说法错误的是( )
- 仿照下面诗歌首节三、四行的句式,在后两节的横线上写出合适的句子。 让我怎样感谢你 当我走向你的时候 我原想亲吻一朵雪花
- 如图所示,倾角为θ的光滑斜面ABC放在水平面上,劲度系数分别为k1、k2的两个轻弹簧沿斜面悬挂着,两弹簧之间有一质量为m
- Of the seven days in a week, Saturday is said to be the most
- 在“2A+3B===2C+4D”的反应中,已知8 g物质A完全反应生成11 g物质C和9 g物质D。若A的相对分子质量为
- 世界上各种气候类型中,在亚洲没有分布的是() A. 温带季风气候B. 温带海洋性气候 C. 地中海气候D. 热带雨林气候
- △ABC中,∠C=90°,AC=8,BC=6,则cosA的值是( ▲ )A.B.C.D.
- 北京奥运火炬实现了成功登上珠峰的预定目标,如图所示是火炬手攀登珠峰的线路图,请根据此图判断,下列说法正确的是() A.由
- 清朝康熙年间,烧制出大量如下图造型和装饰图案的瓷器,而且在瓷器的纹饰中绘有家族、公司、团体、城市等图案标志。下列相关表述
- 某同学希望通过比较电路中不同位置的电流表的读数来研究串联电路的电流规律.所接电路图如图所示,闭合开关后,两电流表指针偏转
- 长为L的平行金属板水平放置,两极板带等量的异种电荷,板间形成匀强电场,一个带电为+q、质量为m的带电粒子,以初速v0紧贴
- (1991第一届初中应用物理知识竞赛题)有一卷无木轴的铜导线,需要确定它的长度,但是不能把导线全部拉开;更不能把导线截断
- 人类在探索自然和科学考察的活动中,经常要面临无氧环境,在你熟悉的物质中,可以选用作为供氧剂的是 A. NaOH
- 下图表示相连线的酸、碱、盐之间可以发生复分解反应,下表提供的四组物质符合下图要求的是() 物质 组别 酸 碱 盐1 盐2
- 图1是A和B两种物质的溶解度曲线,结合图形回答下列问题:(1)70°C时B物质的溶解度为. (2)图中P点的含义是. (
- 读下面所示的一组海峡轮廓图5,回答:图5 (1)E代表 (半岛),F代表 (洲)。 (2
- (7分)下图表示A~D及NaOH等物质间的相互转化关系,其中A为淡黄色固体,B为短周期元素中金属性最强的单质。(1)写出
- Last year the number of students whograduated with a drivin
- 可逆反应aA(g)+bB(g)cC(g)+dD(g)符合图.则下列叙述正确的是()A.a+b<c+d;正反应吸热B.a+
- 已知为纯虚数,且为虚数单位),则( ) A.1 B. C. D.
- 如图所示,同一绝缘水平面内,一个小金属环a和一个大金属环b的圆心在同一点。a中通有顺时针方向的恒定电流I, b环中不通电



