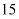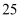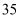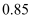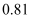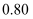化学平衡常数 知识点题库
实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | ||
n(X) | n(Y) | n(M) | n(N) | ||
① | 800 | 0.10 | 0.40 | 0.080 | 0.080 |
② | 800 | 0.20 | 0.80 | a | a |
③ | 900 | 0.10 | 0.15 | 0.06 | 0.06 |
下列说法不正确的是:( )
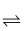 Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为
Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为 
 2NO(g)+O2(g)相关数据如下表所示。下列说法错误的是( )
2NO(g)+O2(g)相关数据如下表所示。下列说法错误的是( )容器 编号 | 物质的起始浓度 (mol·L-1) | 物质的平衡浓度 (mol·L-1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
 >1
D . 达到平衡时,容器Ⅰ与容器Ⅲ中的总压强之比为16∶17
>1
D . 达到平衡时,容器Ⅰ与容器Ⅲ中的总压强之比为16∶17
-
(1) Cl2和水蒸气通过灼热的炭层生成HCl和CO2 , 当有1 mol Cl2参与反应时释放145 kJ热量。写出该反应的热化学方程式。
-
(2) 已知CH3OH(l)的燃烧热为238.6 kJ·mol-1 , CH3OH(l)+1/2O2(g) =CO2(g)+2H2O(g) ΔH=-a kJ·mol-1 , 则a238.6(选填“>”、“<”或“=”)。
-
(3) 已知:As(s)+3/2H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+1/2O2(g)=H2O(l) ΔH2
2As(s)+5/2O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =。
-
(4) 已知在一定温度下:
C(s)+ CO2(g)
 2CO(g) 平衡常数K1
2CO(g) 平衡常数K1C(s)+ H2O(g)
 CO(g)+ H2(g) 平衡常数 K2
CO(g)+ H2(g) 平衡常数 K2CO(g)+ H2O(g)
 H2(g)+ CO2(g)平衡常数K3
H2(g)+ CO2(g)平衡常数K3则K1、K2、K3之间的关系是。
|
温 度(℃) |
360 |
440 |
520 |
|
K值 |
0.036 |
0.010 |
0.0038 |
-
(1) ①由上表数据可知该反应为 (填放热,吸热,无法确定)反应。
②下列措施能用勒夏特列原理解释是(填序号)。
a.增大压强有利于合成氨 b.使用合适的催化剂有利于快速生成氨
c.生产中需要升高温度至500℃左右 d.需要使用过量的N2 , 提高H2转化率
-
(2) 0.2mol氨气溶于水后再与含有0.2mol硫酸的溶液反应放热QkJ,请你用热化学方程式表示其反应式。
-
(3) 常温时,将amol氨气溶于水后,再通入bmol氯化氢,溶液体积为1L,且c(NH4+)=c(Cl﹣),则一水合氨的电离平衡常数Kb=(用ab表示)。
-
(4) 原料气H2可通过反应 CH4(g)+H2O (g)
 CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的
CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的  恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如图所示: 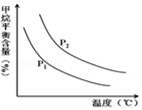
①图中,两条曲线表示压强的关系是:P1P2(填“>”、“=”或“<”)。
②其它条件一定,升高温度,氢气的产率会(填“增大”,“减小”减小,“不变”不变)。
-
(5) 原料气H2还可通过反应CO(g)+H2O(g)
 CO2(g)+H2(g)获取。
CO2(g)+H2(g)获取。 ①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol•L﹣1 , 该温度下反应的平衡常数K值为。
②保持温度仍为T℃,容积体积为5L,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是(填序号)。
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6
-
(1) 亚硝酰氯(Cl—N=O)气体是有机合成的重要试剂,它可由Cl2和NO在通常条件下反应制得,该反应的热化学方程式为。
相关化学键的键能如下表所示:
化学键
Cl—Cl
N
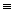 O(NO气体)
O(NO气体) Cl—N
N=O
键能/(kJ·mol-1)
243
630
200
607
-
(2) 燃煤发电厂常利用反应2CaCO3(s)+2SO2(g)+O2(g)
 2CaSO4(s)+2CO2(g) ΔH=-681.8kJ·mol-1 , 对煤进行脱硫处理来减少SO2的排放。对于该反应,在T℃时,借助传感器测得反应在不同时间点上各物质的浓度如下:
2CaSO4(s)+2CO2(g) ΔH=-681.8kJ·mol-1 , 对煤进行脱硫处理来减少SO2的排放。对于该反应,在T℃时,借助传感器测得反应在不同时间点上各物质的浓度如下: 时间/min
浓度/mol·L-1
0
10
20
30
40
50
O2
1.00
0.79
0.60
0.60
0.64
0.64
CO2
0
0.42
0.80
0.80
0.88
0.88
①0~10min内,平均反应速率v(CO2)=mol·L-1·min-1;当升高温度,该反应的平衡常数K(填“增大”、“减小”或“不变”)。
②30min后,只改变某一条件,反应重新达到平衡。根据上表中的数据判断,改变的条件可能是 (填字母)。
A.加入一定量的粉状碳酸钙
B.适当缩小容器的体积
C.通入一定量的O2
D.加入合适的催化剂
-
(3) NOx的排放主要来自于汽车尾气,有人利用反应C(s)+2NO(g)
 N2(g)+CO2(g) ΔH=-34.0kJ·mol-1 , 用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) ΔH=-34.0kJ·mol-1 , 用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示: 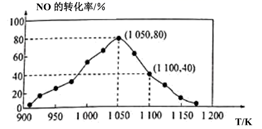
由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa时,该反应的化学平衡常数Kp=[已知:气体分压(P分)=气体总压(Pa)×体积分数]
-
(4) 为避免汽车尾气中的有害气体对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH=-746.8kJ·mol-1 , 生成无毒的N2和CO2实验测得,v正=k正c2(NO)·c2(CO),v逆=k逆c(N2) c2(CO2)(k正、k逆为速率常数,只与温度有关)。①达到平衡后,仅降低温度,k正减小的倍数 (填“>”、“<”或“=”)k逆减小的倍数。②若在1L的密闭容器中充入1molCO和1molNO,在一定温度下达到平衡时,CO的转化率为20%,则
N2(g)+2CO2(g) ΔH=-746.8kJ·mol-1 , 生成无毒的N2和CO2实验测得,v正=k正c2(NO)·c2(CO),v逆=k逆c(N2) c2(CO2)(k正、k逆为速率常数,只与温度有关)。①达到平衡后,仅降低温度,k正减小的倍数 (填“>”、“<”或“=”)k逆减小的倍数。②若在1L的密闭容器中充入1molCO和1molNO,在一定温度下达到平衡时,CO的转化率为20%,则  =(计算结果用分数表示)
=(计算结果用分数表示)
-
(1) 科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。
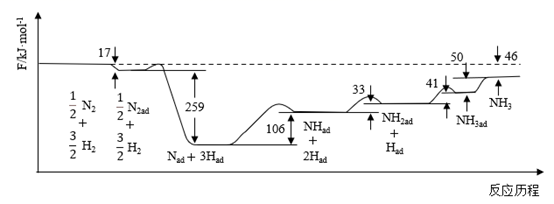
由图可知合成氨反应
 N2(g)+
N2(g)+ 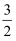 H2(g)⇌NH3(g)的△H=kJ·mol-1 , 该反应历程中最大能垒对应的化学方程式为:。
H2(g)⇌NH3(g)的△H=kJ·mol-1 , 该反应历程中最大能垒对应的化学方程式为:。 -
(2) 2NO(g)+O2(g) ⇌ 2NO2(g) (ΔH Ea)的反应历程由两步基元反应组成:
Ⅰ.2NO(g)⇌N2O2(g) (快) ΔH1<0 Ea1 v1正=k1正c2(NO) v1逆=k1逆c(N2O2)
Ⅱ.N2O2(g)+O2(g)⇌2NO2(g) (慢) ΔH2<0 Ea2 v2正=k2正c(N2O2)c(O2) v2逆=k2逆c2(NO2)
①一定温度下,反应2NO(g)+O2(g)⇌2NO2(g)达到平衡状态,写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=。
②下列关于反应2NO(g)+O2(g) ⇌ 2NO2(g)的说法正确的是。
A.2Ea=Ea1+Ea2
B.增大压强,反应速率常数增大
C.温度升高,正逆反应速率都增大
D.总反应快慢由第二步决定
③在其他条件不变的情况下,2NO(g)+O2(g) ⇌ 2NO2(g)反应速率随着温度升高而减小,请解释原因。
④画出2NO+O2 ⇌ 2NO2的反应过程—能量示意图。

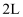 恒容容器中充入
恒容容器中充入 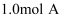 和
和 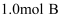 ,发生反应
,发生反应 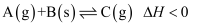 ,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题:
,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题: | | | | | | |
| | | | | | |
-
(1) 前
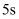 的平均反应速率
的平均反应速率 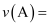 ,达平衡时
,达平衡时  的平衡体积分数为。
的平衡体积分数为。
-
(2) 由表中数据计算该温度下该反应的平衡常数为,随着反应温度升高,该反应的平衡常数(选填“增大”、“减小”或“不变”)。
-
(3) 保持温度不变,起始时向容器中充入
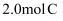 ,达平衡时,
,达平衡时,  的转化率为。
的转化率为。
 )关系如图所示。下列叙述正确的是( )
)关系如图所示。下列叙述正确的是( ) 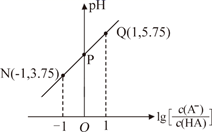
-
(1) SO2的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的SO2。已知吸收过程中相关反应的热化学方程式如下:① SO2(g) + NH3•H2O(aq) =NH4HSO3(aq) △H1 = a kJ•mol-1;② NH3•H2O(aq) + NH4HSO3(aq) =(NH4)2SO3(aq) + H2O(l)△H2 = b kJ•mol-1;③ 2(NH4)2SO3(aq) + O2(g) =2(NH4)2SO4(aq) △H3= c kJ•mol-1 , 则反应 2SO2(g) + 4NH3•H2O(aq) + O2(g) =2(NH4)2SO4(aq) + 2H2O(l) △H = 。
-
(2) NOx的排放主要来自于汽车尾气,有人利用反应C (s) + 2NO(g)
 N2(g) + CO2(g) △H=-34.0 kJ•mol-1 , 用活性炭对NO进行吸附。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率 α(NO)随温度的变化如图所示:
N2(g) + CO2(g) △H=-34.0 kJ•mol-1 , 用活性炭对NO进行吸附。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率 α(NO)随温度的变化如图所示: 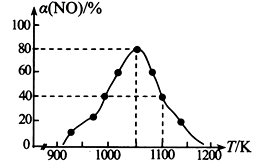
①由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是; 在1100K 时,CO2的体积分数为。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa 时,该反应的化学平衡常数Kp=(已知:气体分压=气体总压×体积分数)。
-
(3) 在高效催化剂的作用下用CH4还原NO2 , 也可消除氮氧化物的污染。在相同条件下,选用A,B,C三种不同催化剂进行反应,生成 N2的物质的量与时间变化关系如图所示,其中活化能最小的是(填字母标号)。
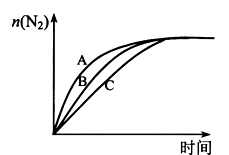
-
(4) 在汽车尾气的净化装置中 CO和NO发生反应:2NO(g) + 2CO(g)
 N2(g) + 2CO2(g) △H2 =-746.8 kJ•mol-1。实验测得,υ正=k正•c2(NO) •c2(CO) ,υ逆=k逆•c(N2) •c2(CO2) (k正、k逆为速率常数,只与温度有关)。
N2(g) + 2CO2(g) △H2 =-746.8 kJ•mol-1。实验测得,υ正=k正•c2(NO) •c2(CO) ,υ逆=k逆•c(N2) •c2(CO2) (k正、k逆为速率常数,只与温度有关)。 ①达到平衡后,仅升高温度,k正增大的倍数(填" >”、“< ”或“=”) k逆增大的倍数。
②若在1L 的密闭容器中充入1 mol CO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则
 =(保留2位有效数字)。
=(保留2位有效数字)。
反应1:C4H10(g,正丁烷)  CH4(g)+C3H6(g) △H1
CH4(g)+C3H6(g) △H1
反应2:C4H10(g,正丁烷)  C2H6(g)+C2H4(g) △H2
C2H6(g)+C2H4(g) △H2
已知几种烃的燃烧热如下:
| 烃 | 正丁烷 | 异丁烷 | 甲烷 | 乙烷 | 乙烯 | 丙烯 |
| 燃烧热(△H)/( kJ∙mol−1) | −2878 | −2869 | −890.3 | −1559.8 | −1411 | −2058.3 |
回答下列问题:
-
(1) 根据上述数据计算,△H1= kJ∙mol−1。
-
(2) 稳定性:正丁烷异丁烷(填“大于”“小于”或“等于”)。
-
(3) 在密闭容器中投入一定量的正丁烷,发生上述反应1和2,测定丁烷的平衡转化率(α)与压强(p)、温度(T)关系如图所示。
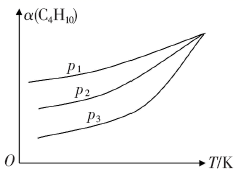
①在相同压强下,升高温度,丁烷的平衡转化率增大的原因是。
②比较压强大小:p1p2p3(填“>”“<”或“=”)。
-
(4) 某温度下,向2L恒容密闭容器中投入2mol正丁烷.假设控制反应条件,只发生反应1,达到平衡时测得CH4的体积分数为
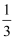 。
。 ①下列情况表明上述反应达到平衡的是(填字母,双选)。
A.混合气体的密度保持不变 B.甲烷、丙烯的生成速率相等
C.混合气体压强保持不变 D.丙烯体积分数保持不变
②该温度下,反应1的平衡常数K=。
 2NH3(g)的反应热和化学平衡常数分别为△H和K, 则相同温度时反应4NH3(g)
2NH3(g)的反应热和化学平衡常数分别为△H和K, 则相同温度时反应4NH3(g)  2N2(g)+6H2(g)反应热和化学平衡常数为( )
2N2(g)+6H2(g)反应热和化学平衡常数为( )
-
(1) 下列有关获取原料气的说法正确的是___________。A . 可通过液化空气分离法得到氮气 B . 可用煤、天然气与水蒸气反应制备水煤气,进而获取氢气 C . 原料气需经净化处理以防催化剂中毒 D . 电解水法获取氢气是一种较为廉价且高效的方法
-
(2) 原料气中的杂质气体H2S可用过量氨水净化吸收,写出化学反应方程式。
-
(3) 工业生产中氮气与氢气按物质的量之比为1:2.8进行投料,合成塔压强p恒定。若起始时氮气通入量为xmol,一段时间后测得氮气的平衡转化率为80%,用平衡分压代替平衡浓度表示平衡常数的KP=(用p表示,气体分压=总压ⅹ物质的量分数)
-
(4) 据统计,每年全世界在合成氨工业中向外排放CO2高达40亿吨,为循环使用CO2减少浪费,常见的方法是利用合成氨的产品NH3和副产品CO2合成尿素:
①2NH3(g)+CO2(g)
 NH2COONH4(l)
NH2COONH4(l) 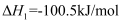 Ea1
Ea1②NH2COONH4(l)
 CO(NH2)2(l)+H2O(l)
CO(NH2)2(l)+H2O(l) 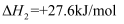 Ea2
Ea2副反应:NH2COONH4+H2O=(NH4)2CO3
已知活化能大小:Ea1<<Ea2
某科研小组模拟工业合成尿素生产,发现反应温度在140℃时生成尿素的反应速率反而比80℃小,可能原因是。
-
(5) 工业合成尿素中,通常氨碳投料比大于2,请分析可能原因___________。A . 氨易获得,成本较低 B . 氨过剩可提高二氧化碳的转化率,加快合成速率 C . 氨气可与体系内水结合,减少氨基甲酸铵水解,抑制副反应发生 D . 氨结合水,促进反应②正向移动

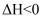 。在一定温度和压强下,于密闭容器中投入一定量C2H4和H2 , 反应达到平衡。下列说法正确的是( )
。在一定温度和压强下,于密闭容器中投入一定量C2H4和H2 , 反应达到平衡。下列说法正确的是( )
 增大
B . 增大容器容积,平衡正向移动,乙烷浓度
增大
B . 增大容器容积,平衡正向移动,乙烷浓度 增大
C . 保持容积不变,升高体系温度,平衡常数K减小
D . 保持容积不变,再充入一定量H2 , 乙烷体积分数
增大
C . 保持容积不变,升高体系温度,平衡常数K减小
D . 保持容积不变,再充入一定量H2 , 乙烷体积分数 增大
增大
反应Ⅰ: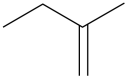 (A)+CH3OH
(A)+CH3OH
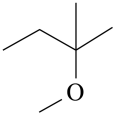 (TAME) ΔH1
(TAME) ΔH1
反应Ⅱ: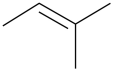 (B) +CH3OH
(B) +CH3OH
 (TAME) ΔH2
(TAME) ΔH2
反应Ⅲ:

 ΔH3
ΔH3
回答下列问题:
-
(1) 反应Ⅰ、Ⅱ、Ⅲ以物质的量分数表示的平衡常数
 与温度T变化关系如图1所示。
与温度T变化关系如图1所示。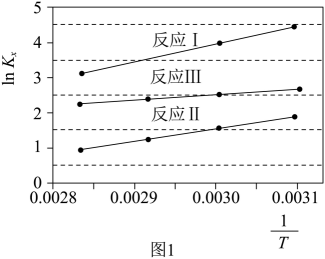
①物质A和B中相对稳定的是(用“A”或“B”表示);
②
 的数值范围是(填标号)。
的数值范围是(填标号)。A.<-1 B.-1~0 C.0~1 D.>1
-
(2) 为研究上述反应体系的平衡关系,向某反应容器中加入
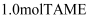 , 控制温度353K,测得TAME的平衡转化率为α。已知反应Ⅲ的平衡常数
, 控制温度353K,测得TAME的平衡转化率为α。已知反应Ⅲ的平衡常数
①平衡体系中B的物质的量为mol,
②反应Ⅰ的平衡常数
 。
。③同温同压下,再向该容器中注入惰性溶剂四氢呋喃稀释,请判断对反应Ⅰ的化学平衡的影响并说明理由
-
(3) 为研究反应体系的动力学行为,向盛有四氢呋喃的另一容器中加入一定量A、B和
 。控制温度为353K,A、B物质的量浓度c随反应时间t的变化如图2所示。
。控制温度为353K,A、B物质的量浓度c随反应时间t的变化如图2所示。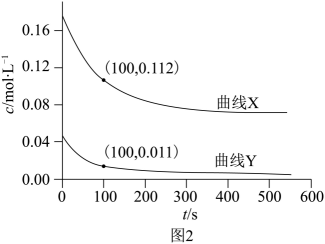
①代表B的变化曲线为(填“X”或Y”);
②
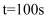 时,判断反应Ⅲ的正反应速率
时,判断反应Ⅲ的正反应速率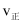 和逆反应速率
和逆反应速率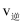 的大小并说明理由
的大小并说明理由
- 下列金属中一定以化合物形态存在于矿物之中的是( ) A.金 B.银
- 铁是一种应用广泛的金属,下列有关铁的说法中,正确的是( ) A、铁丝在氧气中燃烧生成氧化铁 B、铁在干燥
- 佛山《梁氏家谱》中记载:“明宣德四年,祖庙门前明堂狭隘,又多建铸造炉房,堪舆家言,玄武神前不宜火炎,慧(梁文慧)遂与里人
- 如图所示的匀强电场E=103N/C,矩形abcd的ab边与电场线平行,且ab=3 cm,bc=2 cm,将点电荷q=5×
- 【情境】小林晚上要参加少年宫组织的一项活动,放学后打电话告诉妈妈准备晚饭. 小明说:
- 仙人掌适宜生活在干旱的沙漠中,影响它分布的非生物因素是( )A.水分 B.温度
- 下列比较大小正确的是 ( ) A. B. C. D.
- 下面没有说明事物特征的句子是() A、针鼹的外形和刺猬差不多,长300~450毫米,宽不到70毫米,雄的略大一些。 B、
- (8分)下图是某药物中间体的结构示意图:试回答下列问题:⑴观察上面的结构式与立体模型,通过对比指出结构式中的“Et”表示
- 丙烯和某气态烃的混合物,其中H的质量分数小于14.26%,则与丙烯混合的气态烃可能是( )A.甲烷
- 给定整数,设 是抛物线与直线的一个交点. 试证明对于任意正整数,必存在整数,使为抛物线与直线的一个交点.
- 四川雅安历史悠久,先秦时代就已纳入中央政府管辖,历史文化底蕴丰厚,以下与雅安地区进入中原政权版图有关的是 A.开凿灵渠,
- 阅读资料,完成下列问题。 材料一 图16 沿海地区产业结构变化 材料二 农业劳动力非农就业转移较耕地面积减少越快
- 如图3-6-12所示,甲、乙两个完全相同的线圈,在距地面同一高度处由静止开始释放,A、B是边界范围、磁感应强度的大小和方
- 下列高聚物必须是由两种单体缩聚而成的是( ) B、 ,
- The hurricane did damage to many houses and business buildin
- 在培育三倍体无籽西瓜过程中,收获三倍体种子是在 ( ) A.第一年、二倍体母本上 B.第一年、四倍体母
- 阿伏加德罗常数值为NA,下列说法中正确的是 A.一定条件下3.2gSO2与足量O2反应转移电子数为0.1NA B.2.9
- 下列说法符合事实的是( ) A.漂白粉的有效成分是氯酸钠 B.碘化钾的水溶液遇淀粉显蓝色 C.硫在空气中燃烧生成S
- 如图为镁--次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是A.该燃料电池中镁为负极,发生还原反应 B.电池的总反应