反应热的大小比较 知识点
反应热的大小比较 知识点题库
已知700K时,N2+3H2  2NH3 ΔH=-Q kJ/mol,现有甲、乙两个容积相等的密闭容器。保持700K条件下,向密闭容器甲中通入1molN2和3molH2 , 达平衡时放出热量 Q1kJ;向密闭容器乙中通入0.5molN2和1.5molH2 , 达平衡时放出热量 Q2kJ。则Q、Q1、Q2的大小关系是( )
2NH3 ΔH=-Q kJ/mol,现有甲、乙两个容积相等的密闭容器。保持700K条件下,向密闭容器甲中通入1molN2和3molH2 , 达平衡时放出热量 Q1kJ;向密闭容器乙中通入0.5molN2和1.5molH2 , 达平衡时放出热量 Q2kJ。则Q、Q1、Q2的大小关系是( )
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理如下,下列说法正确的是 ( )
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);ΔH=+49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);ΔH=-192.9 kJ·mol-1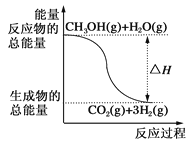
C(s)+O2(g)═CO2(g)△H1
CO2(g)+C(s)═2CO(g)△H2
2CO(g)+O2(g)═2CO2(g)△H3
4Fe(s)+3O2(g)═2Fe2O3(s)△H4
3CO(g)+Fe2O3(s)═3CO2(g)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
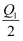 B . Q2<
B . Q2< 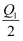 =197 kJ
C . Q2<Q1<197 kJ
D . Q1=Q2=197 kJ
=197 kJ
C . Q2<Q1<197 kJ
D . Q1=Q2=197 kJ
 O2(g)═CO(g)△H2
B . S(s)+O2(g)═SO2(g)△H1; S(s)+O2(g)═SO2(s)△H2
C . 2H2(s)+O2(g)═2H2O(g)△H1 H2(s)+
O2(g)═CO(g)△H2
B . S(s)+O2(g)═SO2(g)△H1; S(s)+O2(g)═SO2(s)△H2
C . 2H2(s)+O2(g)═2H2O(g)△H1 H2(s)+  O2(g)═H2O(g)△H2
D . CaO(s)+H2O(l)═Ca(OH)2(s)△H1; CaCO3(s)═CaO(s)+CO2(g)△H2
O2(g)═H2O(g)△H2
D . CaO(s)+H2O(l)═Ca(OH)2(s)△H1; CaCO3(s)═CaO(s)+CO2(g)△H2
①C (s)+O2(g)═CO2(g)△H1 C(s)+  O2(g)═CO(g)△H2
O2(g)═CO(g)△H2
②S(s)+O2(g)═SO2(g)△H1 S(g)+O2(g)═SO2(g)△H2
③H2(g)+  O2(g)═H2O(l)△H1 2H2(g)+O2(g)═2H2O(l)△H2
O2(g)═H2O(l)△H1 2H2(g)+O2(g)═2H2O(l)△H2
④CaO(s)+H2O(l)═Ca(OH)2(s)△H1CaCO3(s)═CaO(s)+CO2(g)△H2 .
 O2(g)=CO2(g);△H12CO(g)+O2(g)=2CO2(g);△H2
D . H2(g)+Cl2(g)=2HCl(g);△H1
O2(g)=CO2(g);△H12CO(g)+O2(g)=2CO2(g);△H2
D . H2(g)+Cl2(g)=2HCl(g);△H1  H2(g)+
H2(g)+  Cl2(g)=HCl(g);△H2
Cl2(g)=HCl(g);△H2
①C(s)+O2(g)= CO2(g)ΔH1;C(s)+ 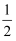 O2(g)= CO(g)ΔH2
O2(g)= CO(g)ΔH2
②S(s)+O2(g)= SO2(g)ΔH3;S(g)+O2(g)=SO2(g)ΔH4
③H2(g)+ 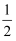 O2(g)=H2O(l)ΔH5;2H2(g)+O2(g)= 2H2O(l)ΔH6
O2(g)=H2O(l)ΔH5;2H2(g)+O2(g)= 2H2O(l)ΔH6
④CaCO3(s)= CaO(s)+CO2(g)ΔH7;CaO(s)+H2O(l)= Ca(OH)2(s)ΔH8
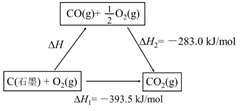
 O2(g) = CO(g) ΔH=ΔH1-ΔH2
D . 化学反应的ΔH , 只与反应体系的始态和终态有关,与反应途径无关
O2(g) = CO(g) ΔH=ΔH1-ΔH2
D . 化学反应的ΔH , 只与反应体系的始态和终态有关,与反应途径无关
a. 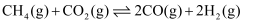 ∆H1
∆H1
b. 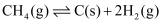 ∆H2
∆H2
c. 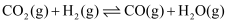 ∆H3
∆H3
d.  ∆H4
∆H4
e. 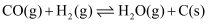 ∆H5
∆H5
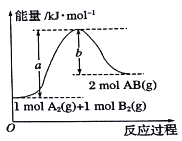
反应Ⅰ: ;
;
反应Ⅱ: 。
。
回答下列问题:
-
(1) 能否通过反应Ⅰ判断等物质的量的CO、
 具有能量的高低?(填“能”或“不能”)。
具有能量的高低?(填“能”或“不能”)。
-
(2) CO的燃烧热
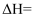
 。
。
-
(3) 下列各图中表示反应Ⅱ能量变化的是____(填字母)。A .
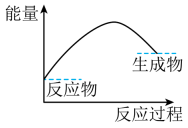 B .
B . 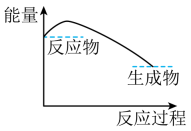 C .
C . 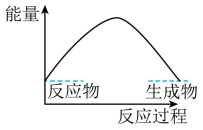 D .
D . 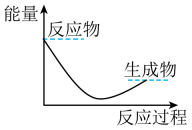
-
(4)
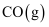 与
与 反应生成
反应生成 , 该反应的热化学方程式为。
, 该反应的热化学方程式为。
-
(5) 依据反应Ⅱ,
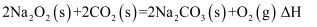 (填“>”“<”或“=”)
(填“>”“<”或“=”)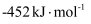 。
。
- 2010年12月21—22日召开的中央农村工作会议指出,要综合施策、多措并举,提高农民职业技能和创收能力,千方百计增加农
- 甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究。操 作现 象 通入氯气至过量I.A中溶液变红 II.稍后
- 66. 我突然想起今晚我该拜访杰克。 It ①____ ②____me that I should ③____ ④_
- 复数的虚部为 A. B. C. D.
- 元素周期表是学习和研究化学的重要工具,请回答下列问题: (1)元素周期表共有 个横行,18个纵行,每一个横行叫做一个,每
- 下列各组词语中,有两个错别字的一组是 ( ) A.能耗 戴手饰 一诺千斤 趁长风破万里浪 B.瑕
- 复数(i是虚数单位)的虚部为
- 初生牛犊能够通过初乳从母体获得特异性免疫力。初乳是母牛分娩后5-7天内所产生的乳,抗体含量比常乳高20-25倍,并且初乳
- 下列有关SO2的叙述不正确的是( )A.能使品红溶液褪色,加热后溶液仍为无色B.能使品红试液褪色,加热后溶液恢复原
- He can swim. _______ . A. So I can B. So can IC. I so can D.
- Can you ______ your sister from that group of girls?A. brin
- 女娲炼石补天处, 。(李贺《李凭箜篌引》)
- 在极坐标系中,圆的圆心的极坐标是 A. B. C. D.
- 读世界人口出生率、死亡率、自然增长率比较图(1998年),回答下列问题。⑴发达国家的人口出生率 ,死亡率
- 下图是工业区位选择模式图,其中线段长短表示影响程度大小,下列情况与甲、乙、丙、丁四图相符的是( )A、甘蔗制糖、制
- 下列物质中能用斐林试剂检测的是 A.胰高血糖素 B.葡萄糖 C.胰岛素 D.神经
- 近一年来,全国人大先后组织了6个执法检查组,对全国人大制定的有关法律的实施情况进行检查。同时,为进一步提高预算审查工作质
- I don’t know if the dictionary is worth___________. A. cos
- 苍蝇、蚊子的后翅退化成平衡棒,可在飞行中保证身体稳定。决定该特征出现的根本原因是 A、适应环境 B、新陈代谢
- 下列是某兴趣小组制取、收集并检验CO2的有关实验操作,其中错误的是 甲



