元素周期律 知识点题库
依据下列说法来判断相应元素的金属性、非金属性强弱,不合理的是( )
A . 卤素单质Cl2、Br2、I2的氧化性
B . 气态氢化物NH3、H2O、HF的稳定性
C . 碱金属单质Li、Na、K与水反应的剧烈程度
D . 1mol Na、Mg、Al分别与足量盐酸反应时失电子数的多少
下列不能作为元素周期表中元素排列的顺序的依据是( )
A . 原子的核电荷数
B . 原子的中子数
C . 原子的质子数
D . 原子的核外电子数
几种短周期元素的原子半径及主要化合价如下表:
元素代号 | X | Y | Z | M | R | Q | |
原子半径(×10﹣10m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | ﹣﹣ |
最低负价 | ﹣﹣ | ﹣1 | ﹣﹣ | ﹣﹣﹣ | ﹣3 | ﹣2 | |
下列说法正确的是( )
A . 元素X和Q形成的化合物中不可能含有共价键
B . X、Z、M的单质分别与水反应,Z最剧烈
C . X、Z、R的最高价氧化物对应的水化物之间可两两相互反应
D . Y的氧化物对应的水化物的酸性一定强于R的氧化物对应水化物的酸性
短周期元素X,Y,Z,W在元素周期表中的相对位置如图所示.已知Y,W的原子序数之和是Z的3倍,下列说法正确的是( )
Y | Z | ||
X | W |
A . 原子半径:X<Y<Z
B . 气态氢化物的稳定性:X>Z
C . Z,W均可与Mg形成离子化合物
D . 最高价氧化物对应水化物的酸性:Y>W
短周期主族元素X,Y,Z,W的原子序数依次增大.X原子最外层比次外层多3个电子;Y,Z均为金属,Y是同周期中原子半径最大的元素,Z的简单离子半径在同周期元素中最小;W的最高价氧化物在无机含氧酸中酸性最强.下列说法正确的是( )
A . X的气态氢化物的热稳定性比O(氧)的强
B . 元素Z,W的简单离子具有相同的电子层结构
C . Y,Z,W的最高价氧化物对应的水化物之间能相互反应
D . 等质量的Y和Z单质分别与足量稀盐酸反应,前者产生的氢气多
下列各题中有关物质的比较,请用“>”、“<”、“=”填空:
-
(1) 酸性:H3PO4HNO3 , H2SO4HClO4;
-
(2) 碱性:Mg(OH)2Ca(OH)2 , NaOHAl(OH)3
-
(3) 氧化性:F2S,N2O2;
-
(4) 热稳定性:CH4NH3 , HClHI.
表为元素周期表中的一部分,列出了10种元素在元素周期表中的位置.试用元素符号、离子符号或化学式回答下列问题.
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
第2周期 | ⑥ | ⑦ | ||||||
第3周期 | ① | ③ | ⑤ | ⑧ | ⑨ | ⑩ | ||
第4周期 | ② | ④ |
-
(1) 10种元素中,化学性质最不活泼的是;(填元素符号)
-
(2) ①③⑤三种元素最高价氧化物对应水化物中,碱性最强的是,(填化学式)该物质内部含有的化学键类型是和;
-
(3) 元素⑦的氢化物的化学式为;该氢化物常温下和元素②的单质反应的化学方程式;
-
(4) ③和⑨两元素形成化合物的电子式是;①和⑦两元素形成四核化合物的电子式是,该物质与CO2反应的化学方程式为;
-
(5) ①和⑤最高价氧化物对应水化物相互反应的离子方程式为:.
图为元素周期表中短周期的一部分,  四种元素中只有一种是金属,下列说法错误的是( )
四种元素中只有一种是金属,下列说法错误的是( )
A . 气态氢化物稳定性:R>Q
B . 元素T的离子结构示意图为 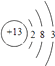 C . 与W同主族的某元素形成的18电子的氢化物分子中既有极性键又有非极性键
D . Q的一种同位素可用于测定文物的年代
C . 与W同主族的某元素形成的18电子的氢化物分子中既有极性键又有非极性键
D . Q的一种同位素可用于测定文物的年代
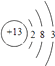 C . 与W同主族的某元素形成的18电子的氢化物分子中既有极性键又有非极性键
D . Q的一种同位素可用于测定文物的年代
C . 与W同主族的某元素形成的18电子的氢化物分子中既有极性键又有非极性键
D . Q的一种同位素可用于测定文物的年代
有四种短周期元素,它们的结构、性质等信息如下表所述:
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
B | B与A同周期,其最高价氧化物的水化物呈两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
请根据表中信息填写:
-
(1) A原子的核外电子排布式.
-
(2) B元素在周期表中的位置;离子半径:BA(填“大于”或“小于”).
-
(3) C原子的电子排布图是,其原子核外有个未成对电子,能量最高的电子为轨道上的电子,其轨道呈形.
-
(4) D原子的电子排布式为,D﹣的结构示意图是.
-
(5) B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为与D的氢化物的水化物反应的化学方程式为.
已知W、X、Y、Z为原子序数依次增大的短周期元素,W与Z同主族,X与Y同周期,且Y与Z的原子序数之和为20。Y单质能与无色无味液体m反应置换出X单质,Z单质也能与m反应置换出W单质。W、X、Y均能与Z形成离子化合物。下列说法错误的是()
A . X、Z两元素的简单离子电子层结构相同
B . X与Z形成的离子化合物一定只含有离子键
C . Y的氢化物比X的氢化物稳定
D . W与Y形成的化合物WY可刻蚀玻璃
下列各组比较中不正确的是()
A . 锂与水反应不如钠与水反应剧烈
B . 还原性:K>Na>Li,故K可以从NaCl溶液中置换出金属钠
C . 熔、沸点:Li>Na>K
D . 碱性:LiOH<NaOH<KOH
-
(1) 工业上用和为原料制取漂白粉,有效成分是,制备原理是(方程式表示)。漂白粉用于漂白的时候,最好与稀盐酸反应,有关化学方程式为。
-
(2) Ca元素在周期表中的位置是 ,Ca与最活泼的非金属元素A形成化合物D,D的电子式为,HCl的沸点比A与H形成的化合物HA的沸点(填“高”或“低”)。
几种短周期元素的原子半径及主要化合价如下表,下列说法正确的是( )
| 元素代号 | X | Y | Z | M | R | Q |
| 原子半径 | 0.37 | 1.86 | 1.43 | 0.99 | 0.75 | 0.74 |
| 最高正价 | +1 | +1 | +3 | +7 | +5 | |
| 最低负价 | -1 | -1 | -3 | -2 |
A . 离子半径:Y>Z>M
B . Y、Z、M三种元素的最高价氧化物的水化物两两之间会反应
C . 化合物XM、YM都是电解质,熔融状态下都能导电
D . 气态氢化物稳定性R>Q
按电子排布,可把周期表里的元素划分成5个区,以下元素属于p 区的是( )
A . Fe
B . Mg
C . Cu
D . As
下列元素属于ⅦA族的是( )
A . 氧
B . 氯
C . 钠
D . 硫
下列元素的原子半径最大的是( )
A . F
B . Cl
C . Br
D . I
短周期元素W、X、Y和Z的原子序数依次增大。W是宇宙中最丰富的元素,W2X是维持生命过程的必需物质,WY可用于玻璃的刻蚀,ZX2是酸雨的主要形成原因之一,室温下化合物ZY4是气体。下列说法错误的是( )
A . Y元素的非金属性最强
B . W2X的沸点高于W2Z的沸点
C . ZY4分子中原子最外层均为8电子结构
D . X和W形成的化合物为H,Z和W形成的化合物为M,H和M可能发生氧化还原反应
图中是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
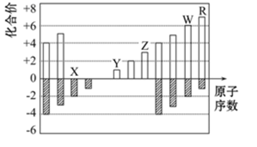
A . 原子半径:Z>Y>X
B . 气态氢化物稳定性:R<W
C . WX3和水反应生成的化合物是离子化合物
D . Y和Z两者最高价氧化物对应的水化物能相互反应
下列下列关于F、Cl、Br、I的比较,错误的是( )
A . 单质的氧化性随核电荷数的增加而减弱
B . 单质的颜色随核电荷数的增加而加深
C . 它们的氢化物的稳定性随核电荷数的增加而增强
D . 它们的原子核外电子层数随核电荷数的增加而增多
LDFCB是电池的一种电解质,该电解质阴离子由同周期元素原子W、X、Y、Z构成,结构如图,Y的最外层电子数等于X的核外电子总数,下列说法正确的是( )
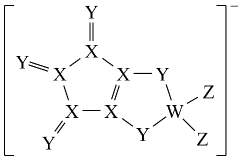
A . 同周期元素第一电离能小于Y的有5种
B . 简单氢化物的还原性:X<Y
C . 四种元素中原子半径最大的是W
D . 四种元素形成的单质中Y的氧化性最强
最近更新
- 有史学家认为:从秦汉起,官僚体制就是中国制度的核心问题,而这个核心问题又可以分成两个大的子问题,一是官僚的选拔问题,二是
- 原核生物中某一基因的编码区起始端插入了一个碱基对。在插入位点的附近,再发生下列哪种情况有可能对其编码的蛋白质结构影响最小
- 中国古代对县级行政区的划分设置有个现象,即原有的县域经济富裕、人口密集了就再分出区域增设县治。此做法最主要考虑是
- ......
- 2010年的上海世博会是探讨人类城市生活的盛会,同时也是人类文化的盛宴,是与人类文明的一次精彩对话。假如你有幸成为志愿者
- 下列选项与第一次工业革命有关的是( )①珍妮机 ②蒸汽机 ③火车 ④汽车 ⑤飞机 ⑥轮船 ⑦电动机
- 我国发射的“嫦娥一号”探月卫星简化后的路线示意图如图所示。卫星由地面发射后,经过发射轨道进入停泊轨道,然后在停泊轨道经过
- 阅读下文,完成后面问题(7分) 我把麻雀养在天空里 ①有一年夏天我买了水耕箱,试作无土栽培,希望不用碰触泥土也能享有
- 阅读下面的文言文,完成1~4题。 廖刚字用中,南剑州顺昌人。宣和初,自漳州司录除国子录,擢监察御史。时蔡京当国,刚论秦无
- 下列各组物质的溶液混合后,能发生反应,且反应前后溶液的总质量不变的是( )A.NaOH和HClB.KNO3和NaO
- 孙中山在《民报》创刊周年庆祝大会上演讲道:“照现在这样的政治论起来,就算汉人为君主,也不能不革命。”此话反映了他主张(
- 下列各项中没有错别字的一项是 ( ) A.踯躅不前 鞠躬尽瘁 无计于事 赍赏B.夙
- 如图所示,在矩形ABCD区域内,对角线BD以上的区域存在有平行于AD向下的匀强电场,对角线BD以下的区域存在有垂直于纸面
- 某班开展历史知识竞猜活动。有一谜语的谜面上有“南湖游船、开天辟地、焕然一新”等词,它的谜底是( ) A.五四爱国运动
- 下列化合物中,既含有极性键又含有非极性键的是 A.Na2O2 B.NH4Cl C.CH4 D
- 人类的多指症是常染色体显性基因控制的遗传病,在人群中的发病率很低。下列针对控制该病基因的解释正确的是
- 下列图示实验正确的是()
- 下表显示X、Y两地同年出现地震的有关资料。X地位于美国西部,Y地位于印度中部。读表回答7-9题。 地点 人口密度 (人
- 当抗原刺激机体产生细胞免疫反应时,效应T细胞发挥的作用是 () A.产生抗体使靶细胞裂解 B.激活靶
- 北京市积极推进电子政务,在各区县政府网站上相机开设了行业服务咨询、举报投诉信箱、网上评议等专栏,有效地推进了政务的公平、



