常见金属元素的单质及其化合物的综合应用 知识点题库
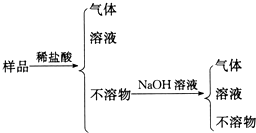
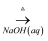 NaAlO2(aq)
NaAlO2(aq)  Al(OH)3
B . S
Al(OH)3
B . S  SO3
SO3  H2SO4
C . Mg(OH)2
H2SO4
C . Mg(OH)2  MgCl2(aq)
MgCl2(aq)  无水MgCl2
D . Fe
无水MgCl2
D . Fe  Fe2O3
Fe2O3  FeCl3
FeCl3
-
(1) 在元素周期表中,铜、银、金元素位于同一族,它们基态原子的价层电子排布式中各能级上的电子数相等,各能层数依次增大,其通式为(用n表示核外电子层数);铜元素所在周期中,基态原子未成对电子数最多的原子M 的价层电子轨道表达式为.
-
(2) 乙醛是重要的化工原料,①CH3CH2OH、CH3CHO的沸点分别为78.5℃、20.8℃,它们的相对分子质量相差2,而沸点相差比较大,其主要原因.
②在H、C、N、O中,第一电离能最大的元素和电负性最大的元素组成的化合物的化学式为(填一种即可),CH4、NH3、H2O分子的键角从大到小的顺序为.
-
(3) 金不溶于硝酸,但溶于“王水”,发生如下反应:Au+4HCl+HNO3═H+NO+2H2O,金溶于王水的主要原因是形成了﹣ , 提高了金的活泼性.在﹣中配位键的数目为,写出该离子的结构式:.
-
(4) 金、银的一种合金具有较强的储氢能力.该合金的晶胞为面心立方结构,银原子位于面心,金原子位于顶点.该合金的化学式可以表示为.
-
(5) Cu(OH)2难溶于氢氧化钠溶液,但是易溶于浓氨水,用离子方程式表示其主要原因:.
①取适量粉末投入蒸馏水中,粉末完全溶解,得到蓝色透明溶液A.
②取A溶液少量,向其中逐滴滴加烧碱溶液直到过量,观察到先有沉淀出现,而后沉淀逐渐增多,然后沉淀又逐渐减少,但最终仍有部分蓝色沉淀.
③再取A溶液两份,一份滴加BaCl2溶液后,出现白色沉淀;另一份滴加硝酸银溶液后也出现白色沉淀.
请回答下列问题:
-
(1) 原白色粉末一定含有,一定不含,可能含有.(填化学式)
-
(2) 写出过程②中涉及到的离子方程式:.
-
(3) 如果要进一步确定可能存在的物质,进行的实验操作及实验现象和结论是.
①CaCl2溶液;②Na2SiO3溶液;③Ca(OH)2溶液;④饱和Na2CO3溶液
① 
② 
③ 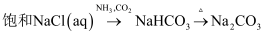
④ 
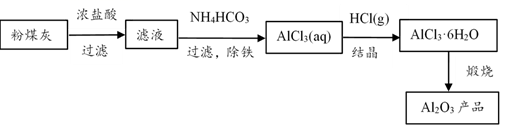
完成下列填空:
-
(1) 铝原子核外有种不同能量的电子,最外层电子的轨道式是,上述流程涉及第二周期元素的原子半径由小到大的顺序是。
-
(2) “除铁”是将Fe3+转化为Fe(OH)3沉淀,反应的离子方程式为,检验溶液中Fe3+是否除尽的方法是。
-
(3) 解释“结晶”过程中向AlCl3浓溶液中通入HCl气体的原因。
-
(4) 上述流程可循环的物质是。
-
(5) 工业上将Al2O3溶解在熔化的冰晶石中电解获得铝,该反应的化学方程式为。
 并探究其性质。
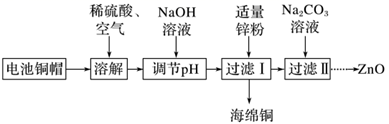
并探究其性质。 资料:  为紫色固体,微溶于
为紫色固体,微溶于 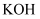 溶液;具有强氧化性,在酸性或中性溶液中快速产生
溶液;具有强氧化性,在酸性或中性溶液中快速产生  ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
-
(1) 制备
 (夹持装置略)
(夹持装置略) 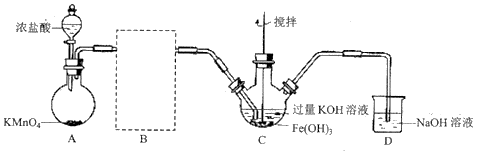
①A为氯气发生装置。A中反应的离子方程式为(锰被还原为
 )。
)。②请在B方框内将除杂装置补充完整,并标明所用试剂。
③
 中得到紫色固体和溶液。
中得到紫色固体和溶液。  中主要反应的化学方程式为。
中主要反应的化学方程式为。 -
(2) 探究
 的性质
的性质 ①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有
 。为证明是否
。为证明是否  氧化了
氧化了  而产生
而产生  ,设计以下方案:
,设计以下方案:方案Ⅰ
取少量a,滴加
 溶液至过量,溶液呈红色。
溶液至过量,溶液呈红色。方案Ⅱ
用KOH溶液充分洗涤C中所得固体,再用KOH溶液将
 溶出,得到紫色溶液b。取少量b,滴加盐酸,有
溶出,得到紫色溶液b。取少量b,滴加盐酸,有  产生。
产生。由方案Ⅰ中溶液变红可知a中含有的离子为,但该离子的产生不能判断一定是
 将
将  氧化,该离子还可能由产生(用离子方程式表示)。
氧化,该离子还可能由产生(用离子方程式表示)。②根据
 的制备实验得出:氧化性
的制备实验得出:氧化性 
 (填“>”或“<”),而方案Ⅱ实验表明,
(填“>”或“<”),而方案Ⅱ实验表明,  和
和  的氧化性强弱关系相反,原因是。
的氧化性强弱关系相反,原因是。③资料表明,酸性溶液中的氧化性
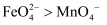 ,验证实验如下:将溶液
,验证实验如下:将溶液 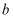 滴入
滴入 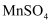 和足量
和足量  的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 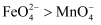 。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:。
。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:。
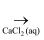 CaSO3
CaSO3  CaSO4
B . Fe3O4(s)
CaSO4
B . Fe3O4(s)  Fe(s)
Fe(s) 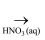 Fe(NO3)3(aq)
C . MgO(s)
Fe(NO3)3(aq)
C . MgO(s) 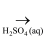 MgSO4(aq)
MgSO4(aq)  Mg(s)
D . Fe
Mg(s)
D . Fe 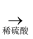 FeSO4(aq)
FeSO4(aq)  Fe(OH)2
Fe(OH)2  FeO
FeO
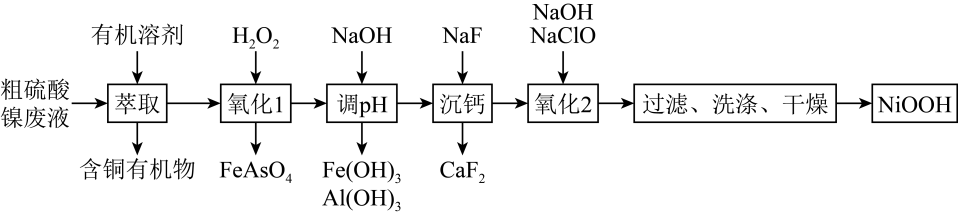
已知:Ksp(FeAsO4)=5.7×10-21 , H3AsO3的还原性比Fe2+强。
回答下列问题:
-
(1) “萃取”时需充分振荡,目的是。
-
(2) “氧化1”中H2O2的作用是,若该废液中H3AsO3和Fe2+的浓度分别是0.02 mol·L-1和0.12 mol·L-1 , 除去砷后的废液中c(
 )=mol·L-1(不考虑反应过程中溶液体积的微小变化)
)=mol·L-1(不考虑反应过程中溶液体积的微小变化)
-
(3) “沉钙”时,若溶液酸度过高,Ca2+沉淀不完全,原因是。
-
(4) “氧化2”反应的离子方程式为。
-
(5) “洗涤”时,检验产品是否洗涤干净的方法是。
-
(6) 已知某镍氢电池的离子导体为KOH溶液,电池反应为MH+NiOOH
 M+Ni(OH)2 , 则放电时,OH-移向电极(填“MH”或“NiOOH”),充电时NiOOH电极上的电极反应式为。
M+Ni(OH)2 , 则放电时,OH-移向电极(填“MH”或“NiOOH”),充电时NiOOH电极上的电极反应式为。
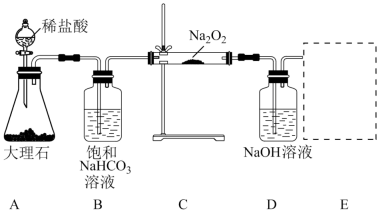
-
(1) 请用离子方程式表示B装置中饱和
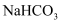 溶液的作用:,请写出装置C中发生的两个化学反应方程式、。
溶液的作用:,请写出装置C中发生的两个化学反应方程式、。
-
(2) 装置C中发生反应的还原剂为(写化学式),每生成1分子
 , 转移个电子。
, 转移个电子。
-
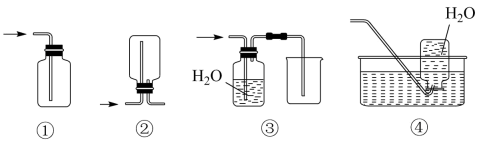
(3) E装置为氧气收集装置,下面4套气体收集装置中,合理的是(填序号)。
-
(4)
 溶液与
溶液与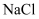 溶液外观高度相似,请设计实验鉴别这两种溶液,写出实验操作和现象。
溶液外观高度相似,请设计实验鉴别这两种溶液,写出实验操作和现象。
- 在“探究摩擦力大小与哪些因素有关”的实验中.实验室备有如下器材:长方体木块,砝码,长木板.弹簧测力计及细绳.关于“摩擦力
- 根据下列实验装置回答问题:(1)写出上图中下列仪器的名称: 用于加热的是 ;用于添加液体药品的是
- 运用所学的对偶修辞方法的知识,给下面春联补出下联。(4分) ①春风含瑞气,。 ②花香鸟语风光美,。
- 假设你是一个导游,带团重走红军长征路,下列哪个地点你们不会选择 ( )
- 下列变化中,属于物理变化的是 A.冰雪融化 B.天然气燃烧C.葡萄酿酒D.光合作用
- 阅读理解。阅读下列材料,从A、B、C、D四个选项中选出可以填入空白处的最佳答案。 News 1 Don’tplay Ru
- 《上海县竹枝词》有诗云:“卅年求富更求强,造炮成船法仿洋。海面未收功一战,总归虚牝掷金黄。”与上述内容有关的历史事件是
- 30.阅读下面的材料,按要求作文。(60分) 年轻人与一位老者饮茶,年轻人喝了一口茶说:“据我所知,茶叶在高温之中的形态
- 用序号填空:下列物质中属于单质的是_______,属于氧化物的是_______,属于盐的是_______。 A.H2OB
- 2008年7月10日,沙特哈立德国王大学城建设工程一期项目签约仪式在阿西尔省省会艾卜哈市隆重举行,该项目由中国广东新广国
- 2005年诺贝尔生理学或医学奖授予澳大利亚学者巴里•马歇尔和罗宾•沃伦,以表彰他们发现了导致胃炎和胃溃疡的病原体,如图为
- 一元二次方程(x-3)(x-5)=0的两根分别为() A、3,-5 B、-3,-5 C、-3,5 D
- 1943年,日本、伪满洲国、汪伪政权、泰国等联合发表宣言:“大东亚各国提携完成大东亚战争,把大东亚从英美的束缚中解放出来
- 如图(1),在△ABC中, .
- 以下农业区:①东北三省,②长江中下游区,③南部沿海区,④黄河中下游区与图示相应的耕作制度和主要农作物结构图,符合实际情况
- 设函数,则函数的零点个数为 ( ) A.1个 B.2个 C.3个 D.4个
- 假设你是李华,加拿大一所学校将于今年暑假组织学生来你校访问。其间,Andy Smith将借住你家。请你代表全家写
- 2003年春天,“非典型性肺炎”在我国人群中开始传染并且逐步扩散到各地,引起党和政府的高度关注。请问“非典”的病原体属于
- 在没有任何其他光照的情况下,舞台追光灯发出的红光照在穿白上衣、绿裙子的女演员身上,观众看到她的A.上衣呈红色,裙子呈黑色
- 随着我国互联网普及率不断提高,电子商务发展迅速,网上消费需求呈现几何式增长的趋势。截至2011年6月,中国网购人数达到l



