铁的化学性质 知识点题库
在硫酸亚铁、硫酸铁和硫酸铜溶液中加入铁粉,充分反应后,滤出的不溶物除铜粉外,尚有少量铁粉,那么在滤液中( )
A . 肯定有Fe2+ , 可能有Fe3+
B . 只有Fe2+ , 没有Fe3+和Cu2+
C . 可能有Fe3+ , 可能有Cu2+
D . 肯定有Fe2+ , 可能有Fe3+、Cu2+
下列有关说法中不正确的是( )
A . 铁与Cl2、盐酸均能发生反应,但生成的含铁物质组成不同
B . 分别加热蒸干并灼烧铁、铝的氯化物溶液,最后得到的物质均为金属氧化物
C . 等物质的量的Na、Cu、Al与足量氯气反应时,消耗的氯气一样多
D . 常温下,铁片、铝片与浓硫酸的反应均只能停留在金属的表面上
下列化合物能由单质直接化合生成的是( )
A . NO2
B . FeCl3
C . SO3
D . FeCl2
下列实验方案可行的是( )
A . 用浓硫酸干燥氨气
B . 用酚酞试液检验酸性溶液
C . 通入Cl2除去FeCl3溶液中的FeCl2
D . 加入Fe粉除去Al3+溶液中的杂质Cu2+
部分金属可以与水在一定条件下发生反应.
-
(1) 将一小块金属钠投入盛有水的烧杯中,待完全反应后,向其中滴加酚酞溶液.
①钠与水反应的化学方程式是.
②上述实验过程中,可观察到的实验现象有(填选项序号),产生现象b的原因是.
a.钠浮在水面
b.钠熔成小球
c.钠球在水面上四处游动,发出嘶嘶声,逐渐消失
d.反应后向烧杯中滴加酚酞溶液,溶液呈红色
-
(2) 铁粉可以与水蒸气在高温下反应,生成 (填化学式)和氢气.
同一还原剂与多种氧化剂在一起时,先与氧化性强的粒子反应,待强的反应完后,再与氧化性弱的反应,称为反应先后规律.已知氧化性:Fe3+>Cu2+ , 在溶有Fe2(SO4)3和CuSO4的溶液中加入铁粉,下列说法中不正确的是( )
A . 若铁粉有剩余,则不溶物中一定有铜
B . 若铁粉有剩余,则溶液中的金属阳离子只有Fe2+
C . 若铁粉无剩余,且溶液中有Cu2+ , 则溶液中一定无Fe3+
D . 若铁粉无剩余,且溶液中无Cu2+ , 则溶液中一定有Fe2+ , 一定无Fe3+
下列金属最易与H2O发生反应的是( )
A . Na
B . K
C . Al
D . Mg
下列物质反应后的溶液中加入KSCN溶液一定会变红色的( )
A . Fe2O3与HCl反应
B . 过量铁粉与稀硝酸反应
C . 少量铁粉与稀盐酸作用
D . 铁粉与CuSO4反应
下列反应不能通过一步反应实现的是( )
A . SiO2→H2SiO3
B . Cu→CuSO4
C . Fe→FeCl2
D . Al→Na[Al(OH)4]
已知一定条件下A,B,C,D之间的转化关系如右图所示。下列说法正确的是( )
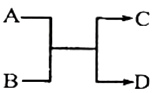
A . 若A为Fe,D为氢气,则B一定为酸
B . 若A,D为化合物,B为水,则C一定是气体单质
C . 若A,B,C,D均为化合物,该反应一定属于复分解反应
D . 若A,B,C,D均为10电子微粒(分子或离子),且C是可使湿润的红色石蕊试纸变蓝的气体,则D常温下一定呈液态
Fe与下列物质反应的产物,能使KSCN溶液显红色的是( )
A . H2O
B . O2
C . S
D . 足量稀HNO3
下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。
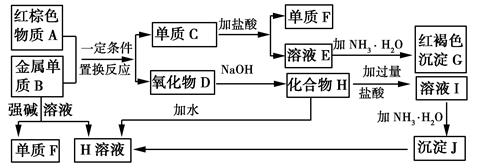
请回答下列问题:
-
(1) 物质A的化学式为。
-
(2) 写出单质B与强碱溶液反应的离子方程式,氧化物D与NaOH溶液反应的化学方程式。
-
(3) 溶液E中加入氨水时,先生成白色沉淀L,L最终变为红褐色沉淀G,写出L变为G的化学反应方程式。
-
(4) 溶液E敞口放置容易变质,写出检验溶液E是否变质的实验操作、现象及结论,为了防止溶液E的变质,可往溶液中加入。
-
(5) 溶液I中所含金属离子是。
为了探究铁铜及其化合物的性质,某同学设计并进行了下列实验。下列说法错误的是( )
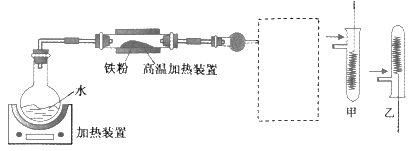
A . 高温加热装置中发生的反应为3Fe(s)+4H2O(g)  Fe3O4(s)+4H2(g)
B . 虚线框处宜选择的装置是甲
C . 实验时将螺旋状铜丝加热变黑后再趁热迅速伸入试管中,可观察到铜丝由黑色变为红色
D . 实验后,可用铝粉在高温下还原玻璃管中的固体获得铁单质
Fe3O4(s)+4H2(g)
B . 虚线框处宜选择的装置是甲
C . 实验时将螺旋状铜丝加热变黑后再趁热迅速伸入试管中,可观察到铜丝由黑色变为红色
D . 实验后,可用铝粉在高温下还原玻璃管中的固体获得铁单质
 Fe3O4(s)+4H2(g)
B . 虚线框处宜选择的装置是甲
C . 实验时将螺旋状铜丝加热变黑后再趁热迅速伸入试管中,可观察到铜丝由黑色变为红色
D . 实验后,可用铝粉在高温下还原玻璃管中的固体获得铁单质
Fe3O4(s)+4H2(g)
B . 虚线框处宜选择的装置是甲
C . 实验时将螺旋状铜丝加热变黑后再趁热迅速伸入试管中,可观察到铜丝由黑色变为红色
D . 实验后,可用铝粉在高温下还原玻璃管中的固体获得铁单质
反应条件会影响化学反应产物或现象。下列有关影响因素的分析错误的是( )
| 选项 | 反应物 | 反应产物或现象 | 影响因素 |
| A | C2H5OH、浓硫酸 | C2H4 或乙醚 | 温度 |
| B | Na、O2 | Na2O 或 Na2O2 | O2 用量 |
| C | Fe、H2SO4 | 有 H2或无 H2 | H2SO4的浓度 |
| D | 氯化铝溶液、氢氧化钠溶液 | 现象不同 | 试剂滴加顺序 |
A . A
B . B
C . C
D . D
给定条件下,下列选项中所示的物质间转化均能通过一步反应实现的是( )
A . 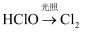 B .
B .  C .
C .  D .
D . 
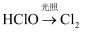 B .
B .  C .
C .  D .
D . 
化学与社会、生产,生活密切相关,下列说法正确的是( )
A . 宋·王希孟《千里江山图》卷中的绿色颜料铜绿的主要成分是氢氧化铜
B . 我国全面启动的北斗导航系统的信号与晶体硅有关
C . 当液氨罐泄漏时,人们应该向高处躲避,将其移入水塘中,并向水塘中加入熟石灰
D . 月饼包装袋中常放入小袋的黑色粉末,目的是防止食品氧化变质
已知甲、乙、丙、丁是四种常见物质,其转化关系如图所示。
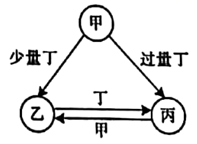
请回答下列问题:
-
(1) 若丁为O2 , 乙常温下为淡黄色单质固体。写出乙中所含元素在周期表中的位置,甲的分子式。
-
(2) 若丙和丁均为金属单质,且丙为我国目前生产量最大,使用最广泛的金属,甲和乙均为盐溶液。比较丙和丁还原性强弱:丙丁(写>、<、=),甲跟丙反应生成乙的离子方程式。
-
(3) 若甲、乙、丙的水溶液均呈碱性且丙可制胃药。写出甲和丙反应生成乙的化学方程式。
2019年国际非政府组织“全球碳计划”12月4日发布报告:研究显示,全球二氧化碳排放量增速趋缓。CO2的综合利用是解决温室问题的有效途径。
-
(1) CO2甲烷化反应是由法国化学家PaulSabatier提出的。CO2催化氢化制甲烷的研究过程如图所示:
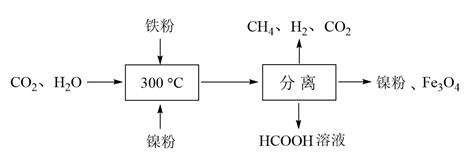
①上述过程中,产生H2反应的化学方程式为。
②HCOOH是CO2转化为CH4的中间体:CO2
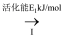 HCOOH
HCOOH 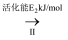 CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少。当增加镍粉用量时,CO2镍催化氢化制甲烷的两步发应中反应速率增加较大的一步是(填“I”或“II”)。
CH4。当镍粉用量增加10倍后,甲酸的产量迅速减少。当增加镍粉用量时,CO2镍催化氢化制甲烷的两步发应中反应速率增加较大的一步是(填“I”或“II”)。 -
(2) CO2经催化加氢可以生成低碳烃,主要有两个竞争反应:
反应I:CO2(g)+4H2(g)
 CH4(g)+2H2O(g)
CH4(g)+2H2O(g)反应II:2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)在1L恒容密闭容器中充入1molCO2和4molH2 , 测得平衡时有关物质的物质的量随温度变化如图所示。

T1℃时,CO2的转化率为。T1℃时,反应I的平衡常数K=。
-
(3) 已知CO2催化加氢合成乙醇的反应原理为2CO2(g)+6H2(g)
 C2H5OH(g)+3H2O(g)△H<0。m代表起始时的投料比,即m=
C2H5OH(g)+3H2O(g)△H<0。m代表起始时的投料比,即m=  。m=3时,该反应达到平衡状态后p(总)=20aMPa,恒压条件下各物质的物质的量分数与温度的关系如图。T4温度时,反应达到平衡时物质d的分压p(d)=。
。m=3时,该反应达到平衡状态后p(总)=20aMPa,恒压条件下各物质的物质的量分数与温度的关系如图。T4温度时,反应达到平衡时物质d的分压p(d)=。 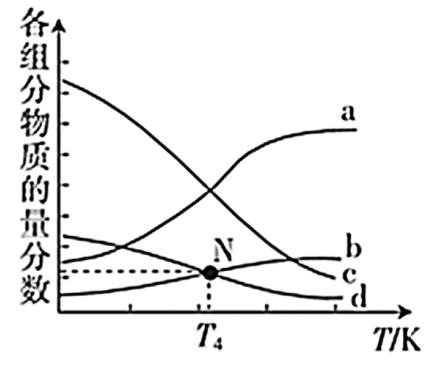
用硫铁矿烧渣(主要成分为Fe2O3和少量SiO2)为原料制取绿矾(FeSO4·7H2O),同时对绿矾在高温下的分解产物进行实验探究。
-
(1) Ⅰ.绿矾制备流程如下:
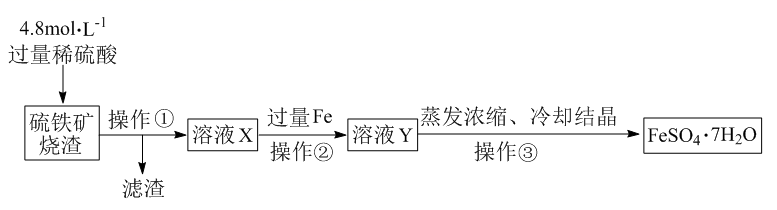 滤渣的主要化学成分是(填化学式)。
滤渣的主要化学成分是(填化学式)。 -
(2) 操作①、②、③是同一分离操作,该操作名称为。
-
(3) 向溶液X中加入过量的铁粉,发生的主要反应的离子方程式为。
-
(4) 若用含90%氧化铁的硫铁矿烧渣100 t,制得278 t绿矾,该工艺生产绿矾的产率为(保留三位有效数字,产率
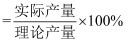 )。
)。
-
(5) Ⅱ.绿矾在高温下的分解产物实验探究
绿矾在加热至高温时会分解,为确定分解产物(已知产物中有SO3气体生成),设计如下实验装置进行了探究:
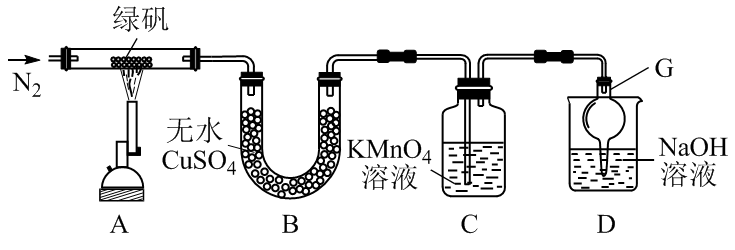
仪器G的名称为。
-
(6) 加热前,先通入一段时间氮气的目的是。
-
(7) 观察到的现象:玻璃直管中有红棕色的固体生成,B中白色固体变蓝,C中溶液褪色,请根据实验现象写出绿矾高温分解的化学方程式。
人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血。市场出售的某种麦片中含有微量、颗粒细小的铁粉,这些铁粉在人体胃酸(主要成分是HCl)作用下转化成亚铁盐。下列叙述不正确的是( )
A . 铁粉具有还原性
B . 铁是人体必需的微量元素
C . 亚铁盐溶液呈浅绿色
D . Fe+2H+=Fe3++H2↑
最近更新
- 右图是某微型实验的装置图。试管中反应发生后,(1)你可能观察到的现象有:
- 读“三种工业化城市化模式图”,完成(1)—(2)题。 (1)下列地区中,其发展模式与②相符的是 A.美国“硅谷”
- 已知集合, ,为集合到集合的一个函数,那么该函数的值域的不同情况有( )种。
- 已知函数在点处的切线为. (1)求函数的解析式; (2)若,且存在,使得成立,求的最小值.
- 1912年1月,孙中山自豪地说:“这是中国有史以来未有之变局,吾民破天荒之创举也。”孙中山所说的“变局”和“创举”是指
- 下列物质中,不属于抗原的是 A.异型红细胞 B.侵入体内的病毒C.移植的异体组织或器官 D.
- β-紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1。下列说法正确的是() A.β-紫罗兰酮
- 下列加线的字读音完全不相同的一组是( ) A.数落 数字 数典忘祖 数见不鲜 B.恶心 厌恶
- 已知集合M={a,b,c}中的三个元素可构成某一三角形的三边长,那么此三角形一定不是( ).A.直角三角形
- 根据下表数据,分析下列说法正确的是A.环境中氧气量最多 B.环境中二氧化碳少,是人体呼出的二氧化碳少 C.人体是吸入气体
- It is the preventionof disease_____ its successful treatmen
- 物质的量浓度相同的下列溶液中,符合按pH由小到大顺序排列的是:A、、、、B、、、、C、、、、D、、、、
- 某研究人员模拟肺炎双球菌转化实验,进行了以下4个实验:( ) ①S型菌的DNA + DNA酶→加入R型菌→注射入小鼠②
- .Using _____ illegal drugs can lead to health problems, and
- 劳动力商品使用价值的一个重要特点是,随着对它的消费( ) A.其使用价值消失,价值也消失 B.其使用价值和价值转移到新产
- 下图是北京孔庙的“万世师表”匾额,下列说法不正确的是( ) A、该匾额的题写者有可能是秦始皇 B、体现题写者对孔子
- .下列句子中有两个错字的一项是( ) A.张宇讲的鬼故事,让人听得毛骨耸然,有的女生听了之后晚上都不敢一个人走夜
- 签证是指一国主管机关在本国或外国公民所持的护照或其他旅行证件上签注、盖印,表示准其出入本国国境。近年来,我国在签证便利化
- It is rather difficult to make friends with her, but her fri
- 同志指出:“在认识和改造世界的过程中,哲学社会科学与自然科学同样重要;培养高水平的哲学社会科学家,与培养高水平的自然科学



