镁、铝的重要化合物 知识点题库
供选用的试剂:A、氢氧化钠溶液 B、稀盐酸 C、水
供选用的仪器:a、试管 b、胶头滴管 c、玻璃棒 d、酒精灯 e、镊子
(1)实验目的:检验试剂瓶中的金属片是镁还是铝
(2)选用的试剂和仪器(填编号)
①试剂: ;②仪器: ;
(3)实验步骤: .
(4)实验现象记录和结论:
①实验中,如果现象为 , 可判断该金属是镁;
②实验中,如果现象为 ,可判断该金属是铝;
(5)实验过程中发生反应的化学方程式为: .
①Al ②Al2O3③Al(OH)3④AlCl3⑤NaHCO3 .
( )
 B .
B .  C .
C . 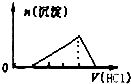 D .
D . 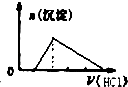
-
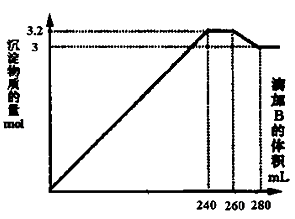
(1) 加入B溶液280mL时,溶液中的沉淀是 ,溶液中的溶质是(填化学式)。
-
(2) 加入B溶液240mL至260mL之间时,发生的离子反应方程式是。
-
(3) 将AB溶液中各溶质的物质的量浓度填入下表:
溶质
硫酸钠
氯化铝
氯化铁
物质的量浓度mol/L
①l: 3 ②2: 3 ③1: 4 ④2: 7
①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2
②铁露置在空气中一段时间后就会生锈,性质更活泼的铝不能稳定存在于空气中
③Al(OH)3、Cu(OH)2受热易分解,Fe(OH)3受热也易分解
④已知:AlCl3是共价化合物。传统工艺不能用电解纯的熔融AlCl3来制取金属铝;也不能用电解熔融的MgCl2来制取金属镁
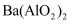 常温可溶于水.如图表示的是向
常温可溶于水.如图表示的是向 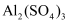 溶液中逐滴加入
溶液中逐滴加入 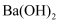 溶液时,生成沉淀的物质的量y与加入
溶液时,生成沉淀的物质的量y与加入 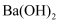 的物质的量x的关系.下列有关叙述正确的是( )
的物质的量x的关系.下列有关叙述正确的是( ) 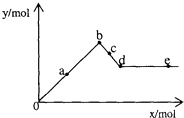
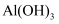 比
比 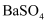 多
B . d-e时溶液中离子的物质的量:
多
B . d-e时溶液中离子的物质的量:  可能等于
可能等于  C . a-d时沉淀的物质的量:
C . a-d时沉淀的物质的量: 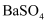 可能小于
可能小于 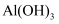 D . c-d时溶液中离子的物质的量:
D . c-d时溶液中离子的物质的量:  比
比  少
少
①向饱和碳酸钠溶液中通入过量的CO2 ②向NaAlO2溶液中逐滴加入过量的稀盐酸 ③向AlCl3溶液中逐滴加入过量稀氢氧化钠溶液 ④向硅酸钠溶液中逐滴加入过量的盐酸
| 化学性质 | 实际应用 | |
| A | 次氯酸具有氧化性 | 漂白粉漂白织物 |
| B | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
| C | 硅透光性好,且折射率合适,能够发生全反射 | 硅可作光导纤维 |
| D | 明矾溶于水可生成Al(OH)3胶体 | 可用于自来水消毒 |
| 实验 | 现象 | 结论 | |
| A | 室温下测0.1 mol·L-1醋酸pH | pH≈3.3 | 醋酸是弱酸 |
| B | 向2 mL 0.1 mol·L-1NaOH溶液中 i.滴加几滴同浓度的MgSO4溶液 ii.再滴加几滴同浓度FeCl3溶液 | i.产生白色沉淀 ii.产生红褐色沉淀 | 溶解度:Fe(OH)3<Mg(OH)2 |
| C | 常温下,将CO2通入苯酚钠溶液中 | 溶液变浑浊 | 酸性:碳酸>苯酚 |
| D | 将少量溴乙烷与NaOH溶液共热,冷却、HNO3酸化后,滴加AgNO3溶液 | 淡黄色沉淀 | 证明含有溴元素 |
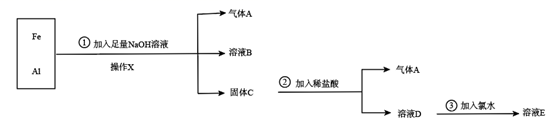
-
(1) 操作X的名称是。
-
(2) ①加入足量
 溶液时发生反应的化学方程式为。
溶液时发生反应的化学方程式为。
-
(3) 检验溶液E中阳离子所需试剂为,现象为。
-
(4) 写出③加入氯水的离子方程式。
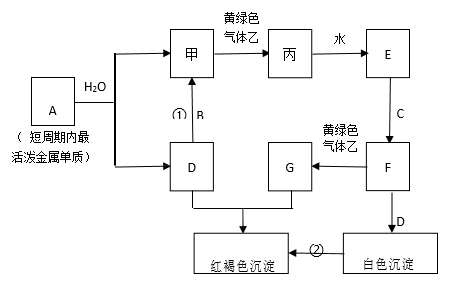
请根据以上信息回答下列问题:
-
(1) 写出下列物质的化学式:乙、丙。
-
(2) 写出下列反应的离子反应方程式:反应①反应②。
-
(3) 金属B的氧化物既能和强酸反应又能和强碱反应,试写出B的氧化物与强碱反应的离子方程式。
-
(1) Ⅰ 化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等都离不开化学。请根据题意回答以下问题:
海底埋藏着大量可燃烧的“冰”,“可燃冰”外观像冰,主要成分为甲烷水合物,并含有少量CO2等。可燃冰属于(填“纯净物”或“混合物”);在较低的温度和压力下,用甲烷为原料可制成金刚石薄膜,该变化属于(填“物理变化”或“化学变化”)。
-
(2) 铝制品表面因有一层氧化铝薄膜而经久耐用,若用铝制容器长期盛装含强碱性的食物该容器表面会发生破损,相关反应的离子方程式为。
-
(3) 粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,除去这些杂质的试剂可选用①Na2CO3、②NaOH、③BaCl2、④HCl,用序号表示加入的先后顺序是。
-
(4) II 新型纳米材料氧缺位铁酸盐(MFe2Ox , 3<x<4,M=Mn、Zn、Ni,且均为+2价,下同)是由铁酸盐MFe2O4经过高温反应得到的。
ZnFe2O4中Fe元素的化合价为。
-
(5) 含氧铁盐K2FeO4的重要应用之一是生成Fe(OH)3胶体吸附净水。实验室可用饱和FeCl3溶液模拟该胶体的制备,请写出化学反应方程式。
-
(6) 在酸性条件下,某反应体系中共存在下列6种粒子:
 、Fe2+、H+、H2O、Cu2O、Cu2+ , 请完成该反应的离子方程式并用双线桥表示电子的转移。
、Fe2+、H+、H2O、Cu2O、Cu2+ , 请完成该反应的离子方程式并用双线桥表示电子的转移。
①重晶石
②
③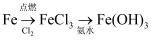
④
- His test results are not very consistent (一致的). He does well
- 直到康乾盛世,中国的小农经济历经千年发展到了辉煌的顶峰,中国的GDP在晚清甚至达到了当时世界的三分之一,然而著名历史学家
- 在高能物理研究中,粒子回旋加速器起着重要作用,如图甲为它的示意图。它由两个铝制D型金属扁盒组成,两个D形盒正中间开有一条
- 下列各句中,加点词语使用正确的一句是( )A.阳春三月,一位老人在杭州西湖岸边展示他高超的拳脚功夫,引来许多行人侧目观赏
- 下列关于动、植物结构层次的叙述正确的是( ) A.动、植物的结构层次均为:细胞 组织 器官 系统生物体
- 敲 雪 ①睡到半夜,忽然觉得好冷。也许,外面下雪了。我想。我
- 下列词语中加点的字,读音有错误的一组是A.炽情(chì) 霎时(chà) 纤维(xiān) 锃光瓦亮(zèng)
- NEMS NEWRIEnvironmental Master of ScienceNEWRI: NanyangEnvir
- 下列消费行为中属于适度消费的是
- 找出没有语病的一项 ( )A.我国目前的测控通信网,是我国航天史上规模最庞大、技术最先进、可靠性更高的系统。B.北京时间
- 阅读下面的文章,完成下面试题。 牛的写意 李汉荣 ①
- 读某日某时海平面天气图(下图,单位:百帕),回答下图中,此时可能出现降水天气的地区是A.山东半岛 B.长江三角洲
- To test eggs, them in a bowel of water; if they float t
- 右图甲是大肠杆菌在复合培养基中的生长曲线,复合培养基中含有葡萄糖和乳糖,图乙表示大肠杆菌内产生G物质的代谢过程。以下说法
- 4.如图是某些物质跨膜运输的图解,下列分析与实际不相符的是()A.图中跨膜运输情况反映了细胞膜的功能特性 B.细胞之所以
- I hear they’ve promoted Tom, but he didn’t mention ________
- —What do you think of store shopping in the future?( ) —Per
- 阅读下面的文段,回答问题。(9分) ①总有这样一些人让我们感动。党的好干部牛玉儒以勤政为民、忘我工作诠释“生命一分钟,敬
- 1871年颁布的《德意志帝国宪法》规定:“皇帝在国际关系上为帝国代表,以帝国的名义宣战或媾和,同外国缔结同盟及其他条约,
- 氧化锌和锌的混合物14.6 g,加入浓度为1 mol/L的盐酸500 mL,充分反应后,所得溶液中Zn2+的物质的量浓度



