钠的重要化合物 知识点题库
在含有Fe2+、Fe3+、Al3+、NH4+的溶液中加入足量的Na2O2固体,再加入过量的稀HCl,完全反应后,离子数目几乎没有改变的是( )
A . Fe2+
B . Fe3+
C . Al3+
D . NH4+
16.8gNaHCO3和7.8gNa2O2在密闭容器中灼烧,充分反应后,将密闭容器保持温度为500℃,最后容器内物质是
A . Na2CO3 , Na2O,O2
B . Na2CO3 , CO2 , O2 , H2O(g)
C . Na2CO3 , O2 , H2O(g)
D . NaHCO3 , Na2CO3 , O2
Na2O2、HCl和Al2O3在水中反应,若最后所得溶液中只含AlO2-、Na+、Cl- , 则Na2O2、HCl和Al2O3的物质的量之可能为( )
A . 4∶6∶1
B . 8∶6∶1
C . 3∶3∶1
D . 4∶6∶3
下列物质性质与应用对应关系正确的是( )
A . 过氧化钠可以与CO2反应放出O2 , 可用于潜艇中的供氧剂
B . 硅酸钠溶液呈碱性,可涂在木材的表面作耐火剂
C . SO2具有氧化性,可用于纸浆的漂白
D . 明矾溶于水可形成有氢氧化铝胶体,可用于自来水的杀菌消毒
将某些化学知识用数轴表示,可以收到直观、简明、易记的效果.用数轴表示的下列知识正确的是( )
A . 硫及其化合物的化合价与氧化还原反应的关系: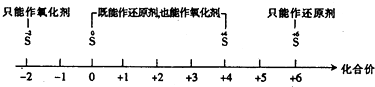 B . 分散系的分类:
B . 分散系的分类: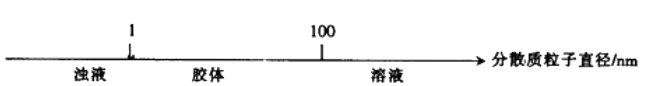 C . AlCl3溶液与NaOH溶液反应后铝元素的存在形式:
C . AlCl3溶液与NaOH溶液反应后铝元素的存在形式: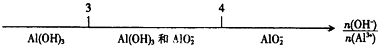 D . CO2与NaOH溶液反应后的产物
D . CO2与NaOH溶液反应后的产物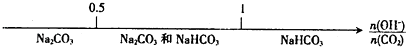
 B . 分散系的分类:
B . 分散系的分类: C . AlCl3溶液与NaOH溶液反应后铝元素的存在形式:
C . AlCl3溶液与NaOH溶液反应后铝元素的存在形式: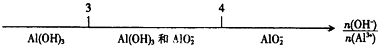 D . CO2与NaOH溶液反应后的产物
D . CO2与NaOH溶液反应后的产物
把一瓶不饱和的烧碱溶液分成4等份.保持温度不变,向4份溶液中分别加入一定量的NaOH固体、Na2O2、Na2O和Na,使溶液均恰好饱和,下列说法中正确的是( )
A . 加入的NaOH质量不一定最大
B . 加入的Na2O2和Na2O的物质的量之比为1:1
C . 制成饱和溶液后,4份溶液中所含NaOH质量相同
D . 加入的NaOH,Na2O2 , Na2O、Na的物质的量之比为2:1:1:2
下列物质不是黄色或淡黄色的是( )
A . 单质硫
B . 过氧化钠
C . 氢氧化铁胶体
D . 三氯化铁稀溶液
下列说法正确的是( )
A . 淀粉与稀H2SO4共热,再加银氨溶液水浴加热,无银镜生成,说明淀粉水解产物无还原性
B . SiO2+2C  Si+2CO 说明碳的非金属性大于硅的非金属性
C . 向NaAlO2溶液中滴加饱和NaHCO3溶液,有白色沉淀产生,是因为两者都发生了水解反应,且相互促进
D . 将CO2通入Na2SiO3溶液中,有白色沉淀生成,证明H2CO3酸性比H2SiO3强
Si+2CO 说明碳的非金属性大于硅的非金属性
C . 向NaAlO2溶液中滴加饱和NaHCO3溶液,有白色沉淀产生,是因为两者都发生了水解反应,且相互促进
D . 将CO2通入Na2SiO3溶液中,有白色沉淀生成,证明H2CO3酸性比H2SiO3强
 Si+2CO 说明碳的非金属性大于硅的非金属性
C . 向NaAlO2溶液中滴加饱和NaHCO3溶液,有白色沉淀产生,是因为两者都发生了水解反应,且相互促进
D . 将CO2通入Na2SiO3溶液中,有白色沉淀生成,证明H2CO3酸性比H2SiO3强
Si+2CO 说明碳的非金属性大于硅的非金属性
C . 向NaAlO2溶液中滴加饱和NaHCO3溶液,有白色沉淀产生,是因为两者都发生了水解反应,且相互促进
D . 将CO2通入Na2SiO3溶液中,有白色沉淀生成,证明H2CO3酸性比H2SiO3强
根据要求填空:
-
(1) 实验室用钠和硫酸铜溶液反应,有关反应的化学方程式有:,;
-
(2) 表面附有氧化膜(成分是MgO)的镁条放入稀硫酸中,开始反应时的离子方程式是:;
反应片刻后,可观察到有气体产生,其离子方程式是:.
-
(3) 用小苏打片(NaHCO3)治疗胃酸(0.2%~0.4%的盐酸)过多的化学方程式为:.
-
(4) 看图回答下列问题:
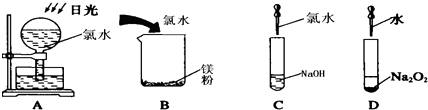
图中不会产生气体的是(填编号),写出D中发生反应的化学方程式:.
下面是比较过氧化钠和氧化钠性质异同的有关叙述,其中错误的是( )
A . 过氧化钠和氧化钠长期置于空气中最终产物相同
B . 过氧化钠和氧化钠都能与二氧化碳或水发生化合反应
C . 过氧化钠和氧化钠与水反应都有氢氧化钠生成
D . 过氧化钠是强氧化剂,而氧化钠是一种碱性氧化物
下列物质露置在空气中,质量会减轻的是( )
A . NaOH
B . Na 2O2
C . 无水CaCl2
D . Na2CO3·10H2O
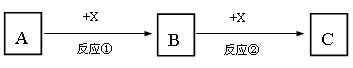
A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(反应条件及副产物已略去)。
-
(1) 若A、B、C均为含有同种非金属元素的化合物,A为使湿润的红色石蕊试纸变蓝的气体,B接触空气立刻变为C,则反应①的化学方程式为。
-
(2) 若A、B、C为焰色反应均呈黄色的化合物,X为无色无味气体,则反应②的离子方程式为。
-
(3) 若A、B、C均为含有同种金属元素的化合物,X是强碱,则反应②的离子方程式为。
-
(4) 若A为单质Fe,X为稀硝酸,若向B的溶液中加入氢氧化钠溶液,现象为。
-
(5) 若A和X均为单质,B为可使品红溶液褪色的气体,则反应②的化学方程式为。
将质量为W1 g的钠、铝混合物投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V1L.向溶液中逐滴加入浓度为a mol·L−1的HCl溶液,过程中有白色沉淀产生后又逐渐溶解,当沉淀恰好消失时所加HCl溶液体积为V2L。将溶液蒸干充分灼烧得到固体(NaCl和Al2O3)W2 g.下列关系式中错误的是( )
A . 24n(Al)+35.5n(Na)=W2−W1
B . n(Na)+3n(Al)=aV2
C . n(Na)+3n(Al)=V1/11.2
D . aV2=V1/22.4
化学知识可以帮助解决日常生活中遇到的许多问题,下列说法错误的是( )
A . 胃酸过多的病人,可以服用碳酸氢钠来中和胃酸
B . 明矾有吸附性,可用于自来水的杀菌消毒
C . 溴化银见光易分解,是一种重要的感光材料,是胶卷中必不可少的成分
D . Na2O2吸收CO2产生O2 ,可用作呼吸面具供氧剂
氧化铬绿(Cr2O3)的性质独特,在冶金、颜料等领域有着不可替代的地位。一种利用淀粉水热还原铬酸钠制备氧化铬绿的工艺流程如下:
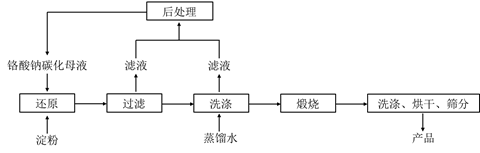
已知:①向含少量Na2CO3的铬酸钠碱性溶液中通入CO2可制得不同碳化率的铬酸钠碳化母液;
②“还原”反应剧烈放热,可制得Cr(OH)3浆料。
-
(1) 该工艺中“还原”反应最初使用的是蔗糖或甲醛,后来改用价格低廉的淀粉。请写出甲醛(HCHO)与铬酸钠(Na2CrO4)溶液反应的离子方程式。
-
(2) 将混合均匀的料液加入反应釜,密闭搅拌,恒温发生“还原”反应,下列有关说法不正确的是(填标号)。
A 该反应一定无需加热即可进行 B 必要时可使用冷却水进行温度控制
C 铬酸钠可适当过量,使淀粉充分反应 D 应建造废水回收池,回收含铬废水
-
(3) 测得反应完成后在不同恒温温度、不同碳化率下Cr(Ⅵ)还原率如下图。实际生产过程中Cr(Ⅵ)还原率可高达99.5%以上,“还原”阶段采用的最佳反应条件为。
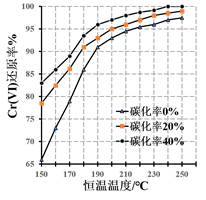
-
(4) 滤液中所含溶质为。该水热法制备氧化铬绿工艺的优点有、(请写出两条)。
-
(5) 由水热法制备的氢氧化铬为无定型氢氧化铬[Cr(OH)3·nH2O]。将洗涤并干燥后的氢氧化铬滤饼充分煅烧,质量损失与固体残留质量比为9:19,经计算得出n=。
-
(6) 重铬酸钠(Na2Cr2O7·H2O)与硫酸铵热分解法也是一种生产氧化铬绿的方法,生产过程中产生的气体对环境无害,其化学反应方程式为。
下列叙述正确的是( )
A . Na2O与Na2O2中阴、阳离子的个数比均为1:2
B . 足量Cl2、O2分别和两份等质量的Na反应,前者得到电子多
C . 胃酸过多可用服用碳酸钠
D . 钠投入水中会熔成小球,并四处游动,说明钠与水反应放热并生成氧气
下列有关图像的说法正确的是( )
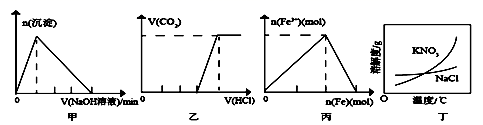
A . 图甲表示:向某明矾溶液中逐滴加入NaOH溶液至过量,生成沉淀的物质的量与滴加NaOH溶液体积的关系
B . 图乙表示:向含等物质的量的NaOH和Na2CO3的混合溶液中逐滴加入稀盐酸至过量,生成气体的体积与滴加HCl溶液体积的关系
C . 图丙表示:在稀硝酸溶液中逐渐加入铁粉至过量,溶液中Fe3+物质的量与逐渐加入铁粉物质的量的变化关系
D . 除去混在硝酸钾中少量的氯化钠可用“蒸发浓缩、趁热过滤”的方法
下列说法中不正确的是( )
①用小苏打可用于治疗胃酸过多 ②SO2的水溶液能导电,所以SO2是电解质 ③液态HCl不导电,所以HCl是非电解质 ④硫酸氢钠电离出的阳离子有氢离子,所以硫酸氢钠是酸 ⑤制备Fe(OH)3胶体,通常是将饱和氯化铁溶液与氢氧化钠溶液混合加热 ⑥某溶液中加入盐酸产生使澄清石灰水变浑浊的气体,则一定含有CO32-
A . ①③④⑤⑥
B . ②③④⑤⑥
C . ①②④⑥
D . ①②③④
A~H为中学化学中常见物质,其转化关系如图所示,其中“O”代表化合物,“口”代表单质,A为医学上治疗胃酸过多的一种药剂,G为淡黄色固体,C在通常状况下为无色液体,F为金属单质。请回答下列问题:
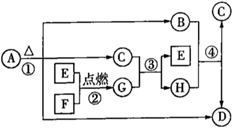
-
(1) G的化学式为,G中阴、阳离子个数比为,每生成1 mol G转移电子的物质的量为。
-
(2) A、D的水溶液均呈(填“酸性”“碱性”或“中性”)。反应①②③④中属于氧化还原反应的有个。A~H中焰色呈黄色的物质有种。
-
(3) 写出下列反应的化学方程式。
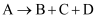 :,
:, 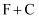 :。
:。
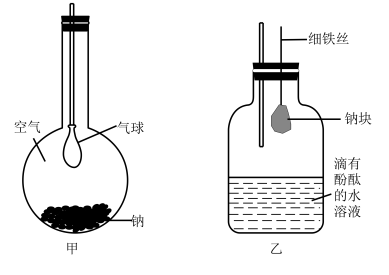
根据所学知识回答下列问题:
-
(1) 将一小块新切的金属钠迅速放入平底烧瓶底部按图甲所示塞紧瓶塞。一段时间后可观察到的现象有,发生反应的化学方程式为。
-
(2) 按图乙所示的装置,进行钠与水反应的实验,实验开始时,振动细铁丝使钠块掉入滴有酚酞的水溶液中,可观察到钠与水反应的现象,不同的现象反映钠的不同性质。
①能证明钠的密度比水的小的现象是。
②能证明钠的熔点低的现象是。
③能证明有氢氧化钠生成的现象是。
-
(3) 少量
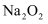 与
与 溶液可发生反应,其化学方程式为
溶液可发生反应,其化学方程式为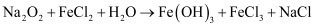 (未配平)。已知
(未配平)。已知 的化学计量数为6配平上述化学方程式,并用单线桥法标出电子转移的方向和数目:。该反应中被还原的元素是(填元素符号),氧化产物是(填化学式)。
的化学计量数为6配平上述化学方程式,并用单线桥法标出电子转移的方向和数目:。该反应中被还原的元素是(填元素符号),氧化产物是(填化学式)。
-
(4) 向
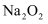 中滴加浓盐酸试管壁发热,有刺激性气味的气体产生,反应后所得溶液呈浅黄绿色。推测产生该气体的反应的化学方程式为。
中滴加浓盐酸试管壁发热,有刺激性气味的气体产生,反应后所得溶液呈浅黄绿色。推测产生该气体的反应的化学方程式为。
最近更新
- 某同学利用图甲所示的实验装置,探究物块在水平桌面上的运动规律。物块在重物的牵引下开始运动,重物落地后,物块再运动一段距离
- 中国古代吏治腐败时会出现以钱买官的现象。“三千索,直秘阁,五百贯,擢通判”,就是对这一现象的揭露。这句话所反映的情况发生
- 对下列语句中运用的修辞方法及其表达作用的解释,不正确的一项是 ()A.那些文字拙劣的、词不达意的、欠通的语句密密麻麻的,
- 已知某饱和溶液的以下条件:①溶液的质量;②溶剂的质量;③溶液的体积;④溶质的摩尔质量;⑤溶质的溶解度;⑥溶液的密度。其中
- 下列过程遵循“碱基互补配对原则”的有()①DNA复制 ②mRNA与核糖体结合 ③转录 ④翻译 ⑤RNA复制
- 阅读下面这篇文章,完成9-12题。 2016文化热点看什么 这是一个巨变的时代,一个繁荣的时代,一个活力大爆发的时
- 一块铁块放到火炉中加热一段时间后,会变大的物理量是( ) A.内能 B.质量 C.比热
- X、Y、Z三种气体进行反应3X+Y2Z,在三种不同情况下测得反应速率为①v(X)=1 mol·L-1·min-1 ②v
- 阅读下面的文字,完成后面题目。(23分) 你在大雾里得意忘形(节选) 铁 凝 1.那时在冀中乡村,我常在清晨无边的大地上
- 学习金属单元后,我们知道Zn、Fe、Cu三种金属的活动性顺序为:Zn>Fe>Cu.为验证这一结论,下面实验设计合理的是(
- 高氯酸铵(NH4ClO4)是复合火箭推进剂的重要成分,实验室可通过下列反应制取: NaClO4(aq)+NH4Cl(aq
- 如图所示是火警报警装置的一部分电路示意图,其中R2是半导体热敏传感器,它的阻值随温度升高而减小,a、b接报警器,则()A
- 下列活动中所得到数值与实际数值相比,可能偏小的是() A. 标志重捕法调查池塘中鲤鱼的种群密度时,部分鲤鱼
- 下列句子中横线处填入的词语,最准确的一组是 () 有时,一个美丽的谎言______
- I bought a dress for only 10 dollars in a sale; it was a rea
- 最新科技报导,美国夏威夷联合天文中心的科学家发现了新型氢微粒,这种新粒子是由3个氢原子核(只含质子)和2个电子构成,对于
- 关于物体的质量,下面说法正确的是 ( )A.同一块铁
- 据某地气象部门统计,该地区每年最低气温在-2 ℃以下的概率为,设ξ为该地区从2005年到2010年最低气温在-2 ℃以下
- You use the word “________” when you are describingsomething
- 我国某中学地理兴趣小组开展“当地经纬度测算课题研究”活动,其操作方法是:在一年中白昼最短的这一天,选择操场上Q处垂直竖立



