氨的性质及用途 知识点题库
(1)有颜色的气体是 ;
(2)水溶液呈碱性的气体是 ;
(3)能与水反应,且在反应中既做氧化剂又做还原剂的气体是
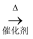 4NO+6H2O
B . 液氨可以作为溶剂使用,而氢的沸点极低,不易液化
C . 氨气比空气轻,标准状况下密度约为0.76 g•L﹣1
D . 氨气与氢气相比,优点在于氨气不容易发生爆炸,使用时更安全
4NO+6H2O
B . 液氨可以作为溶剂使用,而氢的沸点极低,不易液化
C . 氨气比空气轻,标准状况下密度约为0.76 g•L﹣1
D . 氨气与氢气相比,优点在于氨气不容易发生爆炸,使用时更安全
A | B | C | D | |
纸蝴蝶上的喷洒液 | 石蕊 | 石蕊 | 酚酞 | 石蕊 |
小烧杯中的溶液 | 浓盐酸 | 浓氨水 | NaOH溶液 | 浓硫酸 |
-
(1) 氮气的结构式为,氮的氢化物除了氨气,还有一种在常温下呈液态的肼,分子式为N2H4 , 请写出肼的电子式;
-
(2) NH3与NaClO反应可得到肼,该反应的化学方程式为;
-
(3) 肼在碱性环境下可以形成肼一空气燃料电池,肼被氧化为N2 , 该电池负极的反应式为,每生成56g N2要消耗标准状况下的氧气的体积为 L.
![]() .
.
-
(1) I.氨是一种重要的工业原料。回答下列问题:
催化剂存在下,NH3可用来消除NO的污染,生成两种对环境无害的物质。写出反应的化学方程式;该反应中氧化产物与还原产物的物质的量之比为。
-
(2) 当运输氨气的管道发生泄漏时,可用一种挥发性液体(写试剂名称) 进行检查,出现的现象是。
-
(3) II.联氨(N2H4)具有较强的还原性。工业上用过量氨气和NaClO溶液来制备。
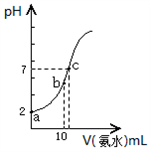
制取NaClO所用的原料是、。解释氨气过量的原因。常温下,向10mL pH=2的盐酸中滴加等浓度氨水。加入氨水的体积(V)与溶液pH的关系如图所示。
-
(4) a点溶液中由水电离产生的c(H+)10-7mol/L (填>、<或=);用平衡移动原理解释b点溶液呈酸性的原因。
-
(5) 比较c点溶液中所有离子浓度大小关系是。
| A | B | C | D | |
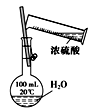
| 实验 | 配制一定物质的量浓度的硫酸溶液 | 打开止水夹,挤压胶头滴管能够引发喷泉 | 制取并收集NO2气体 | 除去CO2气体中的HCl气体 |
| 装置 或 仪器 | | | | |
 B .
B . 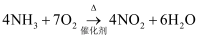 C . 2NH3+3Cl2→N2+6HCl
D . 8NH3+3Cl2→N2+6NH4Cl
C . 2NH3+3Cl2→N2+6HCl
D . 8NH3+3Cl2→N2+6NH4Cl
-
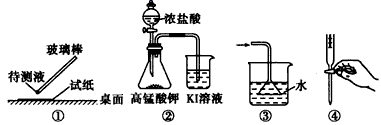
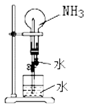
(1) Ⅰ.氨气的制备
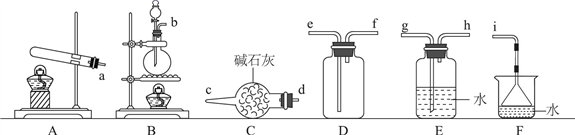
氨气的发生装置可以选择上图中的(填大写字母),反应的化学方程式为。
-
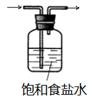
(2) 欲收集一瓶干燥的氨气,选择上图中的装置,按气流方向写出其接口的连接顺序:发生装置管口→(填小写字母)。
-
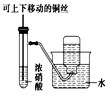
(3) Ⅱ.氯气与氨气的反应
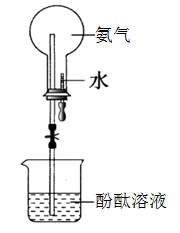
室温下,用收集到的氨气按下图所示装置进行实验(实验前k1、k2关闭)。
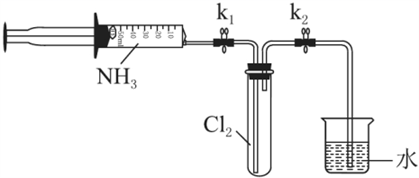
打开k1 , 缓缓推动注射器活塞,向试管中注入约3倍于氯气体积的氨气,关闭k1 , 恢复室温。试管中可观察到的现象是。发生反应的化学方程式为。
-
(4) 再打开k2 , 可观察到的现象是。
 NaCl +N2↑+2H2O
B . 装置II的作用是冷凝水蒸气
C . 装置II末端收集纯净干燥的N2只能用向下排空气法
D . 加热片刻后需要将酒精灯移开,说明该反应是放热反应
NaCl +N2↑+2H2O
B . 装置II的作用是冷凝水蒸气
C . 装置II末端收集纯净干燥的N2只能用向下排空气法
D . 加热片刻后需要将酒精灯移开,说明该反应是放热反应
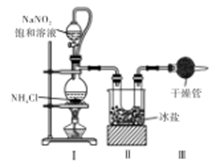
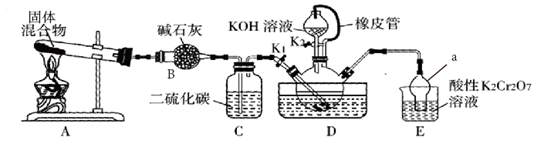
已知:①NH3不溶于CS2 , CS2密度比水大且难溶于水;
②三颈烧瓶内盛放CS2、水和催化剂,发生反应:CS2+3NH3 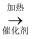 NH4SCN+NH4HS,该反应比较缓慢,且NH4SCN在高于170℃易分解。
NH4SCN+NH4HS,该反应比较缓慢,且NH4SCN在高于170℃易分解。
-
(1) 仪器a的名称。
-
(2) C装置的作用是:观察气泡的流速,便于调控生成氨气的速率;三颈烧瓶内的导气管插人下层CS2液体中,原因是。
-
(3) 待实验中观察到现象时,熄灭A处酒精灯,待D中无气泡产生时关闭K1.保持三颈烧瓶内液温105℃一段时间,使NH4HS=NH3↑+H2S↑进行完全后,打开K2 , 继续保持液温105℃,滴入适量的KOH溶液,写出生成KSCN的化学方程式。
-
(4) 装置E的作用为吸收尾气,防止污染环境,写出吸收NH3的离子方程式。(提示:
 →Cr3+)
→Cr3+)
-
(5) 反应结束后将三颈烧瓶中的固体催化剂滤去,再蒸发浓缩、、过滤、洗涤、干燥,得到硫氰化钾晶体。
-
(6) 晶体中KSCN含量的测定:称取10.0g样品,配成1000mL溶液。量取20.00mL溶液于锥形瓶中,加入适量稀硝酸,再加人几滴Fe(NO3)3作指示剂,用0.1000mol·L-1AgNO3标准溶液滴定,达到滴定终点时消耗AgNO3标准溶液18.00mL。(已知:滴定时发生的反应为SCN-+Ag+=AgSCN↓(白色)晶体中KSCN的质量分数为。(只要求写出计算结果)
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验氯水中是否含有 | 用玻璃棒蘸取溶液点在 | 若试纸变红后不褪色,则说明溶液中含有 |
| B | 浓氨水是否具有挥发性 | 烧杯中放两个棉花球,分别滴加几滴浓氨水和浓硫酸,用表面皿盖住 | 若烧杯中充满大量白烟,则说明浓氨水具有挥发性 |
| C | 验证乙醇发生消去反应后的产物 | 乙醇与浓硫酸混合加热到170℃,将产生的气体通入酸性高锰酸钾溶液中 | 若溶液紫红色褪去,则说明产生的气体中一定含有乙烯 |
| D | 探究浓度对化学平衡的影响 | 在 | 若溶液由橙色变为黄色,则说明降低 |
-
(1) 氨气是氮的最简单氢化物,电子式,其水溶液呈(填“酸性”、“中性”或“碱性”),原因是。氨的催化氧化是工业制硝酸的基础,该反应的化学方程式是。
-
(2) 联氨(又称肼,N2H4 , 无色液体)分子中极性键与非极性键的个数比为,其中氮的化合价为。实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为。
-
(3) 叠氮酸(HN3)酸性略大于醋酸,叠氮酸的电离方程式为,联氨被亚硝酸氧化可以生成叠氮酸,反应的化学方程式为。
 具有还原性,可用作制冷剂
B . 浓硫酸具有脱水性,可用于气体的干燥
C . 二氧化硫具有氧化性,可用于纸浆的漂白
D .
具有还原性,可用作制冷剂
B . 浓硫酸具有脱水性,可用于气体的干燥
C . 二氧化硫具有氧化性,可用于纸浆的漂白
D .  溶液能与
溶液能与 反应,可用作铜制线路板的蚀刻剂
反应,可用作铜制线路板的蚀刻剂
- 有学者说,因辛亥革命,中国人的脑袋与双膝不再为磕头而准备着,而是为思考问题、为走路而准备着。这里强调的是辛亥革命A.提供
- (1)已知反应A+3B2C+D,在30 s内A的浓度减小了0.5 mol·L-1,则此段时间内以B的浓度变化表示的反应
- 传说中炎帝、黄帝部落联盟经过长期的发展,形成日后的( )A中华民族 B华夏族
- 使第二次世界大战的规模进一步扩大,世界上的主要国家和绝大部分地区都被卷入战争漩涡的事件是 A. 英法对德宣战
- 下列估测值接近实际的是 A. 中学生的质量约为45kg B.人步行的速度约为5m/s C. 课桌的高度约为2m
- 人民法院和人民检察院是我国的 A.国家权力机关 B.审判机关 C.司法机关 D.法律监督机关
- 7.“此时中枢部门的分立,主要由其处理的政务范围不同所决定,而不取决于或出令、审覆、执行的程度环节分工。……基本上按照所
- 读长江中下游与青海、西藏地区土地生产潜力和最大人口密度表,回答21~22题。 年生物量/ 万吨 可承载 人口/万 最大人
- 如图所示的现象中,由光折射形成的是
- a、b是一条水平绳上相距为l的两点.一列简谐横波沿绳传播,其波长等于l.当a点经过平衡位置向上运动时,b点A.经过平衡位
- 在下列物质中,不属于人体内环境组成成分的是() A.血红蛋白 B. 血
- .(12分)阅读下列材料,回答问题。 历代都城布局图包含了政治、经济、文化等多种信息。 比较图一、图二,提取两项有关我国
- Whenwe saw his face, we knew ________ was bad. A. some n
- The firm was successfully run and ________,he owed his succe
- 以下关于氨碱法与联合制碱法的认识,不正确的是() A.氨碱法生产纯碱的原料便宜易得,步骤简单,是最早的制碱工艺 B.联合
- 2009年12月1日晚,欧盟举行仪式庆祝_______生效。该条约将使欧盟在国际舞台上 成为一个真正的实体。 A.
- 生活中每个人可能都有过被误解的经历,当你百口莫辩的时候,是不是特别的沮丧?当误解消除的那刻,心情是不是顿时雨过天晴?拿起
- 下列说法均摘自某科普杂志,你认为无科学性错误的是( )A.铅笔芯的原料是重金属铅,儿童在使用时不可用嘴吮咬铅笔,以
- 被誉为中国“新四大发明”之一的复方蒿甲醚(C16H26O5)是治疗疟疾的有效药品。下列关于复方蒿甲醚的说法错误的是 A.
- ―Karen, can I talk to you for a minute? ―Sure, ________? A.h

 试纸上
试纸上 溶液中滴加数滴
溶液中滴加数滴  溶液
溶液 与水反应的平衡正向移动
与水反应的平衡正向移动


