卤素原子结构及其性质的比较 知识点题库
根据元素周期表和元素周期律,下列推断中错误的是
A . 砹是一种有色固体,它的气态氢化物很不稳定,
B . F2与水反应比Cl2与水反应剧烈
C . 铷的硫酸盐易溶解于水,其氢氧化物一定是强碱
D . 溴化氢比氯化氢稳定,HClO4酸性强于HBrO4
随着卤素(F、Cl、Br、I)原子半径的增大,下列递变规律正确的是( )
A . 单质熔、沸点逐渐降低
B . 气态氢化物稳定性逐渐增强
C . 卤素离子的还原性逐渐增强
D . 单质的氧化性逐渐增强
在化学学习中常可根据已知的实验事实,对某些物质的化学性质作出推测,请判断下列推测合理的是( )
A . 从红热的铜丝能在氯气中燃烧,推测红热的铁丝也能在氯气中燃烧
B . 从碘单质使淀粉试液变蓝,推测 I﹣也能使淀粉试液变蓝
C . 从Fe能从CuSO4溶液中置换出Cu,推测Na也能从CuSO4溶液中置换出Cu
D . 从二氧化碳通入Ca(OH)2溶液能产生白色沉淀的事实,推测二氧化碳通入CaCl2溶液也能产生白色沉淀
卤素单质从F2到I2在常温常压下的聚集状态由气态、液态到固态的原因是( )
A . 原子间的化学键键能逐渐减小
B . 范德华力逐渐增大
C . 原子半径逐渐增大
D . 氧化性逐渐减弱
按照氟、氯、溴、碘的顺序,下列递变规律中正确的是( )
A . 单质的熔、沸点逐渐降低
B . 与H2反应越来越容易
C . F﹣、Cl﹣、Br﹣、I﹣的还原性逐渐增强
D . 单质的氧化性逐渐增强
下列关于卤素(用X表示)的叙述正确的是( )
A . 其单质都能与水反应,通式为X2+H2O═HX+HXO
B . HX易溶于水,其水溶液都是强酸
C . 其单质都有颜色,都有毒
D . 最高价含氧酸的通式为HXO4
下列关于卤素的叙述不正确的是( )
A . 随核电荷数递增,卤素单质熔沸点升高
B . 随核电荷数递增,卤化氢的稳定性增强
C . 随核电荷数递增,卤素离子的还原性增强
D . 随核电荷数递增,卤素原子半径增大
下列说法正确的是( )
A . 卤素元素都有正化合价
B . 卤素元素的单质都只具有氧化性
C . 卤素元素的最低化合价都是﹣1价
D . 卤素元素氢化物都是强酸
随着卤素原子半径的增大,下列递变规律正确的是( )
A . 单质的熔沸点逐渐降低
B . 单质的氧化性逐渐增强
C . 相同条件下,单质的密度逐渐变小
D . 单质的颜色逐渐加深
下列关于F、Cl、Br、I性质的比较,不正确的是( )
A . 单质的颜色随核电荷数的增加而加深
B . 它们的氢化物的稳定性随核电荷数的增加而增强
C . 它们的原子核外电子层数随核电荷数的增加而增多
D . 被其他卤素单质从其卤化物中置换出来的可能性随核电荷数的增加而增大
卤族元素包括元素,它们原子的最外层都有个电子,在化学反应中易得到个电子,因此均体现出较强的氧化性;但从F到I,电子层数依次增多,原子半径逐渐,原子核对最外层电子的引力逐渐,所以非金属性逐渐,单质的氧化性逐渐。
卤族元素随着原子序数的增大,下列递变规律正确的是( )
A . 原子半径逐渐增大
B . 单质的氧化性逐渐增强
C . 单质熔、沸点逐渐降低
D . 气态氢化物稳定性逐渐增强
下列所示的实验方案正确,且能达到实验目的的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 比较镁、铝的金属性强弱 | 分别在MgCl2和AlCl3溶液中滴加氨水直至过量,观察现象 |
| B | 比较Cl2、Br2的氧化性强弱 | 将少量氯水滴入FeBr2溶液中,观察现象 |
| C | 证明SO2具有漂白性 | 将SO2通入酸性高锰酸钾溶液中,溶液褪色 |
| D | 证明电离常数Ka:HSO3->HCO3- | 测得同浓度的Na2CO3溶液的pH大于Na2SO3溶液 |
A . A
B . B
C . C
D . D
下列叙述正确的是( )
A . 关于碱金属单质,它们都是电和热的良导体,均为银白色
B . H2、D2、T2互为同位素
C . 碱金属单质都可以保存在煤油中,碱金属单质在空气中加热均可生成多种氧化物
D . F2 、Cl2、Br2 、I2单质的颜色随核电荷数的增加而加深
氟是一种卤族元素,但它与其他卤素在单质和化合物的制备与性质上存在较明显的差异。
-
(1) 研究发现,
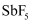 能将
能将  的盐转化为
的盐转化为 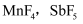 转化成稳定离子
转化成稳定离子  的盐。而
的盐。而  很不稳定,受热易分解为
很不稳定,受热易分解为 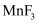 和
和  。根据以上研究写出以
。根据以上研究写出以  和
和 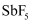 为原料,在
为原料,在 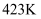 的温度下制备
的温度下制备  的化学方程式:。
的化学方程式:。
-
(2) 现代工业以电解熔融的氟氢化钾
 和氟化氢
和氟化氢 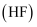 混合物制备氟单质,电解制氟装置如图所示。
混合物制备氟单质,电解制氟装置如图所示。 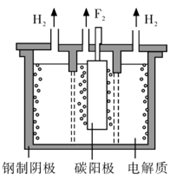
①已知
 是一种酸式盐,写出阴极_上发生的电极反应式:。
是一种酸式盐,写出阴极_上发生的电极反应式:。②电解制氟时,要用镍铜合金隔板将两种气体产物严格分开的原因是。
③已知
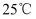 时,氢氟酸
时,氢氟酸 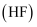 的电离平衡常数
的电离平衡常数 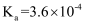 。某
。某 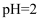 的氢氟酸溶液中,由水电离出的
的氢氟酸溶液中,由水电离出的 
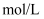 ;若将
;若将 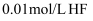 溶液与
溶液与 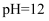 的
的  溶液等体积混合,则溶液中离子浓度大小关系为。
溶液等体积混合,则溶液中离子浓度大小关系为。 -
(3) 已知
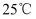 时,
时,  ,此温度下,若实验室中配制
,此温度下,若实验室中配制 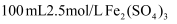 溶液,为使配制过程中不出现浑浊,则至少需要加
溶液,为使配制过程中不出现浑浊,则至少需要加 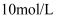 的硫酸
的硫酸 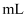 (忽略加入硫酸的体积)。
(忽略加入硫酸的体积)。
已知卤素互化物的性质与卤素单质类似,下列关于 BrCl 的说法错误的是( )
A . BrCl 有强氧化性
B . BrCl 能与水发生氧化还原反应
C . BrCl 是共价化合物
D . BrCl 能与 NaOH 溶液反应生成 NaBrO、NaCl 和 H2O
氯元素的化合价与其形成物质种类的关系如图所示。下列说法错误的是( )

A . e、d分别与b的浓溶液均可以反应生成c
B . d溶液久置酸性将增强
C . b只有还原性
D . f对应的酸性氧化物为Cl2O7
根据氯气及氯的化合物的相关知识,回答下列问题(用化学式或离子符号填写)
-
(1) 氯气与水反应得到的新制氯水含多种微粒。下列现象是由新制氯水中哪种微粒引起的。
①使氯水呈现黄绿色的是,②能使AgNO3溶液产生白色沉淀的是,③能使紫色石蕊试液显红色的是,④能使红色布条褪色的是。
-
(2) 反应8NH3+3Cl2=N2+6NH4Cl可用于氯气管道的检漏,在该反应中,氧化剂为,氧化产物为,氧化剂与还原剂的物质的量之比为。
-
(3) 氯气可以用于制备漂白粉,漂白粉中的有效成分为
-
(4) 在抗击新冠疫情中,"84"消毒液发挥了重要作用。但若将"84"消毒液(主要成分NaClO)与洗厕剂洁厕灵(主要成分盐酸)混合使用,则会产生氯气,其反应的离子方程式为。
鉴别NaCl、NaBr、NaI三种无色溶液可以采用的试剂是( )
A . 碘水、淀粉溶液
B . 碘化钾淀粉溶液
C . 溴水、苯
D . 氯水、CCl4
根据下列实验操作和现象,所得到的实验结论正确的是( )
选项 | 实验操作和现象 | 实验结论 |
A | 将浓硫酸滴到蔗糖表面,固体变黑膨胀 | 浓硫酸具有吸水性和强氧化性 |
B | 向NaI溶液中滴加少量氯水和CCl4 , 振荡、静置,下层溶液显紫色 | 还原性:I->Cl- |
C | 加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结 | NH4Cl固体可以升华 |
D | 向某溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色 | 该溶液中一定含有Fe2+ |
A . A
B . B
C . C
D . D
最近更新
- 下列运算正确的是() A. a3﹣a2=a B. (a2)3=a5 C. a4•a=a5
- 有关愈伤组织的说法错误的是( ) A. 愈伤组织进行异养生活,有氧呼吸 B. 愈伤组织细胞再诱导后才进行分化 C.
- 某工业混合液中含有的组分仅可能是乙醚(C4H10O)、乙醇(C2H6O)和水。经分析,液体中各原子数之比为N(C):N(
- 如图N27,要使输出值y大于100,则输入的最小正整数x是________.图N27
- 温家宝总理说,通货膨胀就像一只老虎,如果放出来就很难再关进去。导致恶性通货膨胀的经济原因一般是
- 在紫色洋葱的表皮细胞中含有RNA的结构有() ①细胞质基质 ②线粒体基质 ③叶绿体基质 ④核糖体 ⑤中心体 A.①②③⑤
- 目前,开发海洋资源,如采油、捕鱼、航运等,主要在海底的哪种地形进行?( )A、① B、②
- 右面漫画中的“大饼”代表中国,而围着大饼的是手持匕首的列强,他们迫不及待地对着“大饼”下刀,唯恐落于人后,大饼的主人则只
- 19.仿照下面句式,写一个结构相似、复句形式相同的句子。 只有波涛澎湃的大海,才能创造出沙滩的光洁和柔软;而平静的
- 在一次实验课上,老师要求同学们用试管取一些稀盐酸,下列四位同学的操作合理的是()A. 向试管内注入1mL稀盐酸 B. 向
- 基因对性状的控制过程如下图:下列相关叙述中正确的是() A.①过程是转录,它以基因的两条DNA链分别为模板合成mRNA
- 下列关于氢氧化钠的描述错误的是() A.对皮肤有强烈的腐蚀作用 B.暴露在空气中易潮解 C.是常见的碱,俗称纯碱 D
- 下列词语中书写完全正确的一项是 ( ) A.锦标 棉里藏针 渡河 渡过难关 B.疆硬 信马由缰 反复 翻云覆雨
- 下图漫画中“谎言重复千遍便成了真理”的说法A.是正确的,看到了量的积累的重要性 B.是正确的,看到了认识具有反复性 C.
- 性染色体X和Y不可能同时存在于( )。A、肌细胞 B、上皮细胞 C、乳腺细胞 D、精子
- 某同学想测量某导电溶液的电阻率,先在一根均匀的长玻璃管两端各装了一个电极(接触电阻不计),两电极相距,其间充满待测的导电
- Sunday is the _______ day of a week.A.sixthB.lastC.seventhD.
- 3.依次填入下面一段文字横线处的语句,衔接最恰当的一组是( ) 我们所居的世界是最完美的,就因为它是最不完美的。__
- (2015•眉山模拟)关于下列四幅图的说法正确的是() A. 甲图的实验说明磁场能产生电流 B. 乙图的
- .在各项均为正数的等比数列中,且成等差数列.(1)求等比数列的通项公式;(2)若数列满足,求数列的前项和.



