卤素原子结构及其性质的比较 知识点题库
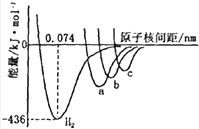
如图中四条曲线分别表示H2、Cl2、Br2、I2分子的形成过程中能量随原子核间距的变化关系,其中表示Cl2形成过程的曲线是(填“a”、“b”或“c”),理由是.
已知最外层电子数相等的元素原子具有相似的化学性质.下列原子中,与氟原子的化学性质相似的是( )
A . C
B . Ne
C . Al
D . Cl
砹(At)属于卤族元素之一,试推测砹(At)单质及其化合物不可能具有的性质是( )
A . 单质砹易溶于某些有机溶剂
B . AgAt是不溶于水的有色固体
C . HAtO4酸性比HClO4强
D . HAt难溶于水,且受热很难分解
卤素互化物是指不同卤素原子之间以共价键结合形成的化合物,XX’型卤素互化物与卤素单质结构相似、性质相近.试回答下列问题:
-
(1) 卤素互化物BrCl能发生下列反应
H2O+BrCl═HBrO+HCl
KBr+BrCl═KCl+Br2
①写出KI与IBr反应的化学方程式 .
②写出苯与(C6H6)与ICl发生取代反应生成一卤代物的化学方程式
-
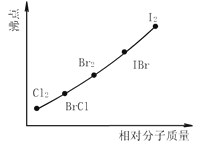
(2) 如图是部分卤素单质和XX′型卤素互化物的沸点与其相对分子质量的关系图.它们的沸点随着相对分子质量的增大而升高,其原因是
-
(3)
试推测ICl的沸点所处的最小范围
氢溴酸(HBr)的稀溶液与稀盐酸的化学性质十分相似,据此判断下列反应不会发生的是( )
A . 2HBr+Na2CO3═2NaBr+H2O+CO2↑
B . 2HBr+CaCO3═CaBr2+H2O+CO2↑
C . HBr+NaOH═NaBr+H2O
D . 2HBr+2Ag═AgBr+H2↑
下列各组物质混合,在冷暗处就可发生剧烈反应的是( )
A . H2和O2
B . H2和Cl2
C . H2和F2
D . H2和I2
根据题意解答
-
(1) 卤素互化物是指不同卤素原子之间以共价键结合形成的化合物,XX’型卤素互化物与卤素单质结构相似、性质相近.已知卤素互化物BrCl能发生下列反应H2O+BrCl=HBrO+HCl
KBr+BrCl═KCl+Br2试回答下列问题:
①写出KI与IBr反应的化学方程式;
②写出KOH与IBr反应的化学方程式;
③写出苯与(C6H6)与ICl发生取代反应生成一卤代物的化学方程式.
-
(2) 氰(CN)2、硫氰(SCN)2的化学性质和卤素(X2)很相似,化学上称为拟卤素.已知还原性强弱为:
Cl﹣<Br﹣<CN﹣<SCN﹣<I﹣.试写出:
①(CN)2与KOH溶液反应的化学方程式
②HSCN溶液与MnO2反应的化学方程式
③NaBr和KSCN的混合溶液中加入(CN)2 , 反应的离子方程式.
利用新制氨水、1mol/LNaBr溶液、淀粉液、以及II中所得溶液,验证卤素单质氧化性的相对强弱.
V分别取5mL 1mol/L NaBr溶液于两支小试管中
VI向两支试管中分别滴加5滴新制氯水,溶液均变为黄色
VII向其中一支试管中继续滴加新制氯水,直至溶液变为棕红色
VIII…
-
(1) 请写出步骤VI中反应的离子方程式;为验证溴的氧化性强于碘,步骤VIII的操作和现象是:,溶液变为黄色.再加入,溶液变为蓝色.
-
(2) 步骤VII的目的是.
-
(3) 氯、溴、碘单质的氧化性逐渐减弱的原因:,同主族元素从上到下,得电子能力逐渐减弱,非金属性减弱.
下列关于卤素形成的酸的水溶液性质,叙述不正确的是( )
A . HF、HClO都是弱酸,HClO3、HClO4均为强酸
B . HBr的水溶液有酸性、氧化性、还原性
C . HI的水溶液还原性很强,在空气中易被氧化变质
D . HX水溶液酸性顺序为:HCl>HBr>HI>HF
下列关于卤族元素的说法正确的是( )
A . F、Cl、Br、I最高正化合价都为+7
B . 卤族元素的单质只有氧化性
C . 从F到I,原子的得电子能力依次加强
D . 卤素单质与H2化合的难易程度按F2、Cl2、Br2、I2的顺序由易变难
下列关于卤素(用X表示)的叙述正确的是( )
A . 其单质都能与水反应,通式为X2+H2O=HX+HXO
B . HX易溶于水,其水溶液都是强酸
C . 其单质都有颜色,都有毒
D . 最高价含氧酸的通式为HXO4
碱金属元素和卤族元素广泛存在,用化学用语回答下列问题。
-
(1) 氢氟酸可以用来雕刻玻璃。用电子式表示氟化氢的形成过程。
-
(2) 过氧化钠可以用于潜水艇中氧气的来源,其与二氧化碳反应的化学方程式是。
-
(3) 次氯酸钠溶液(pH>7)和溴化钠溶液混合,可以作为角膜塑形镜的除蛋白液。二者混合后,溶液变成淡黄色,该反应的离子方程式是。
-
(4) Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl +S +SO2。组装该电池必须在无水、无氧的条件下进行,原因是(用化学方程式表示)。
-
(5) 关于碱金属和卤族元素,下列说法一定正确的是____________。A . 从上到下,单质密度依次增大 B . 从上到下,单质熔沸点依次升高 C . 从上到下,原子半径依次增大 D . 单质都可以与水反应
卤素单质按F2、Cl2、Br2、I2顺序,下列性质递变规律正确的是( )
A . 颜色由浅变深
B . 氧化性逐渐增强
C . 氢化物的稳定性逐渐增强
D . 密度依次减小
已知X、Y、Z、W是原子序数依次递增的同主族元素,下列常见的阴离子能影响水的电离平衡的是( )
A . X-
B . Y-
C . Z-
D . W-
随着卤素原子核电荷数的增加,下列递变规律正确的是( )
A . 单质的熔沸点逐渐降低
B . 气态氢化物的稳定性逐渐降低
C . 卤素最高价含氧酸酸性逐渐增强
D . 卤素单质的氧化性逐渐增强
常温下,下列物质中单质与水反应最剧烈的是( )
A .  B .
B .  C .
C . 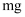 D .
D . 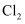
 B .
B .  C .
C . 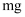 D .
D . 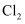
下列关于碱金属元素和卤素的说法中正确的是( )
A . 卤素单质越活泼,其熔沸点就越低
B . 卤素单质都能和水剧烈反应
C . 碱金属均能沉于煤油下方
D . 碱金属在空气中加热均能生成多种氧化物
关于卤素单质(X2)的下列叙述中正确的是( )
A . 都能与氢气因剧烈化合而爆炸
B . 都能与铁反应生成FeX3
C . 都能与钠反应生成NaX
D . 都能与水反应生成氢卤酸HX和次卤酸HXO
如图是金属镁和卤素单质(X2)反应的能量变化示意图。下列说法正确的是( )
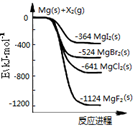
A . 还原性:F->Cl->Br->I-
B . 由MgCl2制取Mg的反应是吸热反应
C . 卤素单质(X2)与碱反应均可生成两种盐
D . 由图可知此温度下MgI2(s)与Br2(g)反应的热化学方程式为:MgI2(s)+Br2(g)=MgBr2(s)+I2(g) △H=+160 kJ·mol−1
某兴趣小组对化合物X开展探究实验。
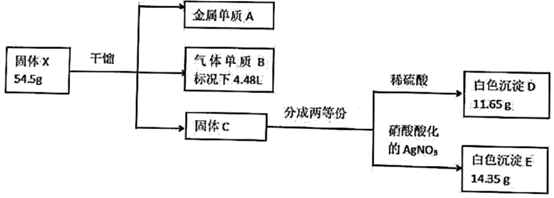
已知X是由三种元素组成的盐,金属单质A银白色常用于实验室做焰色反应实验,不溶于硝酸;气体B在标准状况下的密度为3.17 g/L;所加试剂均足量。
-
(1) X的化学式,固体C的电子式。
-
(2) 金属A溶于王水(浓硝酸:浓盐酸=1:3)生成化合物X对应的酸和遇空气显红棕色的气体,写出金属A溶于王水的化学方程式。
-
(3) 与B中元素同主族元素之间形成的化合物的性质与气体单质B相似,在碱性环境中,XO-→X-+XO
 ,非金属性越弱该反应越容易发生。写出该族第四周期与第五周期元素形成的化合物YZ与氢氧化钠溶液反应的离子方程式。
,非金属性越弱该反应越容易发生。写出该族第四周期与第五周期元素形成的化合物YZ与氢氧化钠溶液反应的离子方程式。
-
(4) 下列有关说法正确的是___________。A . 用金属A做焰色反应实验时,需用稀硫酸洗净 B . 某试剂做焰色反应实验时,火焰黄色,证明一定有钠盐,但不一定有钾盐。 C . 工业上使用阴离子交换膜电解饱和食盐水生产气体B D . 白色固体D可用于医疗上检查肠胃的内服药剂 E . 白色沉淀E在光照下颜色会变深,可能溶于氨水
最近更新
- ---Hurry! There's no time to waste. ---OK. But I'm afraid
- 估算的值 A、在1和2之间 B、在2和3之间 C、在3和4之间
- 为加强对抗震救灾资金物资监管,方便群众举报,中央纪委监察部设立号码为010一59592947的举报电话,24小时受理对抗
- 17. ______, his idea was actually worth practicing. A. As it
- 泰国大米连续6年稳居世界销量第一,由此赢得“世界米仓”的桂冠。泰国水稻种植的优越区位条件是 ①平原面积广,土壤肥沃
- Just look at the room. My roommate ____ up his clothes. A.is
- 是重要的核工业原料,在自然界的丰度很低。的浓缩一直为国际社会关注。下列有关说法正确的是( )A.原子核中含有92
- 如图所示,闭合导线框的质量可以忽略不计,将它从图示位置匀速拉出匀强磁场.若第一次用0.3 s时间拉出,外力做的功为W1,
- 如果=
- 光滑水平面上有大小相同的A、B两球在同一直线上运动。两球质量关系为,规定向右为正方向,A、B两球的动量均为,运动中两球发
- 通常情况下长江需要特别加固河堤的是( ) A.南岸 B.北岸 C.东岸
- 下边是关于某次战役的资料卡片,根据卡片信息推断它是()。 关于战役的卡片 信息1:1942年7月至1943年2月 信息2
- 下列各组词语中,有错别字的一组是 A.付出 入不敷出 桃园 世外桃源 B.淹没 湮没无闻 委屈
- 已知一个碳原子上连有两个羟基时,易发生下列转化:请根据下图回答。(1)E中含有的官能团的名称是_________;③的
- 分解因式:a3﹣a=__________.
- 解方程组:.
- 设a>0,b>0. 若关于x,y的方程组无解,则的取值范围是 .
- 质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。该燃料电池以氢气为燃料,空气为氧化剂,铂作催化剂,导电离子是H+
- 抛物线上一点到直线的距离最短,则该点的坐标是: A. B. C. D.
- 求x的值:49x2=(-4)2



