电子式、化学式或化学符号及名称的综合 知识点题库
有关化学用语正确的是( )
A . 四氯化碳的电子式: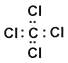 B . 氢氧根的电子式:
B . 氢氧根的电子式: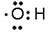 C . 乙烯的最简式 (实验式):C2H4
D . 乙醇的结构简式:CH3CH2OH
C . 乙烯的最简式 (实验式):C2H4
D . 乙醇的结构简式:CH3CH2OH
 B . 氢氧根的电子式:
B . 氢氧根的电子式: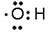 C . 乙烯的最简式 (实验式):C2H4
D . 乙醇的结构简式:CH3CH2OH
C . 乙烯的最简式 (实验式):C2H4
D . 乙醇的结构简式:CH3CH2OH
下列化学用语的使用正确的是( )
A . 氯化铵的电子式为 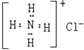 B . 重氢负离子(
B . 重氢负离子( 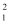 H﹣)的结构示意图为
H﹣)的结构示意图为  C . 次氯酸的结构式为H﹣Cl﹣O
D . 中子数为19的钙离子为
C . 次氯酸的结构式为H﹣Cl﹣O
D . 中子数为19的钙离子为  Ca2+
Ca2+
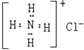 B . 重氢负离子(
B . 重氢负离子( 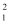 H﹣)的结构示意图为
H﹣)的结构示意图为  Ca2+
Ca2+
下列有关化学用语使用正确的是( )
A . 34S2﹣的结构示意图: 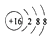 B . H2O2的电子式:
B . H2O2的电子式: 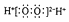 C . 甲烷分子的比例模型:
C . 甲烷分子的比例模型: 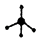 D . 中子数为18的硫原子:
D . 中子数为18的硫原子:  S
S
 S
S
下列化学用语或模型表示正确的是( )
A . 氚原子符号:H
B . H2O2分子结构式:H﹣O﹣O﹣H
C . Mg2+结构示意图: 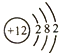 D . HF的形成过程
D . HF的形成过程 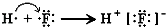
 D . HF的形成过程
D . HF的形成过程
下列物质的电子式书写正确的是( )
A . 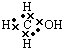 B .
B . 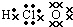 C .
C . 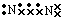 D .
D . 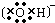
氨气是重要的化工原料,可以用来制备硝酸以及各种化肥产品.
-
(1) 氨分子的电子式为.
-
(2) 写出一水合氨的电离方程式;现在在10mL0.1mol/L的一水合氨溶液中滴加0.1mol/L的盐酸,若要使在常温下混合溶液的pH=7,那么需要滴加盐酸溶液的体积 10mL(选填大于、等于、小于)
-
(3) 用两根玻璃棒,一根蘸取浓氨水,一根蘸取浓硫酸,当两根玻璃棒靠近时,出现的现象是;该反应的化学方程式为.
表示下列粒子结构的图式,不正确的是( )
A . 乙烯的结构式: 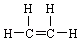 B . 钠离子的结构示意图:
B . 钠离子的结构示意图: 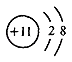 C . 氢分子的电子式:H:H
D . 氯化氢分子的电子式:
C . 氢分子的电子式:H:H
D . 氯化氢分子的电子式: 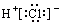
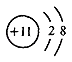 C . 氢分子的电子式:H:H
D . 氯化氢分子的电子式:
C . 氢分子的电子式:H:H
D . 氯化氢分子的电子式: -
(1) Ⅰ.将等物质的量的A和B,混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)
 xC(g)+2D(g),5min 后测得c(D)=0.5 mol/L,c(A):c(B)=1:2,C的反应速率是0.15 mol/(L•min)。
xC(g)+2D(g),5min 后测得c(D)=0.5 mol/L,c(A):c(B)=1:2,C的反应速率是0.15 mol/(L•min)。 B的反应速率v(B)=,X=。
-
(2) A在5min末的浓度是。
-
(3) 此时容器内的压强与开始时之比为。
-
(4) Ⅱ.二氯化二硫(S2Cl2)是一种琥珀色液体,是合成硫化染料的重要原料。
a.S2Cl2分子中所有原子都满足8电子稳定结构,写出它的电子式;
b.指出它分子内的键型。
-
(5) 硒的原子序数为34,硒的单质及其化合物用途非常广泛。
a.硒在元素周期表中的位置是。
b.硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是(填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
回答下列问题
-
(1) 画出磷原子的原子结构示意图:。
-
(2) 写出H2S分子的电子式:。
-
(3) 写出表示含有8个质子,10个中子的原子的化学符号:。
-
(4) 已知阴离子aXm—和阳离子bYn+具有相同的核外电子排布,则a、
B、m、n之间的关系为a=。
-
(5) 用电子式表示氯化镁的形成过程:。
-
(6) 写出Na2O2中所含化学键的类型。
-
(7) 拆开1mol H—H键,1mol N—H键, 1mol
 键分别需要吸收的能量为436kJ ,391kJ,946kJ:则1mol N2完全转化成NH3热量(填“吸收”或“放出”)kJ;
键分别需要吸收的能量为436kJ ,391kJ,946kJ:则1mol N2完全转化成NH3热量(填“吸收”或“放出”)kJ;
-
(8) 利用下列反应:Fe+Cu2+=Fe2++Cu 制一个化学电池,写出电极反应式:负极:;正极__。
将对应的符号或名称补充完整):
2个氢原子 FeSO4
硝酸根离子 Ca(OH)2
烃是一类简单的有机化合物。
-
(1) 天然气属于(填“纯净物”或“混合物”),其组成以为主。该分子的电子式是,其空间结构是。
-
(2) 烷烃随着碳原子数的增多,沸点逐渐(填“升高”或“降低”),碳原子数≤的烷烃呈气态,它们和氯气发生取代反应的条件是。
-
(3) 2,2,3-三甲基丁烷的结构简式是,其一氯代物有种,该烷烃与正庚烷互为(填“同系物”或“同分异构体”)。
下列表示不正确的是( )
A . Na+的结构示意图  B . 水分子的结构式:
B . 水分子的结构式: 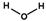 C . 乙烯的球棍模型
C . 乙烯的球棍模型  D . CO2的电子式
D . CO2的电子式 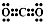
 B . 水分子的结构式:
B . 水分子的结构式:
下列化学用语表述错误的是( )
A . 电解CuCl2溶液:Cu2++2Cl-  Cu+Cl2↑
B . NaCl的形成过程:
Cu+Cl2↑
B . NaCl的形成过程: 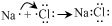 C . HCl在水中电离:HCl=H++Cl-
D . NH4Cl在水中发生水解:NH4++H2O
C . HCl在水中电离:HCl=H++Cl-
D . NH4Cl在水中发生水解:NH4++H2O  NH3·H2O+H+
NH3·H2O+H+
 Cu+Cl2↑
B . NaCl的形成过程:
Cu+Cl2↑
B . NaCl的形成过程:  NH3·H2O+H+
NH3·H2O+H+
下列化学用语和化学符号使用正确的是( )
A . 次氯酸的结构式:H-Cl-O
B . CCl4的比例模型:  C . 碳酸氢钠的电离方程式:NaHCO3=Na++HCO
C . 碳酸氢钠的电离方程式:NaHCO3=Na++HCO  D . 氨基的电子式:
D . 氨基的电子式: 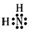
 D . 氨基的电子式:
D . 氨基的电子式:
下列表示错误的是( )
A . 羟基的电子式 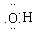 B . 丁烷的球棍模型
B . 丁烷的球棍模型 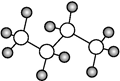 C . 乙烯的球棍模型
C . 乙烯的球棍模型 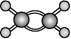 D . CH3-C≡C-CH(CH3)2的名称是2-甲基戊炔
D . CH3-C≡C-CH(CH3)2的名称是2-甲基戊炔
 C . 乙烯的球棍模型
C . 乙烯的球棍模型
NaN3是一种易溶于水( 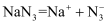 )的白色固体,可用于有机合成和汽车安全气囊的产气药等,钠法(液氨法)制备NaN3的工艺流程如图:
)的白色固体,可用于有机合成和汽车安全气囊的产气药等,钠法(液氨法)制备NaN3的工艺流程如图:
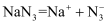 )的白色固体,可用于有机合成和汽车安全气囊的产气药等,钠法(液氨法)制备NaN3的工艺流程如图:
)的白色固体,可用于有机合成和汽车安全气囊的产气药等,钠法(液氨法)制备NaN3的工艺流程如图: 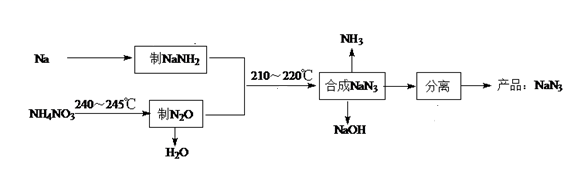
-
(1) 钠元素位于周期表第周期第族。
-
(2) NH3的电子式为。
-
(3) 反应NH4NO3
 N2O↑+2H2O↑中,每生成1molN2O转移电子的物质的量为mol。
N2O↑+2H2O↑中,每生成1molN2O转移电子的物质的量为mol。
-
(4) 销毁NaN3可用NaClO溶液,该销毁反应的离子方程式为(
 被氧化为N2)。
被氧化为N2)。
下列化学用语表达正确的是( )
A . 纯碱的化学式: B . 气体的摩尔体积为22.4L/mol
C . NaOH的电子式:
B . 气体的摩尔体积为22.4L/mol
C . NaOH的电子式: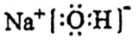 D . 钠离子的结构示意图:
D . 钠离子的结构示意图: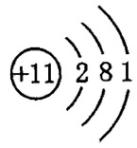
 B . 气体的摩尔体积为22.4L/mol
C . NaOH的电子式:
B . 气体的摩尔体积为22.4L/mol
C . NaOH的电子式: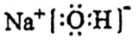 D . 钠离子的结构示意图:
D . 钠离子的结构示意图:
下列化学用语表示错误的是( )
A . CO2的分子模型示意图: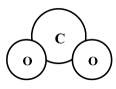 B . sp2杂化轨道模型:
B . sp2杂化轨道模型: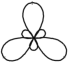 C . HIO的电子式:
C . HIO的电子式: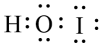 D . HCN的结构式:H—C≡N
D . HCN的结构式:H—C≡N
 B . sp2杂化轨道模型:
B . sp2杂化轨道模型: C . HIO的电子式:
C . HIO的电子式:
元素符号、反应方程式、结构示意图、电子式以及结构式统称为化学用语。下列有关化学用语的表示方法错误的是( )
A . 质子数为17,中子数为20,电子数为18的微粒符号:  B . 乙烯分子的结构简式:
B . 乙烯分子的结构简式: 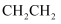 C .
C . 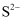 的结构示意图:
的结构示意图: 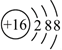 D . 次氯酸的电子式:
D . 次氯酸的电子式: 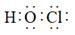
 B . 乙烯分子的结构简式:
B . 乙烯分子的结构简式: 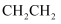 C .
C . 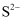 的结构示意图:
的结构示意图: 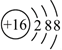 D . 次氯酸的电子式:
D . 次氯酸的电子式:
X、Y、Z,W、R是原子序数依次增大的前四周期元素(0族元素除外)。X的简单气态氢化物M呈正四面体结构;Y的某种单质可作为杀菌消毒剂;Z的原子半径在短周期中最大;W的质子数等于X与Z的质子数之和;R有多种氧化物,其中一种氧化物可作为红色油漆或涂料。用相关化学用语回答下列问题:
-
(1) W元素在周期表中的位置是,
 溶液保存时常加入,检验
溶液保存时常加入,检验 溶液是否变质的实验方案是。
溶液是否变质的实验方案是。
-
(2)
 的电子式为,
的电子式为, 含有的化学键是。
含有的化学键是。
-
(3) Y的简单氢化物由液态变为固态时密度减小,其原因是。
-
(4) 工业上可利用电子传感器检测来煤坑道中化合物M的含量,其工作原理如下图所示,则多孔石墨电极a的电极反应式为。
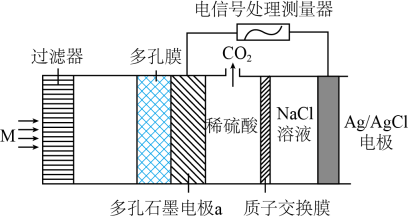
最近更新
- 在资源的利用过程中,发生了化学变化的是() A.利用海水晒盐 B.用干冰人工降雨 C.公交车使用天然气作燃料
- 2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系。下列叙述错误的是( ) A.a为电池的正极
- 下列各项中,没有错别字的一项是 A.座谈 婉约 绊脚石 再接再厉 B.祥瑞 程式
- 科学家成功地把人的抗病毒干扰素基因植入烟草细胞中的DNA分子上,使烟草获得了抗病毒的能力。这个事实说明,DNA上控制生物
- 法国一科学家在研究牲口炭疽病时,进行了如下实验:把供实验用的绵羊分为甲、乙两组。甲组绵羊用病毒性已削弱的炭疽病的病原体注
- 某同学探究骨骼肌的收缩情况,将带有坐骨神经的腓肠肌标本如下图装置,根据实验分析:(1)针刺实验装置中的腓肠肌,发现指针向
- 如图,点在的平分线上,,则需添加的一个条件是(只写一个即可,不添加辅助线):
- 下列实验装置设计正确的是
- 补写出下列名篇名句中的空缺部分,任选5句。(5分) (1) ,情随事迁,感慨系之矣。
- 19. 补写出下列名篇名句中的空缺部分。(6分) (1)看万山红遍,层林尽染;漫江碧透, 。(《沁园春·长
- I don’t know the time because I mywatch at home.
- 在电场中描绘等势线的实验中,如改用电压表代替灵敏电流表,该如何找出等势点?
- 下列变化中,前者是物理变化,后者是化学变化,且都有明显颜色变化的是 A.用冰水混合物冷却SO3气体;加热I2 B
- After a short holiday, he _____ himself once more to his stu
- 下列化合物中既易发生取代反应,也可发生加成反应,还能使KMnO4酸性溶液褪色的是A.乙烯 B.乙醇 C.甲苯
- 埃及斑蚊是传播某种传染病的媒介.某地区在喷洒杀虫剂后,此蚊种群数量减少了99%,但一年后,该种群又恢复到原来的数量,此时
- 已知双曲线C:的一个焦点是,且. (1)求双曲线C的方程; (2)设经过焦点的直线的一个法向量为,当直线与双曲线C的右支
- 下列关于胶体和溶液的比较中,正确的是( )A.溶液中溶质粒子不带电,胶体分散质粒子带电B.溶液中通过一束光线没有特
- 下列说法正确的是 A.将CO2通入溶有足量氨气的BaCl2溶液中,无白色沉淀生成 B.将盐酸、KSCN溶液
- 如图3所示,闭合开关S后,当滑片P向左移动时,电压表示数将 ;当滑片P在滑动变阻器的a、c两个端点位置时,电压表



