碳、一氧化碳、氢气还原氧化铜实验 知识点题库
下列实验基本操作中错误的是( )
(1)加热
(2)停止加热
(3)通纯净的氢气
(4)停止通氢气.
(1)可用于净化空气的是
(2)可用于制电线的是
(3)可用作食品干燥剂的是
(4)可用作干电池的电极的是

-
(1) B中反应的化学方程式是 ,该反应的还原剂是 .
-
(2) 实验过程中,C中的现象是 ,D处点燃的目的是
-
(3) 对该实验的分析正确的是 (选填编号)
A.实验结束时应先熄灭B处酒精灯
B.C中增加的质量与B中固体减少的质量相等
C.实验过程中,共通入0.56g一氧化碳可生成1.28g铜
D.反应结束后继续通入一氧化碳的目的是防止铜被氧化
-
(4) 甲同学认为A装置用于证明一氧化碳不能和石灰水反应,乙同学认为省略A可达到同样的目的,理由是 .
-
(1) 除去铁锈可以用.
-
(2) 食盐中添加可以预防甲状腺肿大.
-
(3) 梧州地处红壤地区,土壤显酸性,农业上常用改良酸性土壤.


|
| | |
| 甲 | 乙 | 丙 |
-
(1) 甲中获得铁的化学方程式是。
-
(2) 乙中证明铁发生反应的依据是。
-
(3) 丙中能发生反应的原因是。

-
(1) A实验中集气瓶内水的作用是。
-
(2) B实验中玻璃管的作用是。
-
(3) C实验过程中,当蒸发皿中出现时,停止加热。用提纯的精盐配制100g 7.5%的生理盐水,若溶质质量分数偏小,其原因可能有。
①氯化钠固体不纯
②用量筒量取水时操作有误,如取水时俯视读数
③烧杯中有水
④称量时精盐和砝码放反了
⑤装瓶时,有少量溶液洒出
-
(4) D实验中酒精灯加网罩的作用。

-
(1) A中的反应的方程式为
-
(2) 请画出B中的导管示意图。
-
(3) 如何检验反应后B溶液中仍有氢氧化钠?

 提示:木炭不与稀硫酸反应
提示:木炭不与稀硫酸反应 
-
(1) 过滤操作中必须用到的玻璃仪器有:烧杯、玻璃棒和。
-
(2) 反应
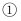 的化学方程式为。
的化学方程式为。
-
(3) 反应
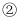 属于反应
属于反应  填写基本反应类型
填写基本反应类型  ,滤液Ⅱ中的溶质为
,滤液Ⅱ中的溶质为  填写化学式
填写化学式  。
。
-
(4) 试剂甲可以选用下列溶液中的
 填序号
填序号  。
。 
-
(5) 对滤渣Ⅰ进行分析,肯定含有的物质是,为了完善实验方案,可对滤渣Ⅰ中的进行回收。


-
(1) 能证明废气中有水蒸气存在的现象是;发生反应的化学方程式是。
-
(2) B的作用是。
-
(3) 仅根据E中澄清石灰水变浑浊,无法确定一氧化碳的存在,其理由是。
-
(4) 如果D处黑色粉末变红,则说明废气中含有,D处玻璃管中发生反应的化学方程式是。
-
(5) F处的大号注射器,可以引导气体流向,其另一个主要作用是。
-
(1) 下列物质均由离子构成的是 。A . CO2、CO B . 碳酸镁、碳酸钠 C . 甲烷、乙烯 D . 金刚石、石墨
-
(2) CO和CO2均为碳的氧化物,且组成元素相同,但它们的化学性质却有很大的区别,这是因为 。
-
(3) 实验室可用如图所示的装置制取纯净、干燥的CO,然后用CO还原Fe2O3并检验气体产物。

①C装置中的加热仪器的名称是 ;C装置中反应的化学方程式为 。
②A装置中草酸(H2C2O4)在浓硫酸和加热的条件下发生分解生成CO、H2O和另一种氧化物,请写出反应的化学方程式:。
③为达到实验目的,正确的接口连接顺序为a接、接、接、 接 。
④该实验装置有不足之处,请给出改进措施。
-
(4) 二氧化碳与水和偏铝酸钠(NaAlO2)反应生成碳酸氢钠和难溶于水的氢氧化铝,若有66g二氧化碳与偏铝酸钠溶液充分反应,理论上可以生成多少克氢氧化铝?

(提出问题)HDPE膜由什么元素组成?
(查阅资料)①HDPE膜能够燃烧,燃烧可能生成一氧化碳;
②碱石灰主要成分是氢氧化钠固体和氧化钙固体。
(实验探究)如图所示,先通入干燥氮气,再将4.2g的HDPE膜样品在足量的氧气中点燃,并将燃烧产物依次通过装置A、B、C、D(装置中每步反应均进行完全)。

(实验记录)
| 装置质量 | A装置总质量 | C装置总质量 |
| 实验前 | 100.0 | 100.0g |
| 实验后 | 105.4g | 113.2g |
-
(1) (实验分析)
装置A中浓硫酸的作用是。
-
(2) 实验中观察到装置B中黑色粉末变成红色,证明HDPE膜燃烧产物中有。
-
(3) 装置B中发生的化学反应方程式为。
-
(4) 小华同学想探究反应后装置C中的溶质,设计了以下实验方案,请你帮他完成实验报告。
实验步骤
实验现象
实验结论
①取适量溶液于试管中,滴加足量的溶液,
出现,
则装置C中的溶质含有Na2CO3。
②静置后.再在上述溶液中滴加,
溶液变成红色,
则装置C中的溶质除Na2CO3之外,还有。
-
(5) (数据处理和实验结论)
通过记录A、C装置反应前后的质量变化,根据质量守恒定律得出:HDPE膜由(填元素符号)元素组成。

-
(1) 常温下,若乙为红色粉末,甲为黑色粉末,则丙的化学式是,甲与乙反应的化学方程式为。
-
(2) 若丁为常见难溶性盐,常温下甲为气体,则:甲与乙反应的化学方程式为,乙与丙反应的化学方程式为。

-
(1) 酒精灯加网罩的目的。
-
(2) 加热一段时间后,观察到被加热的试管中的现象是,发生反应的化学方程式为。
-
(3) 停止加热时,应该。
- 书面表达 请你根据下列材料写一篇介绍猴子Molly的小短文。 ⒈ 猴子名字:Molly; ⒉ 性别:雌性; ⒊ 籍贯:黔
- 若集合,,则集合等于( ) A. B. C. D.
- 阅读下面一首古诗,回答以下问题。秋夜曲张仲素丁丁漏水夜何长,漫漫轻云露月光。秋逼暗虫通夕响,征衣未寄莫飞霜。注:漏水:古
- 图3是观察电容器放电的电路,电源直流电压为8V。先将开关S与1相连,电源向电容器充电,然后把开关S掷向2端,电容器通过电
- 如图,用皮带传动的两个轮子(设皮带不打滑),A点为轮边缘处一点,B点为轮边缘处一点,C点为轮上的一点。已知,则:(
- 巫医乐师百工之人,君子不齿, , !(韩愈《师说》)
- 读我国某区域图,回答下列问题。(10分) 材料一 宁东——山东±660千伏直流输电工程将该区域生产的电力直送
- 已知豌豆种皮灰色(G)对白色(g)为显性,子叶黄色(Y)对绿色(y)为显性。如以基因型ggyy的豌豆为母本,与基因型Gg
- 下列关于两极格局形成的表述,不正确的是( ) A.美苏国家利益和意识形态矛盾冲突加剧是两极格局形成的原因
- 下列词语中,没有错别字的一组是( )A.抉择 自负盈亏 不胫而走 一寸光荫一寸金B.凭悼 各行其是
- 《独立宣言》写道:“代表权对人民来说具有无可估量的意义,而对暴君来说是可怕的。”这句话体现在美国1787年宪法中就是(
- 当前我国笔记本电脑价格出现了“大跳水”现象。一方面随着我国电脑行业技术日益成熟,劳动生产率不断提高,给降价带来了很大空间
- 下列说法正确的是 A. 需加热才能发生的反应一定是吸热反应 B. 任何放热反应在常温条件一定能发生反应 C. 反应物和生
- 15世纪末16世纪初所谓“地理大发现”的含义是:() A.发现了美洲大陆 B.开辟了欧洲到亚洲的新航路 C.人类首次完成
- American parents usually think that theirchild should not ha
- 如图表示有关蛋白质分子的简要概念图,对图示分析正确的是( )A.a中肯定含有S元素 B.①过程形成多肽的方式是脱
- 用二分法求方程的近似根的算法中要用哪种算法结构( )A.顺序结构 B.条件结构 C.循环结构 D.
- 中新网2009年10月12日电:据发改委网站消息,为深入推进西部大开发,积极扩大内需,促进西部地区平稳较快发展,国家计划
- 阅读下面选文,完成以下小题。 下午,医生来了,“她现在脱离危险了,现在只要注意营养和调理就行了。”医生抓住苏艾颤抖的手说
- 拿破仑说:“我的真正光荣并非是打了40次胜仗;滑铁卢之战抹去了关于这一切的回忆。但有一样东西是不会被人遗忘的,它将永垂不






