离子或物质的共存问题 知识点题库
下列离子在pH=1和pH=14的两种溶液中都能大量存在的是( )
A . Cl﹣
B .  C . Mg2+
D .
C . Mg2+
D . 
 C . Mg2+
D .
C . Mg2+
D . 
下列各组物质在pH=3的溶液中能大量共存,且形成无色溶液的是( )
A . KCl、NaCl、Na2CO3
B . AgNO3、NaNO3、HCl
C . CuSO4、H2SO4、MgCl2
D . KNO3、Ca(NO3)2、NH4Cl
下列离子能在pH=1的无色溶液中大量共存的是( )
A . Cu2+、SO  、Cl-、Na+
B . OH-、K+、NO
、Cl-、Na+
B . OH-、K+、NO  、Ba2+
C . Mg2+、SO
、Ba2+
C . Mg2+、SO  、Al3+、NO
、Al3+、NO  D . Na+、CO
D . Na+、CO 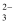 、Ca2+、Cl-
、Ca2+、Cl-
 、Cl-、Na+
B . OH-、K+、NO
、Cl-、Na+
B . OH-、K+、NO  、Ba2+
C . Mg2+、SO
、Ba2+
C . Mg2+、SO  、Al3+、NO
、Al3+、NO  D . Na+、CO
D . Na+、CO 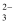 、Ca2+、Cl-
、Ca2+、Cl-
下列物质中,能在溶液中大量共存的是( )
A . Na2CO3、K2SO4、HCl
B . FeCl3、NaNO3、NaOH
C . Ca(OH)2、NaCl、HCl
D . CuSO4、NaNO3、H2SO4
分别将下列各组物质(其中酸是过量的)同时加入水中,最后能得到无色透明的溶液的是( )
A . FeCl3、KOH、H2SO4
B . Na2CO3、Ca(OH)2、HNO3
C . CuSO4、NaOH、HNO3
D . Ba(OH)2、H2SO4、HCl
将下列物质同时加入到水中,能大量共存且得到无色透明溶液的是( )
A . CaCl2 HCl NaNO3
B . KOH HCl (NH4)2SO4
C . K2CO3 Ba(NO3)2 NaOH
D . FeCl3 NaCl KNO3
甲、乙两化工厂分布如图所示,箭头代表水流方向,如果在a处取水样检测,水中含有少量NaOH、Na2SO4;在c处取水样检测,pH=7且水中只含有少量NaCl.则b处水中含有的一组物质是( )

A . MgSO4 NaCl
B . H2SO4 Ba(NO3)2
C . BaCl2 HCl
D . H2SO4 MgCl2
某校化学兴趣小组在课外活动中,对某溶液进行了多次检验,其中3次检验的结果如表所示.
序号 | 溶液中检验出的物质 |
① | KCl、K2SO4、Na2CO3 |
② | Na2SO4、BaCl2、K2CO3 |
③ | Na2SO4、KCl、K2CO3 |
阅读表后回答:
-
(1) 表中第次结果肯定不准确.
-
(2) 为验证其他2次检验结果中是否存在SO42﹣、CO32﹣和Cl﹣ , 又进行以下操作:①加入过量的(填物质名称,下同),目的是检验并将其除去;②加入溶液,过滤;③向滤液中加入溶液.该小组同学查阅资料后,发现可以利用焰色反应来确定溶液中存在的阳离子.
-
(3) 通过上述实验,该小组还是觉得无法确定其他2次检验结果中哪一次是正确的,你认为可能的原因是.
在水溶液中,一般不跟其他物质发生复分解反应的是( )
A . 氯化钾
B . 硝酸
C . 硝酸钠
D . 氢氧化钠
某不纯的 K2CO3 样品中可能含有的杂质是 Na2CO3、KNO3、CuSO4 和 Ba(NO3)2 几种物质中的一种或几种,进行以下实验:
①取一定量该样品放入烧杯中并加入足量水搅拌后,样品全部溶解且得到无色溶液;
②向无色溶液中加入过量的 CaCl2 溶液充分反应,出现白色沉淀,将白色沉淀经过滤、洗涤、干燥、称量。根据上述实验现象回答:
-
(1) 样品所含杂质肯定没有;
-
(2) 若所取的样品为 13.8 克,得到白色沉淀 9 克,则样品中杂质的可能组成:。
下列各组离子在溶液中能大量共存的是( )
A . Ca2+ Cl− Na+  B . Cu2+ K+
B . Cu2+ K+  OH−
C . H+ Na+
OH−
C . H+ Na+ 
 D . K+ Na+
D . K+ Na+ 

下列离子能在 pH=1 的溶液中大量共存的是( )
A . Ag+、  -、Cl-、Na+
B . OH-、K+、
-、Cl-、Na+
B . OH-、K+、  、Ba2+
C . Mg2+、
、Ba2+
C . Mg2+、  、Al3+、
、Al3+、  D . Na+、
D . Na+、  、Ca2+、Cl-
、Ca2+、Cl-
现有含NaCl、Na2SO4、NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、NO3-的相互分离。相应的实验过程可用下列流程图表示:

-
(1) 写出上述实验过程中所用试剂、沉淀的化学式:试剂1:试剂3:沉淀C:
-
(2) 写出溶液a中所含有的阳离子
-
(3) 恰当地控制试剂4的加入量的方法是
有一包白色粉末,可能含有Ba(OH)2、KNO3、FeCl3、Na2CO3、Na2SO4中的一种或几种。为了确定其成分,进行如下实验:
① 取一定量的白色粉末加入足量的水,振荡,静置,得到白色沉淀,上层清液为无色。
② 过滤,在白色沉淀中加入一定量的稀盐酸,白色沉淀部分溶解,且有气泡产生,产生的气体能使澄清石灰水变浑浊。
-
(1) 据此推断,该白色粉末中一定含有;可能含有。
-
(2) 写出部分沉淀被溶解的化学方程式:。
下列各组离子能在指定溶液中大量共存的一组是( )
A . 在pH=1的溶液中:Ba2-、CO32-、Zn2-
B . 在pH=13的溶液中:H+、Mg2-、Cl−
C . 在氯化钠溶液中:Ag+、Ca2-、NO3-
D . 在氢氧化钠溶液中:Na+、Ba2+、Cl-
甲、乙、丙、丁四种溶液中,分别含有Ba2+、Mg2+、Na+、H+、Cl-、CO32-、SO42-、OH-中的一种阳离子和一种阴离子。为确定四种溶液中所含的离子,小科进行了下面实验:
①将甲溶液分别与其他三种溶液混合,都有白色沉淀生成;
②将乙溶液与丁溶液混合,有气泡产生;
③向丙溶液中滴入AgNO3溶液,出现白色沉淀,加稀硝酸后,沉淀不消失;
分析实验得到的以下结论中错误的是( )
A . 甲溶液中一定含有Ba2+
B . 乙溶液中可能含有SO42-
C . 丙溶液中一定含有Cl-
D . 丁溶液中一定含有Na+
某无色溶液中,可能含有Na+ 、H+、Cl-、SO42-四种离子。现欲检验两种阴离子是否存在,进行了如下操作:
-
(1) 取适量溶液,先向其中滴加足量的溶液,若有白色沉淀生成,则证明有SO42-存在;
-
(2) 再取上层清液再滴加溶液,又出现白色沉淀,则可证明有Cl-的存在。
二氧化硫是大气的主要污染物,严禁直接排放,工业上常用NaOH溶液来吸收。

-
(1) 写出NaOH溶液吸收SO2的化学方程式。
-
(2) 图中小球分别表示NaOH溶液及吸收SO2后所得溶液中溶质的微粒,其中"●"表示的微粒是。
有一包白色固体,可能由BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种组成。为确定其成分,实验小组进行实验。实验过程中所加试剂均足量,实验过程及现象如图所示。


-
(1) 白色沉淀A与稀盐酸反应的化学反应方程式:。
-
(2) 白色沉淀C的化学式为。
-
(3) 这包白色固体是由(填化学式)组成的。
某无色透明的溶液,在 pH=0 和 pH=14 的条件下都能大量共存的是( )
A . Fe2+、K+、  、
、 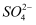 B . Mg2+、
B . Mg2+、  、
、 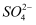 、Cl-
C . Ba2+、Na+、
、Cl-
C . Ba2+、Na+、  、
、 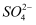 D . Na+、K+、
D . Na+、K+、  、
、 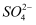
 、
、 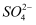 B . Mg2+、
B . Mg2+、  、
、 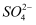 、Cl-
C . Ba2+、Na+、
、Cl-
C . Ba2+、Na+、  、
、 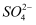 D . Na+、K+、
D . Na+、K+、  、
、 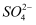
最近更新
- Myheart sank when the man at the immigration counter gesture
- 下图是实验室制取气体的一些常见装置。请回答下列问题:(1)标号为①仪器的名称是 ; (2)实验室用高锰
- 下列关于热化学反应的描述中正确的是 A.CO(g)的燃烧热是283.0 kJ·mol−1,则反应2CO2(g)=2CO(
- 如图所示,在距地面一定高度的地方以初速度v0向右水平抛出一个质量为m,带负电,电量为Q的小球,小球的落地点与抛出点之间有
- 当前,在部分中学生的日常生活消费中出现了追求名牌的风气。针对这种现象,你认为正确的态度应该是( ) ①摒弃盲目攀比
- 阅读下面两首诗,然后回答问题(8分)夜书所见叶绍翁萧萧梧叶送寒声,江上秋风动客情。知有儿童挑促织,夜深篱落一灯明。春兴武
- 当u>2f时,凸透镜能够成缩小的实像,利用这种现象制成的光学仪器是: A. 照相机; B.幻灯机;
- 用下列序号填空: ①烧杯 ②试管 ③胶头滴管 ④玻璃棒 ⑤量筒 ⑥漏斗:能直接加热的玻璃仪器 ; 吸取
- 在场强大小为E的匀强电场中,一质量为m、带电荷量为+q的物体以某一初速沿电场反方向做匀减速直线运动,其加速度大小为0.8
- 恒温恒容的情况下,反应A2(g)+B2(g)2AB(g)达到平衡状态的标志是 A.容器内气体的密度不随时间而变化 B.容
- 我国新修订的《环境空气质量标准》增加了PM2.5监测指标。PM2.5(particulatematter)是指2.5微米
- (08年湖北卷文)(本小题满分12分) 如图,在直三棱柱中,平面侧面 (Ⅰ)求证: (Ⅱ)若,直线AC与平面所
- 阅读下列景观图片和气候统计图,判断对应关系,并按要求填表。
- 点A(-3,4)和B(3,4)关于_________对称.
- 有机化学反应因反应条件不同,可生成不同的有机产品。例如: (1) (X为卤素原子) (2)苯的同系
- 下列物质溶解于水时,溶液的温度无明显变化的是( )A、浓硫酸 B、氢氧化钠固体 C、氧化钙固体 D、硝酸钾
- — We haven’t heard from Jane for a long time. — What do you
- 4.依次填入下面一段文字横线处的语句,前后衔接最为恰当的一组是( ) 中国人民抗日战争的胜利,充分证明了中国是救亡
- 读珠江三角洲图,完成第5~6题。5.省级行政单位A的优良港口是() A.太子港 B.维多利亚港
- 亚洲某地,位于45°E、20°N,该地所在国家有着独特的自然与人文景观。结合下图,该地所属的气候类型是() 图2-T2-



