第3章 物质的性质与转化 知识点题库
 可回收垃圾
B .
可回收垃圾
B .  餐厨垃圾
C .
餐厨垃圾
C .  有害垃圾
D .
有害垃圾
D .  其他垃圾
其他垃圾
要求且完全正确的是( )
选项 | 实验操作 | 实验现象 | 实验结论 | 离子反应 |
A | 向FeCl2溶液中加入Zn片 | 浅绿色溶液变为无色 | Zn具有还原性 | Fe2++Zn═Zn2++Fe |
B | 向FeCl2溶液中滴新制氯水 | 浅绿色溶液变为棕黄色 | Fe2+具有还原性 | 2Fe2++Cl2═2Fe3++2Cl﹣ |
C | 向FeCl3溶液中加入铁粉 | 棕黄色溶液变为浅绿色 | Fe具有还原性 | Fe+Fe3+═2Fe2+ |
D | 向FeCl3溶液中加入铜粉 | 蓝色溶液变为棕黄色 | Fe3+具有氧化性 | Fe3++Cu═Fe2++Cu2+ |
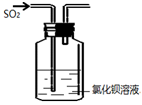
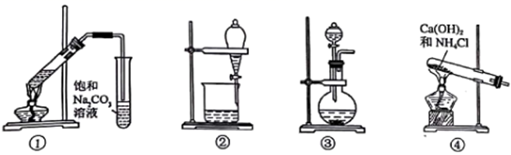
用图装置(还有一部分装置没画出)来验证某混合气体中同时含有SO2和CO2
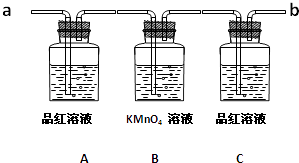
①实验时,该混合气体应从端通入; 从端连接盛有澄清石灰水的实验装置(用“a”或“b”填空).
②预期能观察到A瓶溶液中的现象为.
③C瓶溶液的作用是.
④证明该混合气体中含有CO2的实验现象是.
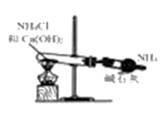 B . 向容量瓶中转移溶液
B . 向容量瓶中转移溶液 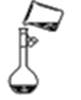 C . 吸收HCl
C . 吸收HCl 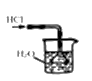 D . 稀释浓硫酸
D . 稀释浓硫酸 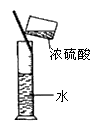
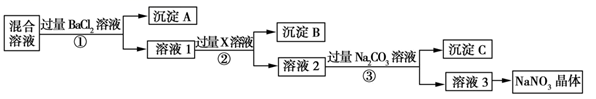
请回答下列问题:
-
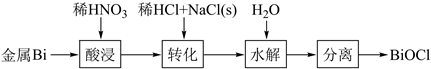
(1) 写出实验流程中下列物质的化学式:试剂X,沉淀A。
-
(2) 上述实验流程中①②③步均要进行的实验操作是(填操作名称)。
-
(3) 上述实验流程中加入过量Na2CO3溶液的目的是。
-
(4) 按此实验方案得到的溶液3中肯定含有(填化学式)杂质。为了解决这个问题,可以向溶液3中加入适量的(填化学式),之后若要获得NaNO3晶体,需进行的实验操作是(填操作名称)。
-
(1) 实验室用废铜屑制备SO2的化学方程式为。
-
(2) 将SO2通入NaHS溶液,溶液中有淡黄色沉淀,说明SO2具有性。
-
(3) 将SO2通过品红溶液,溶液红色逐渐褪去,将褪色后的溶液微热,又显浅红色,这现象可解释为。
-
(4) 将SO2通入橙黄色酸性K2Cr2O7溶液,溶液逐渐变为浅绿色,该反应中氧化剂与还原剂的物质的量之比为。(Cr2O72-被还原为Cr3+)
-
(5) 常温下,改变0.1mol•L-1H2SO3溶液(SO2水溶液)的pH,溶液中的H2SO3、HSO3-、SO32-的物质的量分数δ(X)[δ(X)=
 ]随pH的变化如图所示:
]随pH的变化如图所示: 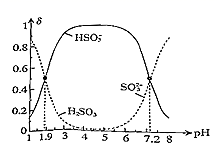
H2SO3的lgKa1=;反应HSO3-+OH-
 SO32-+H2O的lgK=;用0.100mol•L-1NaOH溶液滴入0.100mol•L-1H2SO3溶液(甲基橙作指示剂)中,溶液由红色变为橙色时,发生的主要反应的离子方程式为。
SO32-+H2O的lgK=;用0.100mol•L-1NaOH溶液滴入0.100mol•L-1H2SO3溶液(甲基橙作指示剂)中,溶液由红色变为橙色时,发生的主要反应的离子方程式为。
| | | | |
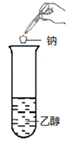
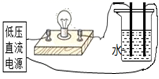
| A.少量二氧化硫通入氯化钡溶液中,产生白色沉淀亚硫酸钡 | B.在新制Cu(OH)2悬浊液中加入少量的葡萄糖,加热,产生砖红色沉淀 | C.将少量钠投入到无水乙醇中,钠表面有气泡产生 | D.在盛水的烧杯中加入氯化钠固体,小灯泡会逐渐亮起来 |
下列说法错误的是( )
选项 | 劳动项目 | 化学知识 |
A | 自主探究:以油脂为原料制肥皂 | 油脂可发生皂化反应 |
B | 家务劳动:用白醋清洗水壶中的水垢 | 乙酸具有挥发性 |
C | 社区服务:用84消毒液对图书馆桌椅消毒 | 含氯消毒剂具有强氧化性 |
D | 学农活动:用厨余垃圾制肥料 | 厨余垃圾富含N、P、K等元素 |
-
(1) 1828年,德国化学家维勒(Friedrich Wohler)首次用加热的方法使无机物氰酸铵
 转化为有机化合物尿素
转化为有机化合物尿素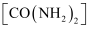 。已知氰酸铵在热水中就能发生分解,尿素加热至
。已知氰酸铵在热水中就能发生分解,尿素加热至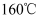 分解,分解时均产生氨气。
分解,分解时均产生氨气。①氰酸铵属于化合物(选填“离子”或“共价”)。
②鉴别氰酸铵和尿素的实验方法是。
-
(2) 液氨是富氢物质,是氢能的理想载体,利用合成氨可以实现储氢和输氢。合成氨时,在
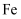 催化剂作用下的反应历程如下表(*表示吸附态):其中,
催化剂作用下的反应历程如下表(*表示吸附态):其中, 的吸附分解反应速率慢,决定了合成氨的整体反应速率。
的吸附分解反应速率慢,决定了合成氨的整体反应速率。化学吸附
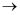
表面反应
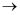
脱附
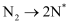

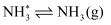
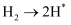


①采用液化空气分离的方法可获得原料气中
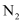 。先将空气液化后再汽化,液态空气汽化时首先分离出。
。先将空气液化后再汽化,液态空气汽化时首先分离出。②高温高压时,在催化剂作用下,已知
 参加反应生成
参加反应生成 放出
放出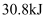 的热量。则合成氨的热化学方程式为。
的热量。则合成氨的热化学方程式为。③实际生产中,原料气中
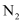 和
和 物质的量之比为1∶2.8。试分析说明原料气中
物质的量之比为1∶2.8。试分析说明原料气中 适度过量有利于提高整体反应速率的原因:。
适度过量有利于提高整体反应速率的原因:。 -
(3) 在低温,加压的条件下,氨气与二氧化碳可以合成尿素。试写出氨气与二氧化碳生成尿素和水的化学方程式:。
- 隋文帝是我国历史上非常有作为的君主,下列哪一项措施不属于隋文帝所为A.夺取北周政权,建立隋朝 B.灭掉
- 下列关于人类遗传病的叙述,错误的是( ) ①一个家族仅一代人中出现过的疾病不是遗传病 ②一个家族几代人中都出现过
- 10.依次填入下面一段文字横线处的语句,衔接最恰当的一组是( )(3分) 最近,一个名叫“酒店控”的终端在APPS
- 如图,竖直环A半径为r,固定在木板B上,木板B放在水平地面上,B的左右两侧各有一档板固定在地上,B不能左右运动,在环的最
- 在△ABC中,AC=3,∠A=,点D满足=2,且AD=,则BC的长为.
- ―Hello! May I speak to Jack,please? ―Yes.speaking. ―Oh,
- People willlive ______ 200 years old in the future. A.
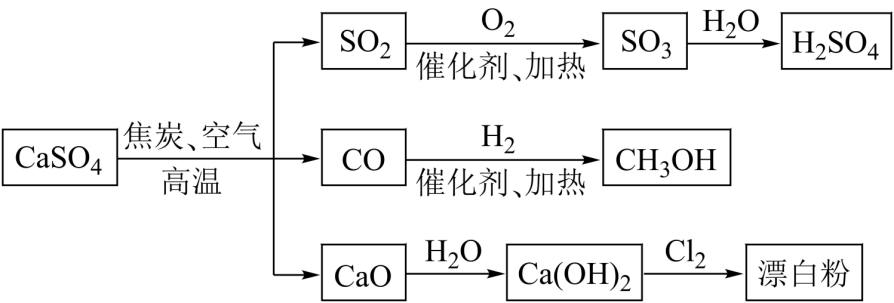
- 硫酸是化工生产中重要的酸,其产量最大,用途最广,消耗量最多。历史上曾将硫酸的产量或消耗量作为一个国家化工生产发达程度的标
- –Could you clean the living room, Tom? –OK, but I have to __
- 正确的操作能保证实验顺利进行。下列实验操作正确的是( ) A.配制稀硫酸时,将水沿量筒壁慢慢注入浓硫酸中,并不断搅拌
- 将同体积同物质的量浓度的NaCl、MgCl2、AlCl3三种溶液中的Cl-完全沉淀,则需同物质的量浓度的AgNO3溶液的
- (2012年四川资阳) 云南松怕冷的秘密(10分) 罗红里 既为“岁寒三友”之一,松树当然是不怕冷的了。没想到云南二月的
- 光污染已成为人们关注的问题。据测定,室内洁白、平滑墙壁能将照射在墙壁上的太阳光80%反射,在这样刺眼的环境中看书学习会感
- 人口再生产类型由传统型向过渡型转变开始的标志是( ) A.死亡率快速下降,出生率基本不变 B.死亡率和出
- 下列相关卤素的叙述正确的是 A.卤素离子(X-)只有还原性而无氧化性 B.某元素由化合态变成游离态,该元素一定被氧化 C
- 如图,火车厢中有一倾角的斜面,当火车以10m/s2的加速度沿水平方向向左加速运动时,斜面上的物体m还是与车厢相对静止,m
- 2.《荀子·儒效篇》记载:“(周公)兼制天下,立七十一国,姬姓(周王姓姬)独居五十三、”这段材料说明西周分封制中分封的
- 在做“叶绿体色素的提取和分离”实验过程中,研磨绿叶时,加入少许CaCO3的目的是: A.使研磨更加充分
- 18.下列绘画作品中,能够反映宋代市民生活的是 A.《女史箴图》 B.《送子天王图》C.《清明上河图
- 下列能证明氯化氢是共价化合物的实验事实是 A.氯化氢不易分解