第1节 元素与物质分类 知识点题库
工业上将相同物质的量的NaCl、CO2、NH3在30℃时配成溶液,此时溶液中无晶体。当降温至某温度时,开始析出晶体,此晶体是( )
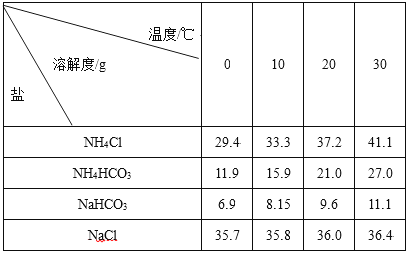
A . NH4Cl
B . NH4HCO3
C . NaHCO3
D . NaCl
下列说法正确的是( )
①Na2O,Fe2O3、Al2O3属于碱性氧化物,CO2、SO2、NO2都能和碱溶液发生反应属于酸性氧化物
②碳酸钠、氢氧化钡、氯化铵、过氧化钠都属于离子化合物
③蔗糖、硝酸钾和硫酸钡分别属于非电解质、强电解质和弱电解质
④醋酸、烧碱、纯碱和生石灰分别属于酸、碱、盐和氧化物
⑤NaHCO3是发酵粉主要成分之一,Na2CO3可冶疗胃酸过多.
⑥盐酸属于混合物,而液氯、冰醋酸均属于纯净物.
A . ①③⑤
B . ④⑤⑥
C . ②③④
D . ②④⑥
下列关于胶体和溶液的说法中,正确的是( )
A . 许多胶体能进行电泳是因为这些胶体带电
B . 布朗运动是胶体粒子特有的运动方式,可以据此把胶体与溶液、悬浊液区分
C . 光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应
D . 将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体
下列事实与胶体性质无关的是( )
A . 向豆浆中加入硫酸钙做豆腐
B . 将植物油倒入水中用力搅拌形成油水混合物
C . 利用丁达尔效应可以区别溶液与胶体
D . 观看电影时,从放映机到银幕有明显的光路
下列物质的分类合理的是( )
A . 酸:HNO3、H2SO4、NaHSO4、HCl
B . 碱性氧化物:CuO、Na2O、CaO、MgO
C . 胶体:牛奶、豆浆、碘酒、氢氧化铝
D . 酸性氧化物:CO2、NO、SiO2、SO3
下列物质按照纯净物、混合物、强电解质、弱电解质和非电解质顺序排列的是( )
A . 纯盐酸X、Y、水煤气、硫酸、醋酸、干冰
B . 冰醋酸、福尔马林、硫酸钡、氢氟酸、氯气
C . 单甘油脂、混甘油脂、苛性钾、氢硫酸、三氧化硫
D . 胆矾、漂白粉、氯化钾、次氯酸、乙醇
既能与稀硫酸反应,又能与NaOH溶液反应,且都有气体放出的是( )
A . NaHCO3
B . Al(OH)3
C . Al
D . Al2O3
下列逻辑关系图示中正确的是( )
A . 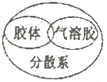 B .
B .  C .
C .  D .
D . 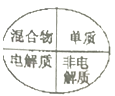
 B .
B .  C .
C .  D .
D . 
甲、乙、丙、丁分别是Al2(SO4)3、FeCl2、NaOH、BaCl2四种物质中的一种。若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,丁溶液滴入甲溶液时,无明显现象发生。据此可推断丙物质是( )
A . Al2(SO4)3
B . NaOH
C . BaCl2
D . FeCl2
有一种星际分子,其分子结构模型如图所示(图中球与球之间的连线代表化学键,如单键、双键、三键等,不同花纹的球表示不同的原子)。对该物质判断正确的是()
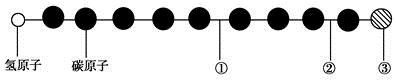
A . ①处的化学键是碳碳双键
B . 该物质是烃的含氧衍生物
C . ③处的原子可能是氯原子或氟原子
D . ②处的化学键是碳碳单键
下列关于胶体的说法错误的是()
A . 雾、豆浆、淀粉溶液属于胶体
B . 胶体、溶液和浊液这三种分散系的根本区别是分散质粒子直径的大小
C . 胶体微粒不能透过滤纸
D . 在25 mL沸水中逐滴加入2 mL FeCl3饱和溶液,继续煮沸可得Fe(OH)3胶体
朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来
的,高处丛生的灌木,落下参差的斑驳黑影……”这段美文中包含的化学知识正确的是( )
A . 荷塘上方的薄雾是水蒸汽
B . 薄雾中的微粒直径大约是2.5pM
C . 月光通过薄雾产生了丁达尔效应
D . “大漠孤烟直”中的孤烟成分和这种薄雾的成分相同
下列关于氯化铁溶液和氢氧化铁胶体的说法中,正确的是( )
A . 分散质的粒子直径均在1~100nm之间
B . 两者都具有丁达尔效应
C . 后者可用于净水
D . 前者是混合物,后者是纯净物
关于一些重要的化学概念有下列说法,其中正确的是( )
①Fe(OH)3胶体和CuSO4溶液都是混合物 ②BaSO4是一种难溶于水的强电解质 ③冰醋酸、纯碱、小苏打分别属于酸、碱、盐 ④煤的干馏、煤的气化和液化都属于化学变化 ⑤置换反应都属于离子反应
A . ①②⑤
B . ①②④
C . ②③④
D . ③④⑤
下列关于胶体的叙述正确的是( )
A . 胶体区别于其他分散系的本质特征是分散质粒子直径的大小
B . 光线透过溶液和胶体时,均可发生丁达尔效应
C . FeCl3溶液和Fe(OH)3胶体均是红褐色液体
D . 可以通过过滤的方法分离FeCl3溶液和Fe(OH)3胶体
现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
I、甲同学向氯化铁溶液中加入少量的NaOH溶液;
II、乙同学向沸水中滴加饱和氯化铁溶液后,长时间加热;
III、丙同学向25 ml沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
-
(1) 其中操作正确的同学是;他的操作中涉及到的制备胶体的离子反应方程式为。
-
(2) 判断胶体制备是否成功,可利用胶体的。
-
(3) 丁同学将所制得的Fe(OH)3胶体分成两份,并进行下列实验:
①将其中一份装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明。
②向另一份Fe(OH)3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化。
a. 先出现红褐色沉淀,原因是。
b. 随后沉淀溶解,此反应的离子方程式是。
下列分散系能产生“丁达尔效应”的是( )
A . 泥水
B . 氯化铜溶液
C . 溴蒸汽
D . 淀粉溶液
下列说法错误的是( )
A . 利用丁达尔效应鉴别氢氧化铁胶体和氯化镁溶液
B . 在食品包装袋内放入铁系保鲜剂可以防止食品因氧化而变质
C . 硫黄在过量空气中燃烧生成SO3
D . 工业上可用氨水消除燃煤烟气中的二氧化硫
-
(1) 现有10种物质:①稀硝酸 ②Cu ③CaO ④CO2 ⑤CuSO4·5H2O ⑥空气 ⑦C2H5OH ⑧H2O ⑨Ba(OH)2 ⑩蔗糖,其中属于混合物的是(填序号,下同);属于有机物的是;属于电解质的是;属于非电解质的是。
-
(2) 实验室若配制0.5 mol/L的硫酸溶液460 mL。
①需用量筒量取质量分数98%、密度1.84 g/cm3浓硫酸的体积为。
②除用到量筒、烧杯、玻璃棒外,还需要的两种玻璃仪器是。
③下面操作造成所配硫酸溶液浓度偏高的是。
A.浓硫酸稀释后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.定容时俯视刻度线
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
下列叙述中正确的是( )
A . 铁锈的主要成分是 , 能保护内层金属不被腐蚀
B .
, 能保护内层金属不被腐蚀
B . 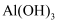 是两性氢氧化物,可溶于强酸或强碱溶液
C . 白色
是两性氢氧化物,可溶于强酸或强碱溶液
C . 白色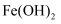 在空气中加热分解生成
在空气中加热分解生成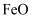 D . 维生素C能将
D . 维生素C能将 转化成
转化成 , 这体现了维生素C的氧化性
, 这体现了维生素C的氧化性
 , 能保护内层金属不被腐蚀
B .
, 能保护内层金属不被腐蚀
B . 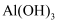 是两性氢氧化物,可溶于强酸或强碱溶液
C . 白色
是两性氢氧化物,可溶于强酸或强碱溶液
C . 白色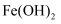 在空气中加热分解生成
在空气中加热分解生成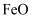 D . 维生素C能将
D . 维生素C能将 转化成
转化成 , 这体现了维生素C的氧化性
, 这体现了维生素C的氧化性
最近更新
- 自然界中种群增长常表现为“S”型曲线。下列有关“S”型曲线的正确叙述是 A.“S”型曲线表示了种群数量和食物的关系 B.
- 小军同学的姐姐是百色市某旅行社的导游员,姐姐的下列行为合理的是( ) A.带旅游团到田阳敢壮山参观黑衣壮风情园 B.
- 目前工业上利用甲烷催化裂解生产不含一氧化碳和二氧化碳的清洁氢气。该过程多用铁、钴和镍等过渡金属纳米催化剂:CH4(g)C
- 芜湖市繁昌窑被称为中国青白瓷的发源地。在陶瓷器制造过程中,一定发生了化学变化的是() A.混合
- 观察下列图片,从图一到图三的变化主要说明了( )A.夏商周时期的主要农具是末耜 B.
- 可用推拉注射器栓塞的方法检查右图装置的气密性.当缓慢 推活塞时,如果装置气密性好,可观察到( )
- 下列离子方程式书写正确的是() A.碳酸钙溶于醋酸:CaCO3+2H+=Ca2++H2O+CO2↑ B.
- 设实数x,y满足 ,则的取值范围是()A.B.C.D.
- 已知的三个内角满足: ,则的形状为( ) A.正三角形
- 这种布料摸起来很舒服。 ________________________________________
- “时空之旅”飞车表演时,演员驾着摩托车,在球形金属网内壁上下盘旋,令人惊叹不已,摩托车沿图示竖直轨道做圆周运动的过程中
- 依据人口分布的特征,可知下列四大地形区人口最稠密的是 A.亚马孙平原 B.撒哈拉沙漠 C.青藏高原
- 下列关于摩尔的说法中,正确的是() A.摩尔是表示物质质量的单位B.摩尔是国际单位制的七个基本物理量之一C.摩尔既是物质
- 阅读下面这首唐诗,然后回答问题。(8分)又呈吴郎杜甫堂前扑枣任西邻,无食无儿一妇人。不为困究宁有此,只缘恐惧转须亲。即防
- It is foggy today. Theplane can't . A. land
- Van Gogh succeeded in selling only onepainting in his lifet
- 有同学想要了解美国联邦体制确立之初的情况,你可以建议他去查阅( )A.《权利法案》
- 甲醇(CH3OH)有毒,误饮可使眼睛失明,甚至死亡。最新研究证明用氨气(NH3)处理含有甲醇的工业废水,可转变为无毒的物
- 关于燃料的热值,以下说法中正确的是 A.燃料的热值与燃料的种类有关系,与燃料的质量和燃烧状况无关 B.燃烧1千克某
- 2011年9月29日,我国成功将无人太空实验舱“ ”送入低地球轨道,为建设永久载人空间站迈出关键一步。A.神州七



