第3节 化学中常用的物理量——物质的量 知识点题库
已知:还原性强弱:I﹣>Fe2+ . 往100mL碘化亚铁溶液中缓慢通入2.24L(标准状况)氯气,反应完成后溶液中有一半的Fe2+被氧化成Fe3+ . 则原碘化亚铁溶液的物质的量浓度为( )
A . 0.6 mol•L﹣1
B . 0.8 mol•L﹣1
C . 1.0 mol•L﹣1
D . 1.2 mol•L﹣1
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A . 常温常压下,8g O2含有4NA个电子
B . 1L 0.1mol•L﹣1的氨水中有NA个NH4+
C . 标准状况下,22.4L盐酸含有NA个HCl分子
D . 1mol Na被完全氧化生成Na2O2 , 失去2NA个电子
设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A . 7.8 g Na2O2与足量水反应转移的电子数为0.1NA
B . 常温常压下,22.4LCH4中含有的氢原子数为4NA
C . 5.6 g铁粉与硝酸反应失去的电子数一定为0.2NA
D . 12.0 g熔融的NaHSO4中含有0.1NA个Na+、0.1NA个H+和0.1NA个SO42﹣
如图所示,①和②为两个体积相同的固定容器,图中“○”和“●”分别表示氢原子和氧原子,则下列说法正确的是( )
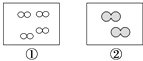
A . 若①中的H2为1 mol,则②中所含原子总数为3.01×1023个
B . ①和②中气体的质量之比为1:8
C . H2、O2均能发生化合反应,但不能发生置换反应
D . 两容器的温度和压强均相同
据报道,科学家已成功合成了少量N4 , 有关N4的说法正确的是( )
A . N4是N2的同素异形体
B . N4是N2的同分异构体
C . 相同质量的N4和N2所含原子个数比为1:2
D . N4的摩尔质量是56g
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A . 0.1 mol•L﹣1醋酸溶液中含有醋酸分子的数目为0.1NA
B . 25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.2 NA
C . 常温下,20 L pH=12的Na2CO3溶液中含有OH﹣数目为0.2 NA
D . 某密闭容器盛有0.1 mol N2和0.3 mol H2 , 在一定条件下充分反应,转移电子数目为0.6 NA
设 NA为阿伏加德罗常数的值,下列叙述正确的是( )
A . 标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5 NA
B . 常温常压下,7.0 g乙烯与丙烯的混合物中含有氢原子的数目为 NA
C . 50 mL 18.4 mol•L﹣1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46 NA
D . 密闭容器盛有0.1 mol N2和0.3 mol H2 , 在一定条件下充分反应,转移电子的数目为0.6 NA
NA代表阿伏加德罗常数的值,下列叙述正确的是( )
A . 标准状况下,1.12 L CCl4含有质子数的数目为3.7NA
B . 常温常压下,3.0 g含葡萄糖的冰醋酸中含有的原子总数为0.4NA
C . 常温时,56g Fe与足量浓硝酸反应,转移的电子数目为3NA
D . 晶体B的结构单元如右图 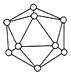 ,则11g晶体B含有0.6NA个三角形(相邻原子构成)
,则11g晶体B含有0.6NA个三角形(相邻原子构成)
 ,则11g晶体B含有0.6NA个三角形(相邻原子构成)
,则11g晶体B含有0.6NA个三角形(相邻原子构成)
相同物质的量的N2和CO两者相比较,下列说法错误的是( )
A . 所占的体积一定相等
B . 所含原子总数相等
C . 所含电子总数相等
D . 所含分子数相等
NA代表阿伏加德罗常数的值。下列说法正确的是( )
A . 常温常压下,36g18O2中所含的中子数为16NA
B . 8.0 g Cu2S和CuO的混合物中含有的铜原子数为0.1NA
C . 电解饱和食盐水时,阳极生成22.4L气体时,转移的电子数为2NA
D . 室温下向1LpH=1的醋酸溶液中加水,所得溶液中H+数目小于0.1NA
空气中的自由电子附着在分子或原子上形成空气负离子,被称为“空气维生素”。 O2-就是一种空气负离子,其摩尔质量为( )
A . 33 g
B . 32g
C . 33 g·mol-1
D . 32g·mol-1
实验室中需要配制1mol/L的H2SO4溶液980mL,应选用容量瓶的规格和量取密度为1.84g/mL,质量分数为98%的浓硫酸的体积分别是( )
A . 980mL,53.3mL
B . 1000mL,54.30mL
C . 1000mL,54.3mL
D . 980mL,53.30g
NA表示阿伏加德罗常数的值。下列说法正确的是( )
A . 32gO2中含有的电子数为16NA
B . 标准状况下,22.4 L H2O中含有的分子数为NA
C . 2.3g Na与100 mL 0.1mol·L-1盐酸反应,转移的电子数为0.01NA
D . 1L 1 mol·L-1 CaCl2溶液中含有的氯离子数为NA
NA为阿伏加德罗常数,下列叙述错误的是( )
A . 18 g H2O中含有的质子数为10NA
B . 12 g金刚石中含有的共价键数为4NA
C . 46 g NO2和N2O4混合气体中含有原子总数为3NA
D . 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
工业上用黄铁矿(FeS2)为原料制备硫酸的流程如下:

-
(1) 沸腾炉中发生反应的化学方程式为4FeS2+11O2
 2Fe2O3+8SO2 , 该反应被氧化的元素是(填元素名称)。
2Fe2O3+8SO2 , 该反应被氧化的元素是(填元素名称)。
-
(2) 利用Fe2O3废渣(俗称“红砂”)制备废水除砷剂的第一步是将“红砂”与硫酸混合,该步反应的化学方程式为。
-
(3) 从接触室出来的混合气体中含有SO2、SO3、O2、N2等气体,设计一个实验方案证明其中含有SO2:。
-
(4) 有些反应中物质浓度不同,性质也不同。浓硫酸有三大特性:吸水性、脱水性、强氧化性。则加热时浓硫酸与木炭反应的化学方程式为。
-
(5) 将一定量锌与100mL18mol/L 浓硫酸充分反应后,若锌完全溶解同时产生气体0.8mol, 将反应后的溶液稀释得400mL,测得c(H+)=2mol/L,则产生气体中SO2 物质的量为mol。
为应对气候变化,我国提出“二氧化碳排放力争于2030年前达到峰值”等庄严的承诺。下列说法错误的是( )
A . CO2溶于水能导电,故CO2是电解质
B . 在标准状况下,1molCO2气体的体积约为22.4L
C . 金属钠着火不能使用泡沫灭火器或者二氧化碳灭火器
D . 大力发展太阳能、风能、核能、氢能等新能源,可以构建绿色低碳的能源体系
室温下过氧化铬( )在硝酸酸化的戊醇中会溶解并发生反应:
)在硝酸酸化的戊醇中会溶解并发生反应:
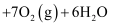 。在5m1
。在5m1 的过氧化铬戊醇溶液中滴入一定量的稀硝酸,在不同时刻测得过氧化铬浓度如下表:
的过氧化铬戊醇溶液中滴入一定量的稀硝酸,在不同时刻测得过氧化铬浓度如下表:
 )在硝酸酸化的戊醇中会溶解并发生反应:
)在硝酸酸化的戊醇中会溶解并发生反应:
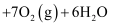 。在5m1
。在5m1 的过氧化铬戊醇溶液中滴入一定量的稀硝酸,在不同时刻测得过氧化铬浓度如下表:
的过氧化铬戊醇溶液中滴入一定量的稀硝酸,在不同时刻测得过氧化铬浓度如下表:
|
时间/min |
4 |
6 |
8 |
10 |
t |
20 |
25 |
35 |
|
|
4.230 |
2.510 |
1.790 |
1.350 |
1.240 |
1.130 |
1.110 |
1.100 |
下列叙述正确的是( )
A . 4~6min内过氧化铬分解的平均速率 B . 8~10min内过氧化铬分解释放的
B . 8~10min内过氧化铬分解释放的 体积为0.86mL(标准状况)
C . 推测表中t的取值范围为:10<15
D . 若升高温度后重新实验发现20min时过氧化铬浓度为
体积为0.86mL(标准状况)
C . 推测表中t的取值范围为:10<15
D . 若升高温度后重新实验发现20min时过氧化铬浓度为 , 则证明反应的△H>0
, 则证明反应的△H>0
 B . 8~10min内过氧化铬分解释放的
B . 8~10min内过氧化铬分解释放的 体积为0.86mL(标准状况)
C . 推测表中t的取值范围为:10<15
D . 若升高温度后重新实验发现20min时过氧化铬浓度为
体积为0.86mL(标准状况)
C . 推测表中t的取值范围为:10<15
D . 若升高温度后重新实验发现20min时过氧化铬浓度为 , 则证明反应的△H>0
, 则证明反应的△H>0
化学与人类生活、生产和社会可持续发展密切相关,请回答下列问题。
-
(1) Ⅰ春秋末期工艺官书《考工记》中记载有“涑帛”的方法,即利用含有碳酸钠的水溶液来洗涤丝帛。
请写出碳酸钠水溶液中通入
 气体的化学方程式。
气体的化学方程式。 -
(2) 用
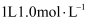 的
的 溶液吸收
溶液吸收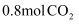 , 所得溶液中
, 所得溶液中 和
和 物质的量浓度之比为。
物质的量浓度之比为。
-
(3) Ⅱ.如图为铁及其化合物的“价一类”二维图。
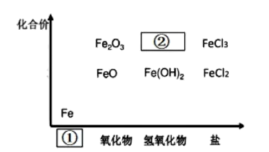
图中①处填,②处填。
-
(4) 某小组在探究
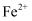 性质的实验(实验1)时,观察到溶液变红,片刻红色褪去,有气体生成。
性质的实验(实验1)时,观察到溶液变红,片刻红色褪去,有气体生成。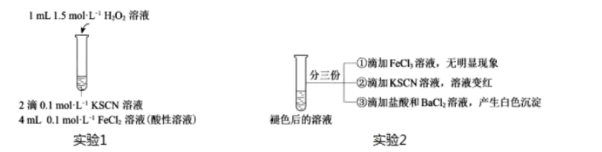
用实验2探究“红色褪去”的原因,则红色褪去的原因是。
下列物理量单位不正确的是( )
A . 物质的量:mol
B . 摩尔质量:g·mol-1
C . 阿伏加德罗常数:mol-1
D . 气体摩尔体积:mol·L-1
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和 的混合气体,这些气体与
的混合气体,这些气体与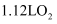 (标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入
(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入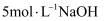 溶液至
溶液至 恰好完全沉淀,则消耗
恰好完全沉淀,则消耗 溶液的体积是( )
溶液的体积是( )
 的混合气体,这些气体与
的混合气体,这些气体与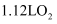 (标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入
(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入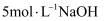 溶液至
溶液至 恰好完全沉淀,则消耗
恰好完全沉淀,则消耗 溶液的体积是( )
溶液的体积是( )
A . 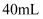 B .
B . 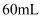 C .
C . 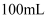 D .
D . 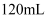
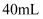 B .
B . 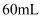 C .
C . 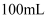 D .
D . 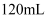
最近更新
- We all know that, __________, the situation will get worse.
- 我国少数民族主要分布在() A、华北、西北、东北 B、西北、西南、东北C、西北、西南、东南 D、华东、华南、华中
- 仔细研读2010年的政府工作报告我们会发现,在“监督”一词的运用上与2009年有许多不同。主要表现在立意和表达意义的层面
- 以下物质的性质属于化学性质的是() A.氧气能助燃 B.食盐
- The price was _____ within the reach of the average househol
- 函数的自变量的取值范围是() A. B. C. D. 且
- 如图所示,可见光光子的能量范围约为,一群氨原子从n=4激发态跃迁到基态的过程中( )A.可以产生射线 B.可以产生
- 我国著名科学家王选因发明汉字激光照排技术大大提高印刷效率而被誉为“当代毕升”。那么,历史上毕升的发明是( )。A.活
- Iknow____ of those people in the room, so I left. A.
- 下列生理活动中与生物膜无直接关联的是 ( ) A.单克隆抗体的分泌过程 B.有氧呼吸
- 古诗文默写填空 (1) ,青山郭外斜。 (2)山重水复疑无路,
- 某女子是白化病基因携带者(Aa),有可能不含该病基因的细胞是 A.肌细胞 B.神经细胞 C.卵细
- 纪念全国人民代表大会成立50周年的隆重集会上强调:人民代表大会制度是我国的根本政治制度,这是我党把马克思主义基本原理同中
- 下列句子标点使用有错误的一项是 A.读书足以怡情,足以傅彩,足以长才。其怡情也,最见于独处幽居之时;其傅彩也,
- 下列现象一定是化学变化的是( ) A.瓷碗破碎 B.酒精挥发 C.石蜡熔化
- 下面两个句子各有一处给语病,在不改变原意的基础上,将改正后的句子写在原句的下面。(2分)(1)发扬并继承中华民族的优秀文
- 目前在学生的日常学习中,抄袭作业已是一种普遍的现象。上周北海某中学就此现象召开了主题班会。班会上,老师和学生就作业布置的
- I shall never beat John at tennis; we are clearly not in the
- As a solo artist, Brightman has sold 26 million albums and t
- 过双曲线的一个焦点F作一条渐近线的垂线,若垂足恰在线段(为原点)的垂直平分线上,则双曲线的离心率为_______