第3节 化学中常用的物理量——物质的量 知识点题库
 称量
B .
称量
B .  转移
D .
转移
D . 已知1 mol不同气体在不同条件下的体积.
化学式 | 条件 | 1mol气体体积 |
H2 | 0℃,101kPa | 22.4 |
O2 | 0℃,101kPa | 22.4 |
CO | 0℃,101kPa | 22.4 |
H2 | 0℃,202kPa | 11.2 |
CO2 | 0℃,202kPa | 11.2 |
N2 | 273℃,202kPa | 22.4 |
NH3 | 273℃,202kPa | 22.4 |
-
(1) 从上表分析得出的结论:①1 mol任何气体在标准状况下的体积都约为.
②1 mol不同的气体,在不同的条件下,体积(填“一定”、“一定不”或“不一定”)相等.
-
(2) 理论依据:相同条件下,1mol任何气体的体积几乎相等,原因是:①,②.
-
(3) 应用:在标准状况下,48g O3的体积为多少升?(写出计算过程)
-
(1) 电解之前,食盐水需要精制,目的是除去粗盐的中的Ca2+、Mg2+、SO42-等杂质离子,使用的试剂有:①Na2CO3溶液 ②Ba(OH)2溶液 ③稀盐酸。其中合理的加入顺序为 (填序号);
-
(2) 实验室欲配制6.00 mol/L的食盐水90 mL,回答下列问题:
①需要纯净的NaClg。
②可供选择的仪器有:a玻璃棒 b烧瓶 c烧杯 d胶头滴管 e试管 f托盘天平、砝码 h药匙。在配制食盐水时不需要使用的有(填字母),还缺少的仪器是。
③配制溶液时,一般可以分为以下几个步骤:计算®称量®溶解()转移()定容()装瓶。
④下列操作会使所配溶液的浓度偏小的是。
A. 转移完溶液后未洗涤玻璃棒和烧杯
B. 容量瓶中原来有少量蒸馏水
C. 定容时,俯视刻度线
D. 称量氯化钠固体时左码右物
-
(3) 在电解饱和食盐水过程中,还生成了H2和NaOH,则所发生反应的化学反应方程式为;
-
(4) 将电解生成的Cl2通入NaOH溶液,生成两种盐,其中一种是消毒液的主要成分NaClO,应用氧化还原反应原理,写出此反应的化学方程式是。
 的
的  落液时,定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度
C . 分液时,分液漏斗中下层液体从下口放出,上层液体从上口例出
D . 蒸馏时,加入几粒沸石是为了防止暴沸
落液时,定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度
C . 分液时,分液漏斗中下层液体从下口放出,上层液体从上口例出
D . 蒸馏时,加入几粒沸石是为了防止暴沸
-
(1) 反应中生成的H2在标准状况下的体积。
-
(2) 所用盐酸中HCl的物质的量浓度。
-
(3) 需用多少体积的36.5%的浓盐酸(ρ =1.20 g/mL)来配置上述盐酸。
-
(1) 稀硝酸的物质的量浓度是 mol·L−1
-
(2) 气体A中若含有H2 , 则W的值一定要大于g.
 表示阿伏加德罗常数的值,下列判断正确的是( )
表示阿伏加德罗常数的值,下列判断正确的是( )
 含有的氮原子数目为
含有的氮原子数目为  B . 常温常压下,
B . 常温常压下, 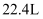
 含有的分子数目为
含有的分子数目为  C .
C .  溶液中含有的钾离子数目为
溶液中含有的钾离子数目为  D . 在标准状况下,
D . 在标准状况下, 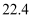 LCO和
LCO和  的混合物的物质的量为1mol
的混合物的物质的量为1mol
A.容量瓶用蒸馏水洗后未加干燥
B.量筒用蒸馏水洗后未干燥
C.将烧杯中浓盐酸移入容量瓶后,未用水洗涤烧杯和玻璃棒,即向容量瓶中加水到刻度
D.用胶头滴管向容量瓶中加水时,不慎超过刻度线,用另外胶头滴管从瓶中吸出部分溶液使剩余溶液刚好达刻度线
E.定容时,俯视液面加水至刻度线
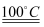 Si3N4+N2↑+3H2↑,每生成1 mol N2 ,转移的电子数为6 NA
C . 8.8 g乙酸乙酯在稀硫酸的作用下充分水解,生成的乙醇的分子数为0.1 NA
D . 用C将6.0g SiO2完全还原为单质Si,生成的CO2的分子数为0.1 NA
Si3N4+N2↑+3H2↑,每生成1 mol N2 ,转移的电子数为6 NA
C . 8.8 g乙酸乙酯在稀硫酸的作用下充分水解,生成的乙醇的分子数为0.1 NA
D . 用C将6.0g SiO2完全还原为单质Si,生成的CO2的分子数为0.1 NA
-
(1) 生成氮气的质量;
-
(2) 已知该物质是一种铵盐,通过计算确定其化学式;
-
(3) 若0.4mol的该铵盐分解,计算被氮元素还原的氯元素原子的物质的量。
| 选项 | 实验目的 | 实验操作 |
| A | 探究浓度对反应速率的影响 | 向2支各盛有4mL0.01mol·L-1KMnO4酸性溶液的试管中,分别加入2mL0.1mol·L-1H2C2O4溶液和2mL0.2mol·L-1H2C2O4溶液,记录溶液褪色所需的时间 |
| B | 配制1.00mol·L-1的NaOH溶液 | 称取4.0g固体NaOH于烧杯中,加入少量蒸馏水溶解,然后转移至100mL容量瓶中定容 |
| C | 探究固体表面积对反应速率的影响 | 称取相同质量的大理石和纯碱,加入到盛有浓度、体积均相同的盐酸的小烧杯中,观察实验现象 |
| D | 探究淀粉溶液在稀硫酸和加热条件下是否水解 | 取少量的水解液于试管中,先加适量的NaOH溶液,再滴入碘水,观察实验现象 |
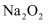 反应,转移电子数为NA
C . 常温下,1LpH=1的
反应,转移电子数为NA
C . 常温下,1LpH=1的 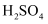 溶液中氧原子数为2NA
D . 标况下,22.4L
溶液中氧原子数为2NA
D . 标况下,22.4L 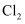 溶于水所得溶液中,
溶于水所得溶液中, 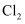 、Cl-、HClO和ClO-微粒总数为2NA
、Cl-、HClO和ClO-微粒总数为2NA
- 2015年诺贝尔化学奖得主托马斯·林达尔最初从事RNA的研究。他研究时发现,RNA极不稳定,遇热就分解,实验无法进行下
- 将1.95gNa2SO4和Na2CO3的混合物溶于水得溶液A,在A中加入足量未知浓度的BaCl2溶液10.0mL,然后过
- 哺乳动物体外受精的过程是( ) ①采卵 ②收集精子 ③卵母细胞的人工培养 ④精子获能处理 ⑤精子和成熟卵子
- 近年来,道德现象高频“出镜”。一方面表现为媒体对道德问题的关注度和民众对道德失范的痛恨度“居高不下”;一方面表现为一批批
- 某市中考化学实验操作考试有四道题:①酸的化学性质;②粗盐提纯;③CO2的制取,收集和验满;④配制一定溶质质量分数的溶液.
- 相同体积、相同氢离子浓度的强酸溶液和弱酸溶液分别跟足量的镁完全反 应,下列说法正确的是() A.弱酸溶液产生较多的氢气
- (6分)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生电化学腐蚀,一段时间后某极产生3.36 L(标准状况)
- 图中阴影部分的点满足不等式组.在这些点中,使目标函数K=6x+8y取得最大值的点的坐标是 .
- 下列哪一项说法是错误的() A.酶的活性是指酶催化一定化学反应的能力 B.温度、pH和酶的抑制剂等条件会影响果胶酶的活性
- 如图15-3-9所示,匀强磁场中有一通以方向如图的稳恒电流的矩形线圈abcd,可绕其中心轴OO′转动,则在转动过程中(
- 伴随我国民主政治的不断完善,公民参与政治生活的热情也不断高涨。在我国的政治生活中,公民参与管理国家和管理社会的基础和标志
- (7分)王羲之尝诣门生家,见棐几①滑净,因书之,真草②相半。后为其父误刮去之,门生惊懊者累日。又尝在蕺山③见一老姥④,持
- 已知:(1)两分子乙酸分子间脱水可形成乙酸酐: (2)HO—CH2—CH=CH—CH2—OH氧化时分子中的碳碳双键会被同
- 2012年5月18日第七届“中博会”在湖南举行,5月17日在长沙举行了盛大的焰火晚会,璀璨夺目的焰火震撼全场,长沙市民深
- When someone steps on your toe by accident, you will hurt pl
- 从辽代到清代,北京古城区城址不断变迁的原因是( ) A.城市空间不断扩展 B
- A、B、C、D是四种可溶的化合物,分别由阳离子K+、Ba2+、A3+、Fe3+和阴离子OH-、、、两两组合而成,它们的溶
- 根据下面材料所提供的信息,拟一条一句话新闻。不超过20个字。 早在2月16日,作为我国新型航天测控网重要组成部分的“远望
- (05广东卷)SARS病原体是一种冠状病毒,其遗传物质是一条单链RNA,下列关于SARS病毒的叙述中,正确的是A.可独立
- 在中,=a,=b,M为OB的中点,N为AB的中点,ON,AM交于点P,则=



