第一单元 含硫化合物的性质 知识点题库
-
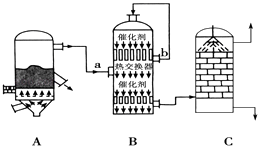
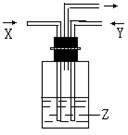
(1) 图中设备A的名称是,B设备气流a、b温度较高的是(填“a”或“b”).
-
(2) CuFeS2是黄铁矿的另一部分,煅烧时,CuFeS2转化为CuO、Fe2O3和SO2 , 该反应的化学方程式为:
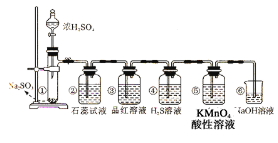
①品红溶液;②KMnO4酸性溶液;③氯水;④滴有酚酞的NaOH溶液.
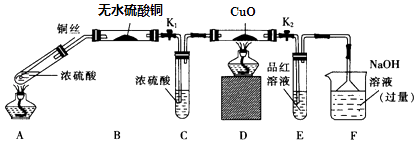
实验I:反应产物的定性探究﹣﹣按如图装置(固定装置已略)进行实验:
-
(1) F装置的烧杯中发生反应的离子方程式是;
-
(2) 实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是
-
(3) 实验结束时,撤去所有酒精灯之前必须完成的实验操作是
-
(4) 实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是
-
(5) 实验Ⅱ:反应产物的定量探究
在铜与浓硫酸反应的过程中,发现有黑色物质出现,且黑色物质为Cu2S.产生Cu2S的反应为aCu+bH2SO4
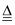 cCu2S+dCuSO4+e H2O,则a:b=
cCu2S+dCuSO4+e H2O,则a:b= -
(6) 为进一步探究该黑色物质的成分,经查阅相关文献获得下列资料.
资料1:
硫酸/mol•L﹣1
黑色物质出现的温度/℃
黑色物质消失的温度/℃
14
Cu 片表面无明显现象
15
约150
约236
16
约140
约250
18
约120
不消失
资料2:X﹣射线晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种.仅由上述资料可得出的如下结论中正确是 .
A . 铜与浓硫酸反应时所涉及的反应可能不止一个 B . 硫酸浓度选择适当,可避免最后产物中出现黑色物质 C . 该反应发生的条件之一是硫酸浓度≥15mol/L D . 硫酸浓度越大,黑色物质越快出现、越难消失.
-
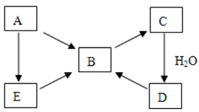
(1) 若A为固体,则D为。写出B→C的化学方程式,B的大量排放可能引起的大气污染问题为
-
(2) 若A为气体单质,则D为。写出E→B的化学方程式,C→D反应过程中氧化剂与还原剂的物质的量比为
| 反应室 | 载气 | 吸收液 | SO42-含量 | 数据分析 |
| ① | n2 | 蒸馏水 | a | i.b≈d>a≈c ii. 若起始不通入NO2 , 则最终测 不到SO42- |
| ② | 3%氨水 | b | ||
| ③ | 空气 | 蒸馏水 | c | |
| ④ | 3%氨水 | d |
-
(1) 在①中发生反应的化学方程式为。
-
(2) ②中的实验现象为紫色石蕊试液,此实验证明二氧化硫是气体。
-
(3) ③中的品红溶液,证明二氧化硫有性。
-
(4) ④中的实验现象是,证明二氧化硫有性。
-
(5) ⑤中的实验现象是,证明二氧化硫有性。
-
(6) ⑥的作用是,反应的化学方程式为。
-
(1) 硫酸铵是某地PM2.5雾霾的主要成分,收集一定量的雾霾固体进行验证。取一定量的雾霾固体于试管中,加入适量的水溶解,把溶液分成两份盛于试管中:
操作步骤
实验现象
结论
①向其中一份
有白色沉淀生成
证明雾霾固体中含有SO42-
②向另一份中加适量NaOH浓溶液并加热,用镊子夹持湿润的红色石蕊试纸靠近试管口
③试管中有气泡产生,靠近试管口的红色石蕊试纸
证明雾霾固体中含有NH4+。综合上面实验,初步说明雾霾固体颗粒中含有(NH4)2SO4
-
(2) 用如图所示简易装置测定空气中SO2的含量。
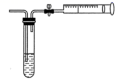
①测定原理:SO2通入碘的淀粉溶液中,溶液由蓝色变为无色,反应的化学方程式为。
②测定方法:在某监测点,量取5.0mL5.0×10-4mol/L的碘溶液,注入图中的试管中,加几滴淀粉指示剂,此时溶液呈蓝色,按图中装置连接好仪器,利用止水夹控制,进行抽气,取下注射器排气,重复操作直到溶液的蓝色全部褪尽为止,共抽取空气8.0L,则测得该监测点空气中SO2的含量为mg/L。
-
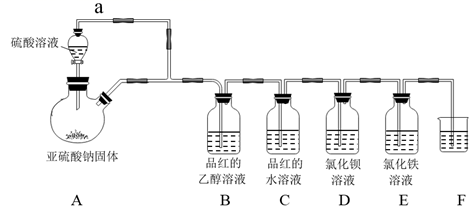
(3) 探究H2SO3的部分性质。选用下面的装置和药品探究H2SO3与HClO的酸性强弱。
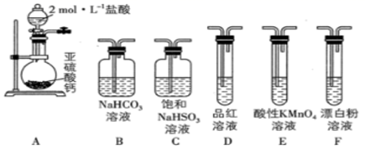
①甲同学认为按照A→C→F→尾气处理的顺序连接装置,可以证明H2SO3与HClO的酸性强弱,乙同学认为该方案不合理,其理由是。
②丙同学采用间接法证明,实验方案为按照A→C→→→→(填字母)→尾气处理顺序连接装置,证明H2SO3的酸性强于HClO的实验现象是。
 +2H2O
+2H2O
| X | Y | Z | |
| A | NO2 | SO2 | BaCl2 |
| B | NH3 | CO2 | Al2(SO4)3 |
| C | NH3 | CO2 | CaCl2 |
| D | CO2 | SO2 | CaCl2 |
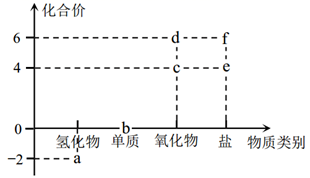
 微溶于酒精,易溶于
微溶于酒精,易溶于  B . 向
B . 向  的溶液中通入
的溶液中通入  ,可产生淡黄色沉淀
C . 滴加
,可产生淡黄色沉淀
C . 滴加  溶液,即可鉴别
溶液,即可鉴别 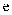 、
、 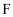 两种溶液
D . 在一定条件下,可实现
两种溶液
D . 在一定条件下,可实现 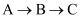 的转化
的转化
 与浓
与浓 反应的实验装置改进如图。下列说法错误的是( )
反应的实验装置改进如图。下列说法错误的是( )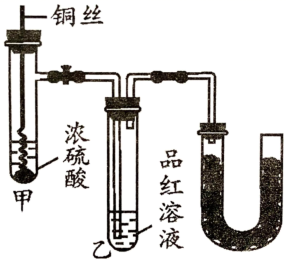
 B .
B . 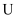 型管中可放置石灰,以吸收
型管中可放置石灰,以吸收 防止污染空气
C . 伸入或者上提铜丝,可以控制反应的发生和停止
D . 实验结束后,立即将
防止污染空气
C . 伸入或者上提铜丝,可以控制反应的发生和停止
D . 实验结束后,立即将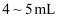 水加入试管甲,观察溶液颜色
水加入试管甲,观察溶液颜色
 的漂白性作抗氧化剂
B . 应用液氨汽化吸热作制冷剂
C . 应用二氧化硅的导电性作光导纤维
D . 应用乙酸的酸性制作乙酸乙酯
的漂白性作抗氧化剂
B . 应用液氨汽化吸热作制冷剂
C . 应用二氧化硅的导电性作光导纤维
D . 应用乙酸的酸性制作乙酸乙酯
- 正项等比数列{}中的a1、a11是函数f(x)=+6x-3的极值点,则 A.1 B.2
- 在一个描述花生的谜语中:“麻屋子,红帐子,里面住着白胖子。”谜语中没有的结构是()。 A.果皮 B.种皮 C.胚
- 依次填入下面一段文字序号处的标点符号,正确的一项是( ) 吕型伟先生说:“教育是事业,事业的意义在于奉献①教育是科
- 如图,—长为L的轻杆—端固定在光滑铰链上,另—端固定—质量为m的小球。一水平向右的拉力作用于杆的中点,使杆以角速度匀速转
- 已知定义在上的函数满足以下三个条件:对于任意的,都有;函数的图象关于轴对称;对于任意的,且,都有,则的大小关系_____
- 随着世界人口的急剧增长和工业的快速发展,淡水供应危机日益成为世界关注的焦点,海水约占地球现有总水量的97%,海水淡化问题
- 下列各句中,加点的词语使用不恰当的一项是( ) A.戴震辑录的《九章算术》,其功绩在于完整地恢复了这部数学经典著作
- Parents today also worry about their children’s diets. Some
- 下列不属于化学变化的是() A.二氧化硫在空气中造成酸雨 B.铜片在酒精灯上加热变黑 C.将石油加热分馏制成汽油、煤油、
- (2019·德州)下面是实验室常见的玻璃仪器,其中能够在酒精灯上直接加热的是 ()
- 2009年1月27日,我国第一个南极内陆科学考察站昆仑站在南极内陆冰盖的最高点冰穹-A(80°22′00″S,77°21
- 酸雨给人类生活和社会发展带来了严重危害。汽车尾气是导致酸雨的重要原因,为减少有害气体的排放,人们在汽车排气管上安装“催化
- 联合国气候变化框架公约《京都议定书》要求发达国家限制CO2等温室气体的排放量,以控制日趋严重的温室效应。 试回答下列问题
- 对于惯性的大小,下面说法中正确的是A两个质量相同的物体,在阻力相同的情况下,速度大的不容易停下来,所以速度大的物体惯性大
- 明成祖时,有人主张对入贡互市的外商征税,明成祖答复:“今夷人慕义远来,乃侵其利,所得几何?而亏辱大体多矣”。对此认识正确
- 下列叙述中,不正确的个数有( )①所有的正数都是整数②一定是正数 ③无限小数一定是无理数④没有平方根 ⑤的平方
- 执行右图所示的程序框图,则输出__ ___.
- “以史为鉴,勿忘国耻”。近代使上海蒙辱开放为通商口岸的第一个不平等条约是 A.《南京条约》 B.《北京条
- 2、根据中国古代宗法制,能够继承周王王位的人首先是( ) A、周王最聪明的儿子
- 阅读下面一首唐诗,然后回答问题。 移家别湖上亭 戎昱 好是春风湖上亭,柳条藤蔓系离情。 黄莺久住浑相识,欲别频啼四五声。



