专题3 从海水中获得的化学物质 知识点题库
-
(1) I.双氧水(主要成分H2O2)是常见的氧化剂、还原剂。
如下图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式。
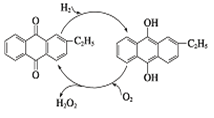
-
(2) H2O2可看作二元弱酸,写出它在水中第一步电离的方程式。
-
(3) II.A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。
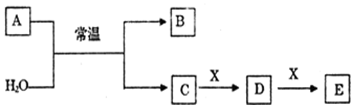
若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式: 。
-
(4) 若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则X可能为(填代号)。
a.NaHCO3 b.Na2CO3 c.Fe(OH)3 d.Na[Al(OH)4]
-
(5) 若A为淡黄色粉末,则A的电子式为。若X为一种最常见的造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为(填代号)。
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
-
(6) 若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红。则A与H2O反应的化学反应方程式为,E是(填化学式)。
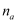 是阿伏加德罗常数的值,下列说法错误的是( )
是阿伏加德罗常数的值,下列说法错误的是( )
 含有的中子数为1
含有的中子数为1 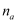 B .
B . 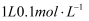 磷酸钠溶液含有的
磷酸钠溶液含有的  数目为0.1
数目为0.1 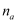 C .
C .  被还原为
被还原为  转移的电子数为6
转移的电子数为6 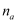 D . 48 g正丁烷和10 g异丁烷的混合物中共价键数目为13
D . 48 g正丁烷和10 g异丁烷的混合物中共价键数目为13 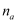
①NaOH溶液和H2SO4溶液:;
②NaCl溶液和AgNO3溶液:;
③Ba(OH)2溶液和H2SO4溶液:;
④Fe与CuSO4溶液反应:;
⑤Na2CO3溶液与Ca(OH)2溶液反应:。
①Al2O3(作耐火坩埚) ②KAl(SO4)2·12H2O(作消毒剂)③Fe2O3(作黄色油漆和涂料) ④NaHCO3(作食用碱) ⑤钠、钾、锶、钡等化合物(作烟花的焰色) ⑥Na2O2(作呼吸面具供氧剂)
-
(1) NaHCO3能用于治疗胃酸过多,反应的离子方程式为。
-
(2) 铁和水蒸气反应的化学方程式为3Fe+4H2O(g)
 Fe3O4+4H2 , 该反应中84g Fe参加反应,转移电子的物质的量为。
Fe3O4+4H2 , 该反应中84g Fe参加反应,转移电子的物质的量为。
-
(3) 制备Fe(OH)3的实验操作:向煮沸的蒸馏水中加入几滴FeCl3溶液,。
-
(4) 密度为1.84g/cm3 , 质量分数为98%的浓硫酸的物质的量浓度为。
 H3O++S2-
B . HS-+H+=H2S
C . CO32-+2H2O
H3O++S2-
B . HS-+H+=H2S
C . CO32-+2H2O  H2CO3+2OH-
D . Fe3++3H2O
H2CO3+2OH-
D . Fe3++3H2O  Fe(OH)3+3H+
Fe(OH)3+3H+
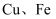 和
和 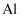 ,此外还含有少量
,此外还含有少量  和
和  。为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的废料抽取氯化铝、绿矾
。为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的废料抽取氯化铝、绿矾  和胆矾晶体。
和胆矾晶体。 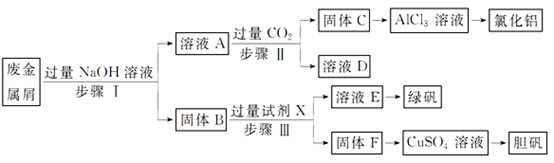
请回答:
-
(1) 写出步骤Ⅰ反应的离子方程式:;;
-
(2) 试剂X是,溶液D是;
-
(3) 在步骤Ⅱ时,用如图所示装置制取
 并通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是;
并通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是; 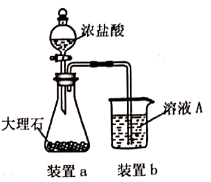
-
(4) 工业上常用溶液E制得净水剂
 ,流程如下:
,流程如下: 
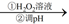
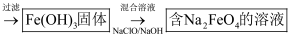
①测得溶液E中
 为
为 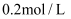 ,若要处理
,若要处理  溶液E,理论上需要消耗25%的
溶液E,理论上需要消耗25%的  溶液
溶液 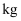 ;
;②写出由
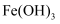 制取
制取  的离子方程式(已知
的离子方程式(已知 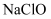 被还原为
被还原为  )。
)。
-
(1) (实验1)配制砷标准溶液
①取0.132gAs2O3 , 用NaOH溶液完全溶解后,配制成1LNa3AsO3溶液(此溶液1mL相当于0.10mg砷)。
②取一定量上述溶液,配制1L含砷量为1mg•L-1的砷标准溶液。
步骤①中,必须使用的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还需。步骤②需取用步骤①中Na3AsO3溶液mL。
-
(2) (实验2)制备砷标准对照液(实验装置如图,夹持装置已略去)
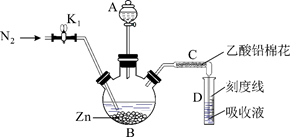
①往B瓶中加入2.00mL砷标准溶液,再依次加入一定量的盐酸、KI试液和SnCl2溶液,室温放置10min,使砷元素全部转化为H3AsO3。
②往B瓶中加入足量锌粒(含有ZnS杂质),立即塞上装有乙酸铅棉花的导气管C,并使C管右侧末端插入比色管D中银盐吸收液的液面下,控制反应温度25~40℃。45min后,生成的砷化氢气体被完全吸收,Ag+被还原为红色胶态银。
③取出C管,在D中添加氯仿至刻度线,混匀,得到砷标准对照液。
乙酸铅棉花的作用是。
-
(3) 完成生成砷化氢反应的离子方程式:。
Zn+H3AsO3+H+=( )+Zn2++( )
-
(4) 控制B瓶中反应温度的方法是;反应中,通入N2的作用是。
-
(5) C管右侧末端导管口径不能过大(一般为1mm),原因是。
-
(6) (实验3)判断样品中砷含量是否超标
称取ag明矾样品替代(实验2)①中“2.00mL砷标准溶液”,重复(实验2)后续操作。对比实验2、3比色管D中液体的颜色,若实验3中液体颜色浅,说明该样品含砷量未超标,反之则超标。
国标规定砷限量为百万分之二(质量分数)。实验测得明矾样品中砷的含量恰好达标,则a的值为g。
 =BaSO4↓
C . 氧化钙与稀盐酸反应:CaO+2H+=H2O+Ca2+
D . 醋酸与氢氧化钾:H++OH¯=H2O
=BaSO4↓
C . 氧化钙与稀盐酸反应:CaO+2H+=H2O+Ca2+
D . 醋酸与氢氧化钾:H++OH¯=H2O
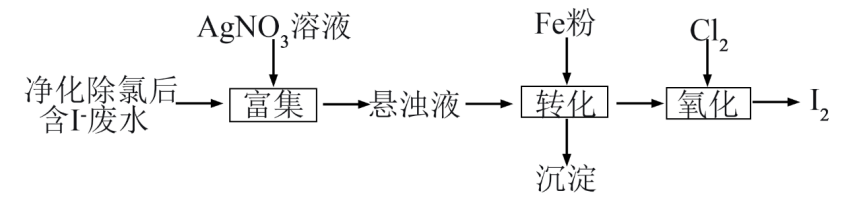
下列说法不正确的是( )
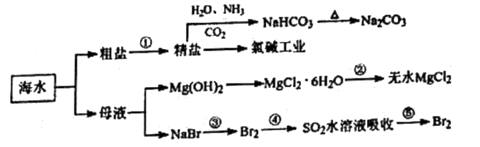
下列说法正确的是( )
 等)通过物理方法即可转为精盐
B . 用澄清的石灰水可鉴别NaHCO3和Na2CO3
C . 在第③步中可通入Cl2使溴离子被还原为Br2
D . 在第④步中,SO2水溶液吸收Br2后,溶液的pH减小
等)通过物理方法即可转为精盐
B . 用澄清的石灰水可鉴别NaHCO3和Na2CO3
C . 在第③步中可通入Cl2使溴离子被还原为Br2
D . 在第④步中,SO2水溶液吸收Br2后,溶液的pH减小
- 设f(x)是定义在R上的增函数,且对于任意的x都有f(-x)+f(x)=0恒成立.如果实 数m、n满足不等式f(m2
- 下列计算正确的是() A.2a3•3a2=6a6 B.a3+2a2=3a5 C.a÷b×=a D.(﹣)÷x
- 下列五组物质,每组中均有一种物质从某种角度分析与其他三种不同,请找出该物质,并说明理由。(1)Fe、S、C、P_____
- 语文综合实践活动。(9分)北漂,指那些漂泊在北京的知识阶层。生活在这个城市,这个城市给他们一份职业,一个饭碗,一间出租屋
- 在一定条件下,甲、乙、丙、丁在某密闭容器内发生反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是( )A
- 如果 ,那么下列结论正确的是( )A . ;B . ;C . ;D . .
- ---Let’s see if the basketball game has started yet. ---St
- 《建议》指出,稳定发展粮食生产,实施优质粮食产业工程,建设大型商品粮生产基地,确保国家粮食安全。这主要是因为 ( ) A
- (南昌市2010年高三第一次模拟考试)元朝是我国历史上第一个由少数民族建立的全国性政权,统治短暂但影响深远。为加强对边
- 某市政府规定,“凡是市政府发布或经市政府同意以部门名义印发的涉及经济社会发展和人民群众切身利益的重要文件,均需进行解读”
- (2012·济宁) 长征精神一直以来鼓舞着一代又一代中国人不断进取。下列红军长征路线按照行程的先后顺序,排列正确的是(
- I wonder why Ann didn’t get ______ the job. She is the right
- 为了较准确地测定一只量程为3V,内阻约3kΩ的电压表的内阻值,在手头没有电流表可用的情况下,某同学设计了如下图所示的实验
- 25℃时,水的电离达到平衡:H2OH++OH-;ΔH>0,下列叙述正确的是( ) A.向水中加入稀氨水,
- 《春思》 贾至① 草色青青柳色黄,桃花历乱②李花香。 东风不为吹愁去,春日偏能惹恨长。 【注】①贾至:唐代洛阳人。这首
- 1945年英国工党上台执政后,大力推行社会福利等政策,目的是为了( ) A.强化自由放任主义
- 非洲最高峰—乞力马扎罗山是著名的“赤道雪山”,近年来,山顶积雪面积不断较小。据此回答29~30题。29.该山顶部出现积雪
- 下列各项中,没有语病的一项是 ( ) A.
- 我国公民和国家的利益在根本上是一致的。据此回答下面试题。 6.在刚刚结束的温哥华冬奥会上,我国选手王濛在身患重感冒的情况
- 声在下列那种物质中传播速度最快: A、水 ; B、玻璃; C、空气;



