第四章 物质结构 元素周期律 知识点题库
下列共有十二种化学符号:
①O2②14C ③238U ④23Na ⑤O3⑥14N ⑦24Mg ⑧ ![]()
⑨235U⑩ ![]() ⑪
⑪ 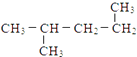 ⑫
⑫ 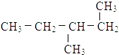
其中:
-
(1) 表示核素的符号共有种.
-
(2) 互为同位素的是(填序号,以下相同).
-
(3) 质量数相等,但不能互称同位素的是
-
(4) 中子数相等,但质子数不相等的是
-
(5) 互为同素异形体的是.
-
(6) 互为同分异构体的是.
原子序数由小到大排列的四种短周期元素X、Y、Z、W的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。M元素与X同主族,与W同周期。
-
(1) M元素是(填元素符号)。
-
(2) Z、W形成的气态氢化物的稳定性为>。(填化学式)
-
(3) 写出M2Z2的电子式:,写出M2Z2与水反应的离子方程式:。
-
(4) 由X、Y、Z、W四种元素中的三种组成一种强酸,该强酸的稀溶液能与铜反应,离子方程式为。
-
(5) 由X、Y、Z、W四种元素组成一种离子化合物A,已知:①1 mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体B,该气体能与氯水反应。则A是(填化学式)。写出气体B与氯水反应的离子方程式:。
短周期元素X和Y可形成离子化合物,其中X的阳离子与Y的阴离子相差一个电子层,下列叙述正确的是( )
A . X和Y一定位于周期表中同一周期
B . X一定是金属元素,Y一定是非金属元素
C . X的最高价一定比Y的最高价低
D . X的离子半径一定比Y的大
现有三种元素的基态原子的电子排布式:①1s22s22p63s23p4;②ls22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是( )
A . 第一电离能:③>②>①
B . 原子半径:③>②>①
C . 电负性:③>②>①
D . 最高正化合价:③>②>①
依据元素周期表及元素周期律,下列推测错误的是()
A . H2SiO3的酸性比H2CO3的强
B . Mg(OH)2的碱性比Be(OH)2的强
C . HCl的热稳定性比H2S的强
D . Na的金属性比Al的强
短周期主族元素X、Y、Z、W原子序数依次增大,X、Y处于同一周期,X原子最外层电子数是次外层电子数的3倍,Z是地壳中含量最多的金属元素,W的最高正价与最低负价绝对值相等。下列说法正确的是()
A . 原子半径:r(X)>r(Y)>r(Z)
B . 由Y、W形成的化合物是共价化合物
C . Z的最高价氧化物对应的水化物是一种强碱
D . Y的简单气态氢化物的热稳定性比W的弱
工业上从电解精炼铜的阳极泥(成分为CuS、Cu2Se、Cu2Te 和少量金属单质Au) 中回收碲、硒的工艺流程如下:
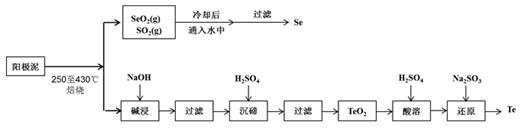
已知:①TeO2是两性氧化物。
②Se和TeO2的物理性质如下:
| 物理性质 | 熔点 | 沸点 | 水溶性 |
| Se | 221℃ | 685℃ | 难溶于水 |
| TeO2 | 733℃ | 1260℃ | 微溶于水 |
-
(1) Se在周期表中的位置为。
-
(2) SeO2与SO2的混合烟气可用水吸收制得单质Se,当有2 mol电子转移时,会生成mol Se。过滤所得粗硒可采用真空蒸馏的方法提纯获得纯硒,采用真空蒸馏的目的是。
-
(3) “碱浸”过滤得到滤渣的主要成分是(填化学式)。
-
(4) “沉碲”时控制溶液的pH为4.5-5.0,生成TeO2沉淀。如果H2SO4的浓度过大,将导致“沉碲”不完全,原因为。
-
(5) “酸溶”将TeO2先溶于硫酸得到Te(SO4)2 , 然后加入Na2SO3溶液进行还原,还原碲的离子反应方程式是。
-
(6) 常温下,SeO2与NaOH溶液反应所得NaHSeO3溶液的pH7(填“>”“<”或“=”),请通过计算说明。(已知25℃时,亚硒酸(H2SeO3)的Ka1=2.5×10-3 , Ka2=2.5×10-7)
下列元素中,非金属性最强的是( )
A . Cl
B . S
C . P
D . F
根据元素周期律,由下列事实进行归纳推测,推测不合理的是( )
| 选项 | 事实 | 推测 |
| A | CaCO3和BaCO3都难溶于水 | SrCO3也难溶于水 |
| B | Si是半导体材料,同族的Ge也是半导体材料 | 第ⅣA族的元素的单质都可作半导体材料 |
| C | HCl在1 500 ℃时分解,HI在230 ℃时分解 | HBr的分解温度介于二者之间 |
| D | Si与H2高温时反应,S与H2加热能反应 | P与H2在高温时能反应 |
A . A
B . B
C . C
D . D
下列物质中,既含共价键又含离子键的是( )
A . KCl
B . CO2
C . MgCl2
D . NaOH
下列说法正确的是( )
A . 异丁烷的一氯取代物有两种
B . 氕、氘、氚是氢元素的三种核素,中子数都为1
C . 乙醛和丙烯醛(CH2=CHCHO)互为同系物
D . O2 和O3互为同素异形体,具有相似的物理性质
X、Y、M、N是短周期主族元素,且原子序数依次增大。已知X原子的最外层电子数是电子层数的3倍,X、M同主族,Y原子在短周期主族元素中原子半径最大。下列说法正确的是( )
A . Y2X和Y2X2中化学键类型相同,阴、阳离子的个数比相同
B . 气态氢化物的热稳定性:M>N
C . M与X的化合物对应的水化物一定是强酸.
D . 离子半径 

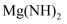 在水中水解生成
在水中水解生成 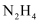 和
和 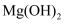 。下列化学用语表述错误的是( )
。下列化学用语表述错误的是( )
A . 中子数为9的氧原子:  B .
B . 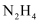 的结构式:
的结构式: 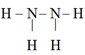 C .
C .  的结构示意图:
的结构示意图: 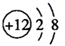 D .
D .  的电子式:
的电子式: 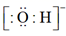
 B .
B .  的结构式:
的结构式: 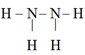 C .
C .  的结构示意图:
的结构示意图:  的电子式:
的电子式:
下列化学用语正确的是( )
A . 氨的电子式: 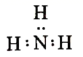 B . 中子数为18的氯的核素:
B . 中子数为18的氯的核素: 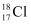 C .
C .  与
与  互为同位素
D .
互为同位素
D . 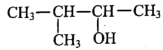 的系统命名:3-甲基-2-丁醇
的系统命名:3-甲基-2-丁醇
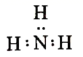 B . 中子数为18的氯的核素:
B . 中子数为18的氯的核素: 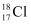 C .
C .  与
与  互为同位素
D .
互为同位素
D . 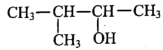 的系统命名:3-甲基-2-丁醇
的系统命名:3-甲基-2-丁醇
长式周期表共有18个纵列,从左到右排为1~18列,碱金属为第1列,稀有气体元素为第18列。按这种规定,下列说法正确的是( )
A . 第2~12列元素中没有非金属元素
B . 最外层电子排布式为ns2np1的元素位于第3列
C . 第4周期第8列元素,其原子结构示意图为 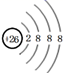 D . 第13~17列元素的最高正化合价均依次增大
D . 第13~17列元素的最高正化合价均依次增大
 D . 第13~17列元素的最高正化合价均依次增大
D . 第13~17列元素的最高正化合价均依次增大
下列化学用语表示正确的是( )
A . N2H4的结构式: 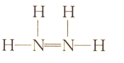 B . Al3+的结构示意图:
B . Al3+的结构示意图:  C . BF3的电子式:
C . BF3的电子式: 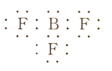 D . 异戊二烯的球棍模型:
D . 异戊二烯的球棍模型: 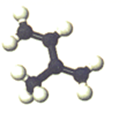
 B . Al3+的结构示意图:
B . Al3+的结构示意图:  C . BF3的电子式:
C . BF3的电子式: 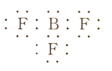 D . 异戊二烯的球棍模型:
D . 异戊二烯的球棍模型: 
在离子 Rn- 中,共有x个核外电子,R原子的质量数为 A,则R原子核内含有的中子数目是( )
A . A–x+n
B . A–x
C . A–x-n
D . A+x-n
下列有关化学用语表示正确的是( )
A . 中子数为10的氧原子: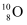 B . Cl2O的球棍模型:
B . Cl2O的球棍模型: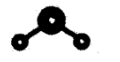 C . HClO的电子式:
C . HClO的电子式: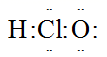 D . 乙醇的最简式:C2H6O
D . 乙醇的最简式:C2H6O
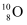 B . Cl2O的球棍模型:
B . Cl2O的球棍模型: C . HClO的电子式:
C . HClO的电子式: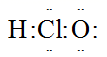 D . 乙醇的最简式:C2H6O
D . 乙醇的最简式:C2H6O
短周期主族元素X、Y、Z、W的原子序数依次增大。X单质可用作保护气,Y为短周期中原子半径最大的元素,Z原子的最外层电子数等于X与Y的最外层电子数之和。下列叙述正确的是( )
A . 简单氢化物的沸点:X<Z
B . Z2W2分子中各原子最外层均达到8电子结构
C . 简单离子的半径:X<Y
D . Y和Z的简单离子均能破坏水的电离平衡
下列各组性质的比较中,正确的是( )
A . 沸点:Li<Na<<K
B . 熔点:金刚石>晶体硅>碳化硅
C . 第一电离能:S<P<Cl
D . 元素的电负性:N>O>F
最近更新
- 设计试管婴儿所引发的主要问题是( ) A.不适合的胚胎的处理问题 B.将此技术用于设计婴儿性别等
- .于良史的五律《春山夜月》的八句诗恰当的排列顺序是 ①欲去惜芳菲 ②南望鸣钟处 ③赏玩夜忘归 ④掬水月在手
- 下列关于细胞的全能性的叙述,不正确的是( ) A.具有全部遗传信息是细胞的全能性的基础 B.是指细胞具有分裂分化成
- 已知函数有且只有一个零点,其中. (Ⅰ)求的值; (Ⅱ)若对任意的,有成立,求实数的最大值; (Ⅲ)设,对任意, 证明:
- 已知酶I、酶Ⅱ、酶Ⅲ的产生分别受独立遗传的三对基因A—a、B—b、C—c控制,这三种酶共同作用可将一原本无色的物质转变为
- 根据下面的新闻材料,拟一条一句话新闻(不超过20字) “红段子”就要来了!在有关部委和几大移动运营商的联合高调推动下,中
- 根据热力学定律和分子动理论,可知下列说法中正确的是 ( )A.当分子间距离等于r0时,分子势能一定等于零B.
- 下图转化关系中,A、B、C、D、E都是短周期元素的单质,在常温常压下A 是固体,其余都是气体,且C呈黄绿色。化合物H和I
- 经济学上所推崇的“橄榄型”收入分配结构,是低收入和高收入相对较少,中等收入占绝大多数的分配结构,这种结构要比我国目前的“
- 在春天,黄河水边上的湿地是很松软的,人在这些湿地上行走时容易下陷,在人下陷时( ) A.人对湿地地面的压力大于湿地地面
- 下列各组物质分类正确的是()酸 碱 盐 氧化物 A 硫酸 纯碱 硫酸钙 氧化铁 B 盐酸 烧碱 纯碱 氧化钙 C 碳酸
- 如图所示,在长方体OABC—O1A1B1C1中,|OA|=2,|AB|=3,|AA1|=2,E是BC中点.建立空间直角坐
- 设向量,,且,则______.
- 函数的定义域是___ _____.
- 计算:_______.
- 书面表达(满分25分) 假设你是李红,最近感冒刚好。你班的美籍同学Mary发来电子邮件询问你的病情,想了解你是不是患了甲
- --Is this yourruler?—Yes,_________. A.it is
- 如图为“验证力的平行四边形定则”实验,三个细线套L1、L2、L3一端共系于一个结点,另一端分别系于轻质弹簧测力计A、B和
- 写出计算12+32+52+…+9992的程序,并画出程序框图.
- 为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动: [探究一](1)将已去除表



