实验活动2 铁及其化合物的性质 知识点题库
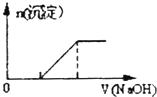 向0.1mol·L﹣1该物质的溶液中滴加0.1mol·L﹣1NaOH溶液,生成沉淀的物质的量与逐滴加入NaOH溶液体积关系如图所示
C . 检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色
D . 向该物质的溶液中摘加Ba(OH)2溶液,恰好使SO42﹣完全沉淀的离子方程式为:Fe2++2SO42﹣+3Ba2++2OH﹣═2BaSO4↓+Fe(OH)2↓
向0.1mol·L﹣1该物质的溶液中滴加0.1mol·L﹣1NaOH溶液,生成沉淀的物质的量与逐滴加入NaOH溶液体积关系如图所示
C . 检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色
D . 向该物质的溶液中摘加Ba(OH)2溶液,恰好使SO42﹣完全沉淀的离子方程式为:Fe2++2SO42﹣+3Ba2++2OH﹣═2BaSO4↓+Fe(OH)2↓
| 选项 | 实验 | 现象 | 结论 |
| A | 向添有KIO3的食盐中加入淀粉溶液、稀盐酸及KI | 溶液变蓝色 | 氧化性:IO3- >I2 |
| B | 将SO2气体通入到Ba(NO3)2溶液中 | 生成白色沉淀 | 此沉淀是BaSO3 |
| C | 将FeCl2样品溶于盐酸后,滴加KSCN溶液 | 溶液变成红色 | 原FeCl2样品已变质 |
| D | 燃烧的钠粒放入CO2中 | 燃烧且有白色和黑色颗粒产生 | 黑色颗粒是炭,白色颗粒可能是Na2CO3 |
-
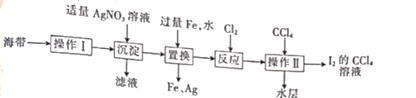
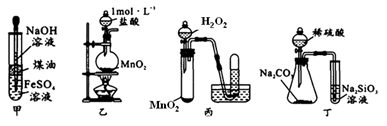
(1) 操作Ⅰ的主要目的是获得含
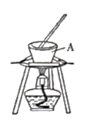
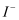 的溶液,他包括灼烧、水浸。其中灼烧用的装置如图所示,仪器A的名称为
的溶液,他包括灼烧、水浸。其中灼烧用的装置如图所示,仪器A的名称为
-
(2) 若“反应”中通入的Cl2恰好将
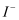 转化为
转化为 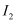 ,则该反应的离子方程式为,由此可以证明Cl2的氧化性(填“强”或“弱”)于
,则该反应的离子方程式为,由此可以证明Cl2的氧化性(填“强”或“弱”)于 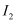
-
(3) 操作Ⅱ的现象是;得到水层的方法:将通入Cl2后的溶液置于分液漏斗中,加人CCl4,振荡静置,
-
(4) 检验“操作Ⅱ”所得水层中是否含有
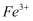 的方法是
的方法是
| 选项 | a | b | c |
| A | Fe | FeCl2 | FeCl3 |
| B | Si | SiO2 | SiF4 |
| C | HNO3 | NO | NO2 |
| D | Al | Al2O3 | Al(OH)3 |
| 实验目的 | 实验操作 | |
| A | 焰色试验后为了除去铂丝上杂质 | 将铂丝用盐酸洗净后,在酒精灯外焰上灼烧至与原来的火焰颜色相同 |
| B | 除去Na2CO3固体中的NaHCO3 | 将固体加热至恒重 |
| C | 探究维生素C的还原性 | 向盛有2mL黄色氯化铁(FeCl3)溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
| D | 制备Fe(OH)3胶体 | 将饱和FeCl3溶液滴加到NaOH浓溶液中 |
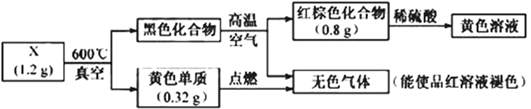
-
(1) X中的非金属元素是,检验黄色溶液中的金属阳离子加入化学试剂是。
-
(2) 黑色化合物
 红棕色化合物的化学方程式是。
红棕色化合物的化学方程式是。
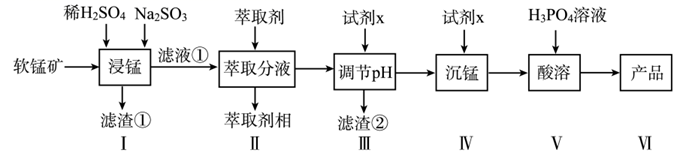
试回答下列问题:
-
(1) 滤渣①的主要成分是;浸锰时,FeO生成Fe3+的离子方程式为,适量的Na2SO3固体的作用是。
-
(2) 检验滤液①中是否含有Fe2+ , 除了用K3Fe(CN)6溶液外,还可以用试剂,若滤液①中含有Fe2+其现象是。
-
(3) 步骤II中,Fe3+的萃取率与pH的关系如图,如pH>1.7后,随pH增大,Fe3+萃取率下降的原因是。
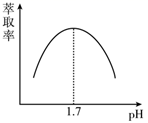
-
(4) 试剂x为某种钠的正盐,从环保、经济角度,x最好为(写化学式);若c(Mn2+)=1.0 mol·L-1 , 调节pH范围应为(该条件下,Ksp[Al(OH)3]=1.0×10-33 , Ksp[Mn(OH)2]=1.0×10-14)。
-
(5) 步骤V酸溶时逐滴加入H3PO4溶液呈酸性才能保证生成物质较多为Mn(H2PO4)2·2H2O,试结合离子方程式说明原因。
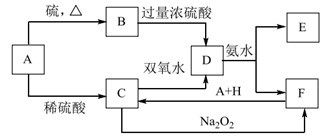
A的一种合金用量最大,用途最广。请回答下列问题:
-
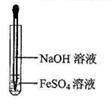
(1) 在C中加入氢氧化钠溶液的现象:。
-
(2) B、H的化学式:B、H。
-
(3) Na2O2的电子式:。
-
(4) 写出鉴定E中阳离子的实验方法和现象:。
-
(5) 在C溶液中加入与C等物质的量的Na2O2 , 恰好使C转化为F,写出该反应的离子方程式:。
-
(1) 所含铁元素既有氧化性又有还原性的物质是______(用字母代号填空)。A . Fe B . FeCl3 C . FeSO4 D . Fe2O3
-
(2) 向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是nm。
-
(3) 检验溶液中是否存在Fe3+的试剂是(填物质名称),若要验证溶液中不含Fe3+而只含有Fe2+ , 正确的实验操作方法及现象是。
-
(4) 电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
①请写出FeCl3溶液与铜反应的离子方程式:。
②欲从制造印刷电路板的废液中回收铜,并重新获得FeCl3溶液的工艺流程如下:
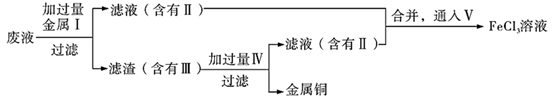
请写出上述流程中加入I和IV的有关物质的化学式:I,IV。请写出通入V反应的离子方程式。
 加入硝酸银溶液都有白色沉淀,再加入稀硝酸沉淀都溶解
加入硝酸银溶液都有白色沉淀,再加入稀硝酸沉淀都溶解
| 选项 | 实验操作 | 现象 | 结论 |
| A | 过量的Fe粉中加入稀HNO3 , 充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | 向溶液中加入少量酸性高锰酸钾溶液 | 紫色褪去 | 可证明溶液中不含Fe3+ , 可能含有Fe2+ |
| C | Fe放入冷的浓硫酸中 | 无现象 | 铁不与浓硫酸反应 |
| D | 向硫酸亚铁溶液中加入氯水,再加入KSCN溶液 | 溶液变为红色 | 不能说明硫酸亚铁溶液中存在Fe3+ |
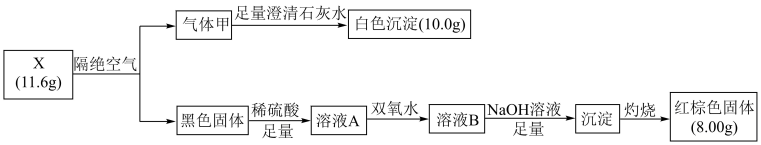
回答下列问题:
-
(1) 气体甲的结构式,X的化学式是。
-
(2) 写出溶液A中加一定量的双氧水后发生反应的离子方程式是。
-
(3) 验证溶液B中可能含有的金属阳离子
 , 下列检验试剂选用正确的是____。
A . 用氯水、KSCN溶液检验是否有
, 下列检验试剂选用正确的是____。
A . 用氯水、KSCN溶液检验是否有 B . 用酸性
B . 用酸性 溶液检验是否有
溶液检验是否有 C . 用
C . 用 溶液检验是否有
溶液检验是否有
选项 | 实验操作和现象 | 实验结论 |
A | 将浓硫酸滴到蔗糖表面,固体变黑膨胀 | 浓硫酸具有吸水性和强氧化性 |
B | 向NaI溶液中滴加少量氯水和CCl4 , 振荡、静置,下层溶液显紫色 | 还原性:I->Cl- |
C | 加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结 | NH4Cl固体可以升华 |
D | 向某溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色 | 该溶液中一定含有Fe2+ |
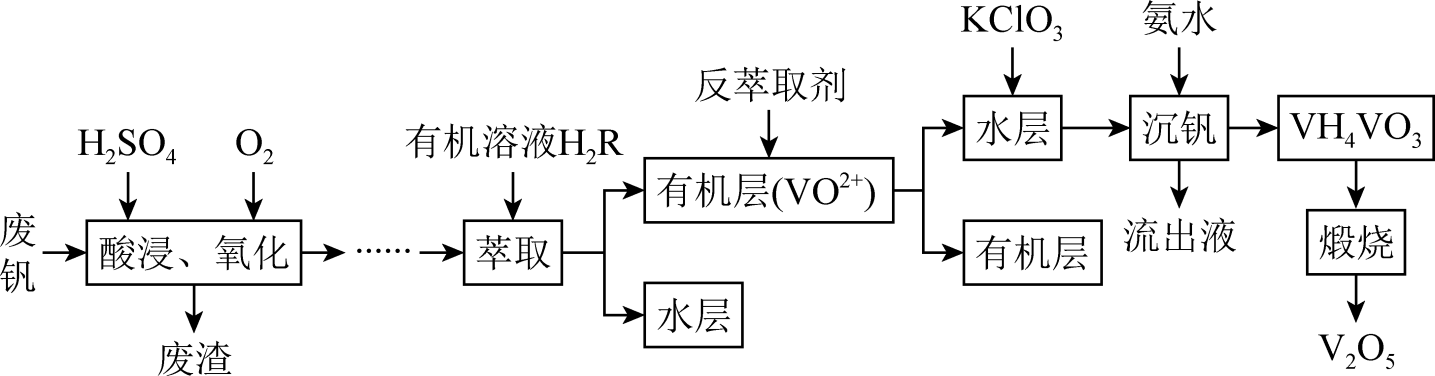
已知:①VOSO4能溶于水,VO2+与Fe不能反应。
②有机溶剂H2R对VO2+及Fe3+萃取率高,但不能萃取Fe2+。
回答下列问题:
-
(1) “酸浸、氧化”过程中若用浓盐酸代替硫酸,V2O5转化为VO2+ , 同时生成有毒的一种气体,反应的化学方程式为。同时该步骤中V2O3转化为VO2+ , 反应的离子方程式为。
-
(2) 萃取前用“铁粉”对酸浸后的浸出液进行处理,主要目的是,为检验处理后的浸出液中是否含有该杂质离子,可选用的化学试剂是(填试剂名称)。
-
(3) “溶剂萃取与反萃取”可表示为:VO2++H2R
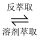 VOR+2H+。为了提高VO2+的产率,反萃取剂可选用。(供选物质:NaCl,NaOH,H2SO4 , 填写相应物质的化学式)
VOR+2H+。为了提高VO2+的产率,反萃取剂可选用。(供选物质:NaCl,NaOH,H2SO4 , 填写相应物质的化学式)
-
(4) 反萃取后的水层中加KClO3 , 使VO2+变为VO
 , ClO
, ClO 变为Cl-。当反应1.5molVO2+时,至少需要KClO3的物质的量为mol。
变为Cl-。当反应1.5molVO2+时,至少需要KClO3的物质的量为mol。
-
(5) 已知NH4VO3难溶于水,Kap=3.0×10-8 , 向10mL0.1mol·L-1NaVO3的滤液中加入等体积的NH4Cl溶液忽略混合过程中的体积变化,欲使VO
 沉淀完全,则NH4Cl溶液的最小浓度为(保留两位有效数字,溶液中某离子浓度≤1×10-6mol·L-1时,认为该离子沉淀完全)
沉淀完全,则NH4Cl溶液的最小浓度为(保留两位有效数字,溶液中某离子浓度≤1×10-6mol·L-1时,认为该离子沉淀完全)
- 研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为5MnO2+
- 钱穆在《中国历史研究法》中提出“中国自秦以下两千年,只可说是一个君主一统的政府,却绝不能说是君主专制。人才的选拔,官吏的
- 计算:.
- 今年的政府工作报告指出,对于确需设置的行政审批事项,要建立权力清单制度,一律向社会公开,清单之外的,一律不得实施审批。给
- In fact ____ is a hard job for the police to keep order in a
- 数列{}中,,(是不为0的常数,),且,,成等比数列. (1) 求数列{}的通项公式; (2) 若=,为数列{}的前n
- 在一真空恒容容器中盛有1 mol PCl5,加热到200 ℃时发生如下反应:PCl5(气)PCl3(气)+Cl2(气),
- 如图B-5所示,叠放在一起的A、B两物体在水平力F的作用下,沿水平面以某一速度匀速运动.现突然将作用在B上的力F改为作用
- 不同商品的需求量对价格变动的反应程度不同。一般来说,下图中反映生活必需品需求量变化情况比较适当的曲线是A.A曲线
- 下列分离混合物常见的仪器:从左至右,用于分离操作正确的是()A.蒸发、萃取、蒸馏、过滤 B.蒸馏、过滤、蒸发、蒸发
- After he left college , he was employed in an international
- 在直角三角形中,,,点是斜边上的一个三等分点,则( ) A.0 B.
- 根据《中华人民共和国反垄断法》等法律法规,2014年9月18日,国家发改委公布了对株式会社等12家日本汽车零部件企业的行
- 从太空上看到的地球形状是( ) A.球形
- 下列选项中属于宪法规定的内容的是①国家的根本制度②公民的基本权利和义务③什么是犯罪④国旗、国徽、国歌、首都⑤国家机构和组
- 容积为2L的烧瓶,在压强为1.0×105Pa时,用塞子塞住,此时温度为27℃,当把它加热到127℃时,塞子被打开了,稍过
- 《长歌行》中表达人生哲理的句子是:______________,______________。
- 一个长方形在平面直角坐标系中,三个顶点的坐标分别是(-1,-1)、(-1,2)、(3,-1),则第四个顶点的坐标是(
- 纳米技术开辟了材料的新天地,在北京的申奥工程中,就使用了我国最近研制的一项新成果——“纳米塑料”。下列说法正确的是(
- 下列说法中正确的是:A、鞋底的花纹是为了增大摩擦;B、离手的千球还能继续在空中运动是由于受到手的推力;C、潜水员在水下看



