第二章 海水中的重要元素——钠和氯 知识点题库
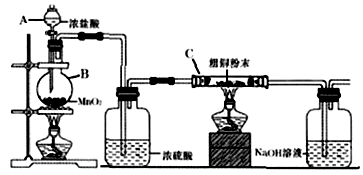
[制备CuCl2·2H2O晶体]
-
(1) 仪器B的名称是;B中反应的离子方程式为。
-
(2) 装置C中粗铜粉末与气体充分反应时的生成物是(填化学式)。反应完成后,将C中的固体用稀盐酸完全溶解、再加入试剂M除杂,经一系列操作便可获得CuCl2·2H2O晶体。
①试剂M应当选用(填符合题意答案字母编号)
a.Cu(NO3)2 b.NaOH c.CuO d.NH3·H2O e.Cu(OH)2
②溶解C中生成物固体时,有时会加入少量双氧水,目的是。
③设计简易实验方案确定所CuCl2·2H2O晶体中不含铁化合物:。
-
(3) [制备CuCl 固体]
将CuCl2·2H2O晶体在HCl气流中加热到140℃得无水CuCl2 , 再加热到300℃以上可获得CuCl固体。
将CuCl2·2H2O晶体在HCl气流中加热脱水的原因是。 -
(4) 为测定CuCl固体的产率,进行如下定量分析:
①将10.26gCuCl2·2H2O晶体先加热到140℃,再加热到300℃以上,充分反应后,将所得固体平均三份,分别转移至三个锥形瓶中。
②分别在三个锥形瓶中加过量FeCl3溶液不断振荡,使固体迅速溶解,再加入2滴1,10—邻菲啰啉一硫酸亚铁络合物作指示剂。
③用1.00mol/L的硫酸铈[Ce(SO4)2]标准液进行滴定。平行测定三份样品溶液,消耗硫酸铈[Ce(SO4)2]标准溶液的平均体积为19.40mL。
反应原理: CuCl+ FeCl3=CuCl2+FeCl2 , Fe2++Ce4+=Ce3++Fe3+
根据上述定量实验计算CuCl的产率为。
-
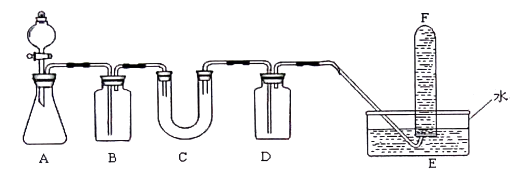
(1) A是制取CO2的装置。写出A中发生反应的化学方程式:。
-
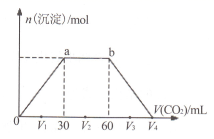
(2) 填写表中空格:
仪器
加入试剂
加入试剂的目的
B
饱和NaHCO3溶液
C
D
 B .
B . 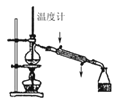 C .
C . 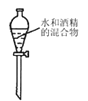 D .
D . 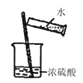
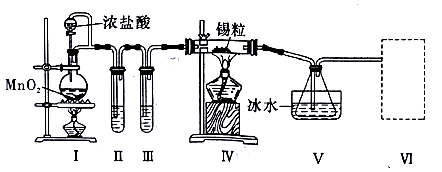
已知:①金属锡熔点为 231℃,化学活泼性与铁相似;②SnCl4 的沸点为 114℃;③SnCl4 易与水反应。
请根据上图装置回答:
-
(1) 装置Ⅳ中发生反应的化学方程式为。
-
(2) 试管II中的试剂是,装置 V 的作用是。
-
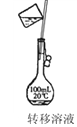
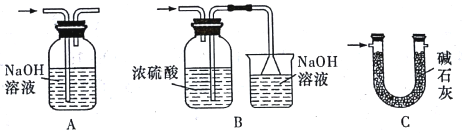
(3) 裝置Ⅵ最好选用下列装置中的(填标号)。
-
(4) 实验结束后,欲回收利用装置Ⅰ中未反应完的 MnO2 , 需要的分离方法。
-
(5) 为了顺利完成实验,点燃酒精灯的正确操作是___________________(填字母)。A . 先点燃 I 处酒精灯,后点燃Ⅳ处酒精灯 B . 先点燃Ⅳ处酒精灯,后点燃 I 处酒精灯 C . 同时点燃 I、Ⅳ两处酒精灯
-
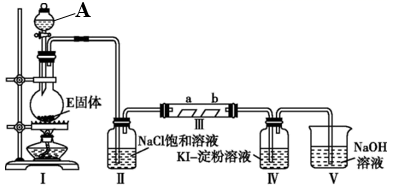
(1) A装置的名称是 , 实验室以二氧化锰和浓盐酸制备氯气的离子方程式是。
-
(2) 装置Ⅱ的作用是。
-
(3) 实验过程中,装置Ⅳ中的实验现象为;发生反应的化学方程式为。
-
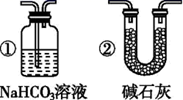
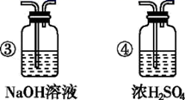
(4) 实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置Ⅱ与Ⅲ之间添加如图中的(填序号)装置。
-
(5) 装置Ⅴ的目的是防止尾气污染,写出装置Ⅴ中发生反应的离子方程式:。
 为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )
 溶于稀氨水中,所得溶液呈中性,则溶液中
溶于稀氨水中,所得溶液呈中性,则溶液中 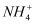 的数目为
的数目为  B . 常温下,
B . 常温下, 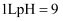 的
的 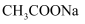 溶液中,发生电离的水分子数为
溶液中,发生电离的水分子数为  C . 将5.6g铁块投入一定量的稀硝酸中,恰好完全反应,一定转移
C . 将5.6g铁块投入一定量的稀硝酸中,恰好完全反应,一定转移  个电子
D . 将
个电子
D . 将 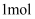 氯气完全溶于水,所得溶液中
氯气完全溶于水,所得溶液中 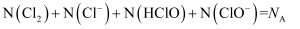
-
(1) Ⅰ.如图为实验室在加热条件下利用二氧化锰和浓盐酸反应制取氯气并验证氯气的某些性质的实验装置。E瓶内放有干燥的红色布条;F的玻璃管中放有红色的铜网。
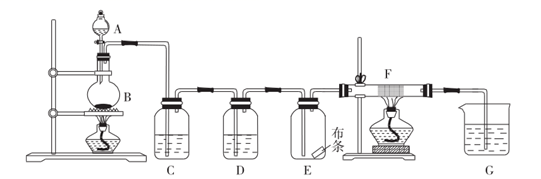
装置C中盛装的溶液是,D中试剂的作用是。
-
(2) 实验中,E瓶内干燥的红色布条(填“褪色”或“不褪色”),说明干燥的氯气(填“具有”或“不具有”)漂白作用。
-
(3) F中反应的化学方程式为。
-
(4) 装置G的作用是,发生反应的离子方程式为。
-
(5) Ⅱ.某实验小组利用以下装置制取并探究氨气的性质:
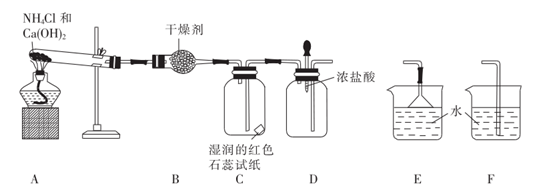
装置A中发生反应的化学方程式为。
-
(6) 装置B中的干燥剂是(填名称)。
-
(7) 装置C中的现象是。
-
(8) 实验进行一段时间后,挤压装置D中的胶头滴管,滴入
 滴浓盐酸,可观察到的现象是。
滴浓盐酸,可观察到的现象是。
-
(9) 为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置是(填“E”或“F”),尾气吸收过程中发生反应的化学方程式为。
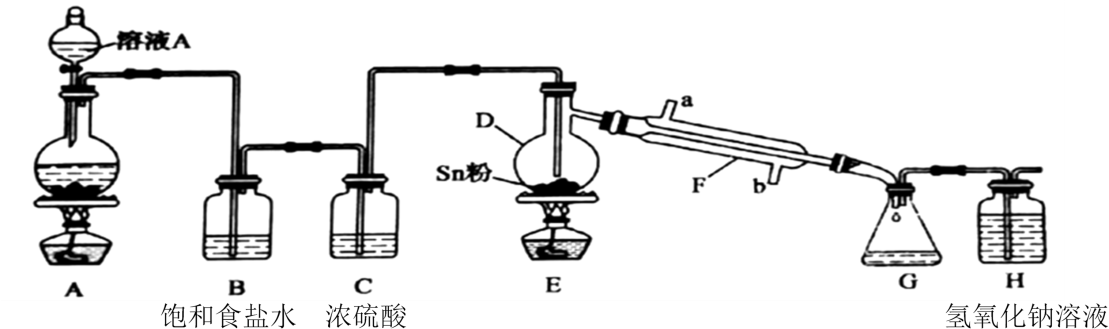
已知:①金属锡熔点为231℃,化学活泼性与铁相似。
②SnCl4为无色液体,熔点-33℃,沸点114℃,极易水解生成SnO2·xH2O,在潮湿的空气中发烟。
③SnCl2中的Sn2+易被氧化为Sn4+。
回答下列问题:
-
(1) 打开分液漏斗上端活塞的作用是,装置A中发生反应的化学方程式为。
-
(2) 实验开始时,正确的操作顺序为(用下列序号排顺序)。
①点燃装置A处酒精灯②点燃装置D处酒精灯③打开分液漏斗活塞
-
(3) 装置B中试剂的作用是,装置F中冷凝水的方向是从端进(填“a”或“b”)。
-
(4) 若没有装置C(其他均相同),则D中发生的主要副反应的化学方程式为:。
-
(5) 该实验装置存在设计缺陷,你的改进措施为。
-
(6) H为尾气处理,请写出反应的离子方程式。
选项 | 素质教育 | 化学知识或原理 |
A | 音乐:“音乐焰火”创造出火树银花不夜天 | 焰色反应属于化学变化 |
B | 体育:北京冬奥会火炬外壳材料是由高性能树脂与碳纤维融合而成的复合材料 | 该复合材料具有耐高温、耐腐蚀等优良的特性 |
C | 美术:宋代《千里江山图》中的绿色来自孔雀石颜料[主要成分为Cu(OH)2·CuCO3],青色来自蓝铜矿颜料[主要成分为Cu(OH)2·2CuCO3] | 孔雀石、蓝铜矿颜料不易被空气氧化且耐酸、耐碱 |
D | 文学:爆竹声中一岁除,春风送暖入屠苏 | 传统爆炸粉为黑火药,其主要成分为木炭、硫磺、KClO3 |
 CuSO4(aq)
CuSO4(aq) Cu
B . 饱和食盐水
Cu
B . 饱和食盐水 NaHCO3
NaHCO3 Na2CO3
C . H2S
Na2CO3
C . H2S S
S SO3
SO3 H2SO4
D . Si
H2SO4
D . Si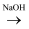 Na2SiO3
Na2SiO3 SiO2
SiO2 H2SiO3
H2SiO3
 固体中的
固体中的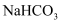
- 科学家在利用无土栽培法培养一些名贵花卉时,培养液中添加了多种必需化学元素。其配方如下: 离 子 K+ Na+ Mg2+
- --- I think you’ve _________ the point. --- What? ---
- 若此图表示某个国家的人口、资源、环境状况,则该国最有可能位于 ( ) A.非洲
- 到1906年,法国德雷福斯案最终得以平反,最能说明 A.共和派和人民群众为维护、发展民主共和制进行着不懈斗争 B.法国废
- 现今世界上较先进的计算机显卡每秒可绘制出27000000个三角形,且显示逼真,用科学记数法表示这种显卡每秒绘制出三角形_
- 设,,则的关系是( ) A. B. C. D.不能比较大小
- 在平面直角坐标系的第一象限内,边长为1的正方形ABCD的边均平行于坐标轴,A点的坐标为(,)。如图,若曲线与此正方形的边
- 用1,2,3,4,5排成一排组成没有重复数字的五位数,并且奇数排在奇数位置,这样的五位数有( )A.12个
- 我国古代的四大发明为人类作出了重要贡献,下图所示是其中哪一项发明外传的示意图( )A.指南针B.造纸术 C.印刷术
- 已知,都是锐角,,,求的值
- .数轴上表示1和3的点分别为A和B,点B关于点A的对称点是点C,则点C 所表示的数是 ( ) A
- 一般来说,动物细胞体外培养需要满足以下条件 ①无毒的环境 ②无菌的环境 ③合成培养基需加血清 ④温度与动物体温
- 具有下列电子排布式的原子中,半径最大的是 A.ls22s22p63s23p3 B.1s22s22p3 C.1s22s2
- 由钠、镁、铝、铁四种金属中的两种组成的混合物12 g,与足量的盐酸反应,产生0.5 mol H2,则该混合物中一定不含(
- [选修1--历史上重大改革回眸]阅读下列材料,回答问题。 材料一: 若夫美、法民政,英、德宪法,地远俗殊,变久迹绝,臣故
- 宋太祖赵匡胤剥夺了功臣宿将的兵权后,鼓励他们“多积金、市田宅以遗子孙。”他主要是为了 ( ) A.巩固专制统治
- 阅读下面的漫画《跳回井里》和文字,按要求作文。(60分)说明:漫画中打油诗的文字为“人人都夸天好大,见了青天又害怕。跳出
- 下列离子方程式表达正确的是 A.Na2S的水解:S2ˉ+ 2H2OH2S +2OHˉ B.用铜电极电解CuSO4溶液:2
- 据报道,2013年5月某日,我国渔民在南海某海域(117°E、16°N)附近进行海上捕捞作业时,受到某邻国军舰的干
- 小刚在学习“新航路开辟”时,做了如下笔记,其中不正确的是( )A.根本原因:资本主义萌芽



