第二章 海水中的重要元素——钠和氯 知识点题库
对一定量气体体积的探究.
已知1 mol不同气体在不同条件下的体积.
化学式 | 条件 | 1mol气体体积 |
H2 | 0℃,101kPa | 22.4 |
O2 | 0℃,101kPa | 22.4 |
CO | 0℃,101kPa | 22.4 |
H2 | 0℃,202kPa | 11.2 |
CO2 | 0℃,202kPa | 11.2 |
N2 | 273℃,202kPa | 22.4 |
NH3 | 273℃,202kPa | 22.4 |
-
(1) 从上表分析得出的结论:①1 mol任何气体在标准状况下的体积都约为.
②1 mol不同的气体,在不同的条件下,体积(填“一定”、“一定不”或“不一定”)相等.
-
(2) 理论依据:相同条件下,1mol任何气体的体积几乎相等,原因是:①,②.
-
(3) 应用:在标准状况下,48g O3的体积为多少升?(写出计算过程)
如图是一种试验某气体化学性质的实验装置,图中B为开关。 如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是( )
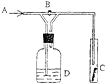
A . 浓H2SO4
B . 浓NaOH溶液
C . 饱和Na2SO4溶液
D . 石灰乳
将相同体积的硫酸铁、硫酸锌和硫酸铝中的SO42-完全沉淀, 需消耗相同物质的量浓度的BaCl2溶液的体积比为3 : 2 : 1,则硫酸铁、硫酸锌和硫酸铝溶液的物质的量浓度之比为( )
A . 3∶2∶1
B . 3∶6∶1
C . 9∶3∶1
D . 3∶1∶3
标准状况下,a L氢气在过量的bL氯气中燃烧,所得混合物用100mL3.00mol·L-1的NaOH溶液恰好完全吸收,则氯气的体积b为( )
A . 2.24L
B . 4.48L
C . 3.36L
D . 1.12L
NA为阿伏加德罗常数,下列说法正确的是( )
A . 7.8g苯所含碳碳双键数目为0.3NA
B . 28g乙烯所含共用电子对数目为6NA
C . 标准状况下,11.2L溴乙烷所含分子数为0.5NA
D . 26g乙炔和苯乙烯的混合物,含有原子总数为6NA
溶质的质量分数为14%的KOH溶液,经加热蒸发去100g水后,质量分数变成28%,体积为80mL,则所得到的此溶液的物质的量浓度为( )
A . 5mol/L
B . 6mol/L
C . 6.25mol/L
D . 6.75mol/L
将10.6 g Na2CO3溶于水配成1 L溶液,该溶液中Na+的物质的量浓度为。向该溶液中加入一定量NaCl固体,使溶液中Na+的物质的量浓度为0.4 mol/L(假设溶液体积不变)需加入NaCl的质量为。
下图表示在没有通风橱时制取纯净的氯气时设计的装置图,图中A、B是可控制的弹簧铁夹。
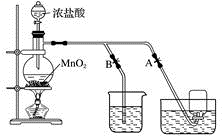
-
(1) 烧杯中盛放的液体是,其作用是,水槽中盛放的液体是。
-
(2) 简述操作过程:(从氯气已经产生开始)在收集氯气之前,应;当氯气纯度合乎要求时,应,当氯气收集完毕时,应。
-
(3) 将8.7 g二氧化锰与含氯化氢14.6 g的浓盐酸共热制氯气,甲同学认为可制得氯气 7.1 g,乙同学认为制得氯气的质量小于7.1 g,你认为(填“甲”或“乙”)同学正确,原因是。
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 标准状况下,4.48 L己烷含有的分子数为0.2NA
B . 15 g甲醛(HCHO)和乙酸的混合物中氧原子数为0.5NA
C . 8.8 g乙酸乙酯中含共用电子对的数目为1.3NA
D . 1 mol甲基(-14CD3)所含的中子数和电子数分别为11NA、10NA
现有烧杯、漏斗、分液漏斗、酒精灯、玻璃棒、量筒、500mL容量瓶、蒸发皿、圆底烧瓶、铁架台(带铁圈)、三脚架、石棉网、火柴、滤纸.若所需试剂均有提供,在以下5个实验中:①沉淀的过滤,②配制500mL1mol/LNaCl溶液,③溴的萃取,④蒸馏,⑤硫酸铜溶液的蒸发浓缩.其中因缺乏某种实验用品而不能完成的实验是( )
A . ①
B . ①和④
C . ③和⑤
D . ②和④
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A . 2H2S+SO2=3S↓+2H2O反应中,每生成1mol氧化产物时转移电子数为NA
B . 物质的量相等的重水与水相差2NA个中子
C . 乙烯和丙烯组成的28g 混合气体中含氢原子数为4NA
D . pH=13的1LBa(OH)2 溶液中所含有OH-数目为0.2NA
已知NA为阿伏加德罗常数的数值,下列有关说法中正确的是( )
A . 22.4L乙烷中所含的极性共价键数目为7NA
B . 某温度下,将1molCl2通入足量水中转移的电子数为NA
C . 常温常压下,3.0g含甲醛的冰酷酸中含有的原子总数为0.4NA
D . 室温下,1LpH为13的NaOH溶液和Ba(OH)2混合溶液中含OH-个数为0.01NA
某化学兴趣小组探究84消毒液(含10.5%NaClO和少量NaOH)与75%医用酒精能否反应,进行如下实验:
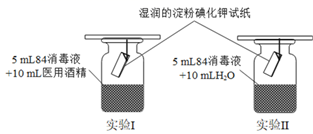
-
(1) 将25mL无水乙醇配成75%医用酒精,下列仪器中不需要使用的有(填名称)。

-
(2) 实验Ⅰ的淀粉碘化钾试纸在3min时变蓝,21min后蓝色褪去,实验Ⅱ则在8min时变蓝,49min后褪色。
①实验中,使淀粉碘化钾试纸变蓝的物质是,而后碘被(填“氧化”或“还原”)导致蓝色褪去。
②对比实验Ⅰ和Ⅱ的现象可以说明乙醇被NaClO氧化,理由是。
③实验过程,测得实验Ⅰ中混合溶液的pH由12.38逐渐增大至12.80,说明乙醇与NaClO反应可能生成。
-
(3) 为了测定84消毒液与医用酒精1:1反应后溶液中剩余NaClO含量:取5.00mL反应后溶液(密度约1g·mL-1)于锥形瓶,加入过量KI溶液和适量硫酸,在冷暗处静置4-5min后,再加入少量淀粉指示剂,用0.1000mol·L-1Na2S2O3标准液滴定,消耗标准液体积为14.80mL。
①滴定前,将锥形瓶置于“冷暗处”的目的是,写出NaClO与KI反应的离子方程式。
②滴定终点溶液的颜色是,84消毒液与医用酒精1:1反应后溶液中NaClO的质量分数=(结果保留3位有效数字;I2+2S2O
 =2I-+S4O
=2I-+S4O 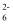 )。
)。
设NA为阿伏加德罗常数的值下列有关叙述正确的是( )
A . 100mL1mol·L-1NH4Cl溶液中含有阳离子的数目小于0.1NA
B . 0.5L0.5mol·L-1醋酸溶液中含有的分子数目小于0.25NA
C . 60gSiO2晶体中含有[SiO4]四面体结构单元的数目为NA
D . 25℃时Ksp(CaSO4)=9×10-6 , 则该温度下CaSO4饱和溶液中含有3×10-3NA个Ca2+
下表所列各组物质中,物质之间不能通过一步反应实现如图转化的是( )
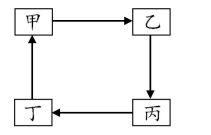
选项 | 甲 | 乙 | 丙 | 丁 |
A | Na | NaOH | Na2CO3 | NaCl |
B | Ca | CaO | Ca(OH)2 | CaCO3 |
C | Al2O3 | AlCl3 | NaAlO2 | Al(OH)3 |
D | 乙醇 | 乙醛 | 乙酸 | 乙酸乙酯 |
A . A
B . B
C . C
D . D
广州地区的自来水是采用氯气消毒的,为了检验Cl-的存在,最好选用下列物质中的( )
A . 石蕊溶液
B . 四氯化碳
C . 氢氧化钠溶液
D . 硝酸银溶液
下列物质应用正确的是( )
A . 纯碱用作治疗胃酸过多的药物
B . 氯气和消石灰用作生产漂白液的原料
C . 二氧化硫用作葡萄酒生产过程中的添加剂
D . 二氧化硅用作北斗芯片中的半导体材料
 为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )
A . 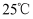 ,
, 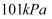 下,
下,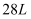 氢气中质子的数目为
氢气中质子的数目为 B .
B . 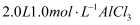 溶液中,
溶液中,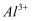 的数目为
的数目为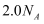 C .
C . 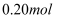 苯甲酸完全燃烧,生成
苯甲酸完全燃烧,生成 的数目为
的数目为 D . 电解熔融
D . 电解熔融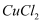 , 阴极增重
, 阴极增重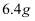 , 外电路中通过电子的数目为
, 外电路中通过电子的数目为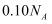
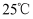 ,
, 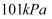 下,
下,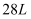 氢气中质子的数目为
氢气中质子的数目为 B .
B . 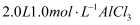 溶液中,
溶液中,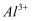 的数目为
的数目为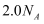 C .
C . 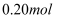 苯甲酸完全燃烧,生成
苯甲酸完全燃烧,生成 的数目为
的数目为 D . 电解熔融
D . 电解熔融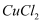 , 阴极增重
, 阴极增重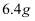 , 外电路中通过电子的数目为
, 外电路中通过电子的数目为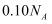
用NA代表阿伏加德罗常数的数值。下列说法正确的是( )
A . 1molCaO2晶体所含离子总数为3NA
B . 将7.1gCl2通入水中,转移电子数为0.1NA
C . 常温下,1L0.1mol·L-1的氨水中含有OH-的数目为0.1NA
D . 标准状况下,11.2LO2、CO2混合气体含有的氧原子数为NA
为验证NaHCO3固体中是否含有Na2CO3 , 下列实验及判断中正确的是( )
A . 加热,观察是否有气体放出
B . 溶于水后滴加澄清的石灰水,看是否有沉淀生成
C . 取固体试样加盐酸,看是否有气泡产生
D . 溶于水后滴加BaCl2溶液,看是否有沉淀生成
最近更新
- 我国各级人民代表大会都有立法权。
- 下列各句中,没有语病的一项是( ) A、中国教育工作者对位于巴黎市中心塞纳河畔的“国立蓬皮杜文化艺术中心”的公
- 小汽车在发生剧烈碰撞时,安全气囊会瞬间弹出,在0.01秒内引发下列化学反应: 2NaN3+NH4NO3═3X↑+2Na+
- 如图,在平面直角坐标系中,边长为2的正方形的边在轴上, 边的中点是坐标原点,将正方形绕点按逆时针方向旋转90°后,点的对
- 已知:若≈1.910,≈6.042,则≈ ,±≈ .
- ____ he remained single all his life. A. Strange though it
- 下列关于人口密度的说法,正确的是( ) A.人口多的国家人口密度就大 B.人口少的国家人口密度就小 C.人口密度
- What’s your opinion of Mr. Ling’s request that we senior stu
- 证明某溶液只含有Fe2+而不含Fe3+的实验方法是( )A.先滴加氯水,再滴加KSCN溶液后显红色B.先滴加KSCN
- 某小组开展“探究生长素类似物促进插条生根的最适浓度”课题研究,在制定实验方案过程中,下列哪一项可以不考虑
- 41. 到游乐园有很多方法:可以坐高速大巴、宾馆的往返汽车,或者乘地铁。 There are _______ wayst
- “在法国,为行将到来的革命启发过人们头脑的那些伟大人物,本身都是非常革命的。”材料中的“伟大人物”主要是指 A.航海家
- 阅读下面的文字,完成1—3题。 大 片 的 路 会 不 会 越 走 越 窄? 尹鸿(清华大学新闻与传播学院教授、副院长)
- 下图是果蝇体细胞的染色体组成,以下说法正确的是( ) A.染色体l、2、4、5组成果蝇的一个染色体组 B.染
- The National Day Parade for the 60th anniversary of the foun
- 下列关于催化剂的说法不正确的是 ( ) A.化学反应前后,催化剂的质量和化学性质都不变 B.催化剂可以提高
- 一小物块以速度v0=10 m/s沿光滑地面滑行,然后沿光滑曲面上升到顶部水平的高台上并由高台上飞出,如图7-7-17所示
- 如图是钠元素的原子结构示意图,下列有关钠原子的叙述不正确的是()A.质子数是11 B.最外层电子数为1 C.核外有3个电
- 中心法则揭示了生物遗传信息由DNA向蛋白质传递与表达的过程。请回答下列问题。⑴a、b、c、d所表示的四个过程依次分别是
- 他代表了一代人的理想1月4日,是作家史铁生的六十岁生日。可惜他没能等到这一天。在2010年的最后一天,史铁生永远离开了他



