第二节 离子反应 知识点题库
下列各组离子在指定的溶液中能大量共存的是( )
①无色溶液中:K+、Cu2+、Na+、SO42﹣
②pH=11的溶液中:CO32﹣、Na+、AlO2﹣、NO3﹣
③加入Al能放出H2的溶液中:Cl﹣、HCO3﹣、NO3﹣、NH4+
④在由水电离出的c(OH﹣)=10﹣13mol•L﹣1的溶液中:Na+、Ba2+、Cl﹣、I﹣
⑤能使红色石蕊试纸变为蓝色的溶液:Na+、Cl﹣、S2﹣、ClO﹣
⑥酸性溶液中:Fe2+、Al3+、NO3﹣、Cl﹣ .
A . ①②⑤
B . ②④
C . ②④⑥
D . ③⑤⑥
由已知电离常数判断,下列关于SO2与Na2CO3(aq)反应的离子方程式的书写中,不合理的是( )
酸 | 电离常数 |
碳酸 | K1=4×10﹣7 K2=5.6×10﹣11 |
亚硫酸 | K1=1.54×10﹣2K2=1.02×10﹣7 |
A . SO2+H2O+2CO32﹣═2 HCO3﹣+SO32﹣
B . SO2+H2O+CO32﹣═H2CO3+SO32﹣
C . 2SO2+2H2O+CO32﹣═H2CO3+2 HSO3﹣
D . SO2+H2O+CO32﹣═HCO3﹣+HSO3﹣
把17.1g Ba(OH)2固体分别加入到100mL 1mol/L的下列物质的溶液中,溶液导电能力变化最小的是( )
A . 醋酸
B . 碳酸钠溶液
C . CuSO4溶液
D . KCl溶液
在无色透明强酸性溶液中,能大量共存的离子组是( )
A . K+、Cu2+、NO3﹣、SO42﹣
B . K+、Na+、Cl﹣、ClO﹣
C . Zn2+、NH4+、NO3﹣、Cl﹣
D . K+、Na+、Ca2+、SO42﹣
在含有稀硫酸的硫酸铁溶液中,下列离子能大量共存的是( )
A . HCO3﹣
B . NO3﹣
C . SCN﹣
D . Ba2+
下列各离子组在指定的溶液中一定能大量共存的是( )
①常温在C(H+)/C(OH﹣)=10﹣10溶液中:K+、Na+、CH3COO﹣、SO42﹣
②常温pH=11的溶液中:CO32﹣、Na+、AlO2﹣、NO3﹣
③水电离出的H+浓度c(H+)=10﹣12mol•L‾1的溶液中:Cl﹣、NO3﹣、Na+、S2O32﹣
④使甲基橙变红色的溶液中:Fe3+、NO3﹣、Na+、SO42﹣ .
A . ①②③
B . ①②④
C . ②③④
D . ①③④
下列离子方程式书写正确的是( )
A . 向FeCl2溶液中通入Cl2:Fe2++Cl2═Fe3++2Cl﹣
B . Ba(OH)2溶液与硫酸反应:OH﹣+H+═H2O
C . 次氯酸钙溶液中通入少量SO2:2ClO﹣+Ca2++SO2+H2O═CaSO3↓+2HClO
D . 碳酸氢钠溶液中加入过量石灰水:HCO3﹣+Ca2++OH﹣═CaCO3↓+H2O
下列各组离子在无色酸性溶液中可以大量共存的有( )
A . Ag+、K+、NO3﹣、Cl ﹣
B . K+、Cu2+、SO42﹣、HCO3﹣
C . Mg2+、Cl﹣、SO42﹣、Na+
D . CO32﹣、K+、NO3﹣、Na+
下列离子方程式中,属于水解反应的是( )
A . HCOOH+H2O⇌HCOO﹣+H3O+
B . CO32﹣+H2O⇌HCO3﹣+OH﹣
C . CO2+H2O⇌HCO3﹣+H+
D . HS﹣+H2O⇌S2﹣+H3O+
下列叙述正确的是( )
A . 取10.00 mL硫酸:在25mL酸式滴定管中装入硫酸,调整初始读数为15.00mL后,将剩余硫酸放入锥形瓶
B . 用乙酸浸泡水壶中的水垢,可将其清除,可以得出结论乙酸的酸性大于碳酸的酸性
C . SO2的水溶液能够导电,所以SO2是电解质
D . 测定醋酸溶液pH用玻璃棒蘸取溶液,点在湿润的pH试纸上
在强酸性、无色透明的溶液中,能够大量存在的离子组是 ( )
A . Na+、Mg2+、NO3-、Cl-
B . Na+、K+、CO32-、NO3-
C . K+、Ba2+、SO42-、Cl-
D . Na+、K+、MnO4-、SO42-
常温下,下列各组离子在指定溶液中能大量共存的是( )
A . c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、NO3-、Cl-
B . 水电离出的c(H+)=10-l2mol/L 的溶液中:Ca2+、K+、Cl-、HCO3-
C . 能使甲基橙呈红色的溶液中:Fe2+、NO3-、SO42-、Na+
D . c(Fe3+)=0.1mol/L 的溶液中:K+、ClO-、SO42-、SCN-
写出下列化学反应的离子方程式
①NaOH溶液和HCl溶液
②Na2CO3和足量HCl
③H2SO4溶液和Ba(OH)2溶液
下列各组离子能够大量共存的是( )
A . 加入Al粉后产生  的溶液中:
的溶液中:  、
、  、
、  、
、  B . 滴加石蕊试剂变红的溶液中:
B . 滴加石蕊试剂变红的溶液中:  、 Fe2+ 、
、 Fe2+ 、  、
、  C . 酸性溶液中: Fe3+ 、
C . 酸性溶液中: Fe3+ 、 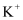 、
、 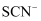 、
、  D . 澄清溶液中:
D . 澄清溶液中: 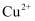 、
、 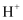 、
、  、
、 
 的溶液中:
的溶液中:  、
、  、
、  、
、  B . 滴加石蕊试剂变红的溶液中:
B . 滴加石蕊试剂变红的溶液中:  、 Fe2+ 、
、 Fe2+ 、  、
、  C . 酸性溶液中: Fe3+ 、
C . 酸性溶液中: Fe3+ 、 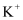 、
、 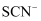 、
、  D . 澄清溶液中:
D . 澄清溶液中: 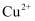 、
、 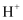 、
、  、
、 
关于电解质强弱及非电解质的组合完全正确的是( )
| A | B | C | D | |
| 强电解质 | NaCl | H2SO4 | CaCO3 | HNO3 |
| 弱电解质 | HF | BaSO4 | HClO | CH3COOH |
| 非电解质 | Cl2 | CO2 | C2H5OH | H2O |
A . A
B . B
C . C
D . D
某强酸性溶液X中可能含有Fe2+、Al3+、NH4+、CO32-、SO32-、SO42-、Cl-中的若干种,现取X溶液进行连续实验,实验过程及产物如下:
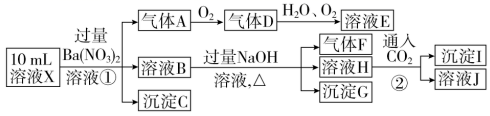
下列说法正确的是( )
A . X中一定存在Fe2+、Al3+、NH4+、SO42-
B . 溶液E和气体F能发生化学反应
C . X中肯定不存在CO32-、SO32-、Al3+
D . 沉淀I只有Al(OH)3
按要求填空:
-
(1) 明矾可用于净水,原因是
 用离子方程式表示
用离子方程式表示  。
。
-
(2) 把
 溶液蒸干、灼烧,最后得到的主要固体产物是。
溶液蒸干、灼烧,最后得到的主要固体产物是。
-
(3)
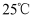 时,
时, 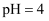 的盐酸中水的电离程度
的盐酸中水的电离程度  填“大于”、“小于”或“等于”
填“大于”、“小于”或“等于” 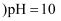 的
的 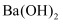 溶液中水的电离程度。
溶液中水的电离程度。
-
(4) 已知常温下,
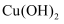 的溶度积常数为
的溶度积常数为 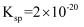 ,已知常温下某
,已知常温下某 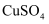 溶液里
溶液里  浓度为
浓度为 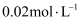 ,如果要生成
,如果要生成 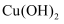 沉淀,则应调整溶液pH大于。
沉淀,则应调整溶液pH大于。
-
(5) 向含有AgI的饱和溶液中:
①加入固体
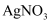 ,则
,则 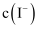
 填“变大”、“变小”或“不变”,下同
填“变大”、“变小”或“不变”,下同  。
。②若改加AgCl固体,则
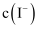 ,而
,而  。
。 -
(6) 常温下,将浓度为
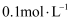 某一元酸HA和浓度为
某一元酸HA和浓度为  溶液等体积混合,混合后所得溶液的
溶液等体积混合,混合后所得溶液的 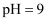 ,混合溶液中由水电离出的
,混合溶液中由水电离出的 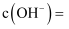
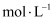 。写出该混合溶液中下列算式的精确结果
。写出该混合溶液中下列算式的精确结果 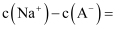
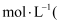 不能近似处理
不能近似处理 
NaHSO4溶于水时和熔融态下电离方式有所不同,向NaHSO4溶液中分别加入下列物质,有气体生成的是( )
A . NaHCO3
B . Ba(OH)2
C . BaCl2
D . CuO
下列反应的化学方程式或离子方程式书写正确的是( )
A . 氢氧化钡溶液与硫酸铜溶液反应:Ba2++  =BaSO4↓
B . CH4在光照条件下与Cl2反应:CH4+Cl2
=BaSO4↓
B . CH4在光照条件下与Cl2反应:CH4+Cl2 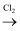 CH3Cl+HCl
C . 向氯化铝溶液中滴加过量氢氧化钠溶液:Al3++3OH-=Al(OH)3↓
D . 碳酸钙溶于盐酸:
CH3Cl+HCl
C . 向氯化铝溶液中滴加过量氢氧化钠溶液:Al3++3OH-=Al(OH)3↓
D . 碳酸钙溶于盐酸:  +2H+=H2O+CO2↑
+2H+=H2O+CO2↑
 =BaSO4↓
B . CH4在光照条件下与Cl2反应:CH4+Cl2
=BaSO4↓
B . CH4在光照条件下与Cl2反应:CH4+Cl2 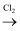 CH3Cl+HCl
C . 向氯化铝溶液中滴加过量氢氧化钠溶液:Al3++3OH-=Al(OH)3↓
D . 碳酸钙溶于盐酸:
CH3Cl+HCl
C . 向氯化铝溶液中滴加过量氢氧化钠溶液:Al3++3OH-=Al(OH)3↓
D . 碳酸钙溶于盐酸:  +2H+=H2O+CO2↑
+2H+=H2O+CO2↑
工业上常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。某课外兴趣小组拟从上述腐蚀废液中(含FeCl3、FeCl2、CuCl2)回收铜,并重新获得FeCl3溶液,设计流程如下:
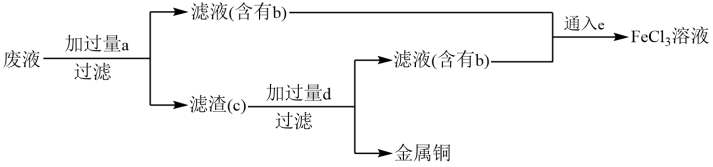
回答下列问题:
-
(1) 写出FeCl3溶液与金属铜发生反应的离子方程式: 。
-
(2) 检验废液中Fe3+存在的试剂是,证明Fe3+存在的现象是。
-
(3) 经检验知废液中仍有Fe3+存在。
①废液中加入过量a,发生的化学反应方程式为;
②过滤操作中需要使用的玻璃仪器有烧杯、;滤渣c的成分为。
-
(4) 写出b与e反应的化学方程式:。
最近更新
- 如图所示,用两根同样长的细绳把两个带同种电荷的小球悬挂在一点,A球的质量大于B球的质量,两球静止时,悬线与竖直线的偏角分
- 2009年是中国60年大庆。而在建国50周年大庆期间,山西太原市放置在主要街道的100多万盆鲜花。竞有22万多盆受到损坏
- 一位著名的宗教界人士说:“美国有办法抓住和绞死伊拉克的前总统萨达姆,但无法拿掉萨达姆在被法庭宣布死刑的那一刻还高举着的《
- 如图,AB是⊙O的直径,CD是⊙O的切线,切点为D,CD与AB的延长线交于点C,∠A=30°,给出 下面3个结论:①AD
- 在平直公路上,自行车与同方向行驶的一辆汽车同时经过某一个路标,它们的位移s(米),随时间t(秒)的变化规律为:汽车,自行
- 作简谐运动的物体,回复力和位移的关系图是下图所给四个图象中的( )
- 下列自然现象与太阳辐射无关的是 A.生物的形成 B.大气和水体的运动 C.煤、石油的形成 D.火山的喷发
- 关于光是电磁波,下列论述中正确的是A.法拉第首先从理论上得出了电磁波的传播速度和实验测得的光速相同B.赫兹用实验测定并计
- 60g铁、镁、锌混合物与足量的稀硫酸充分反应后得到混合溶液,蒸干得到156g固体.则反应产生的氢气质量为() A.2.0
- 下列词语中,有错别字的一组是 A、叠起 高潮迭起 勉励 厉兵抹马 B、辐射 幅员辽阔 退化 蜕化
- 一个通电螺线管两端磁极的极性决定于A.螺线管的匝数 B.通过螺线管的电流方向C.螺线管内有无铁芯
- 正常男性体细胞的染色体组成是( ) A.23对+X B.23对+Y C.22对+XX D.22
- A、B两颗绕地球做匀速圆周运动的人造卫星的轨道半径之比rA : rB=1: 2,设两者绕地球运行的周期分别为TA、TB,
- 某非金属单质A和氧气发生化合反应生成B,B为气体,其体积是反应掉氧气体积的两倍(同温同压)。关于B分子组成的推测一定正确
- 实现山东由经济大省向经济强省的跨越,需要创造经济发展的新优势。大力推进由主创新,把自主创新作为山东发展战略的核心,作为提
- 大气中直径小于或等于2.5微米的固体颗粒物称为PM2.5,它容易诱发呼吸道疾病。2012年2月,国务院发布了新的《环境空
- 晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下: ①高温下用碳还原二氧化硅制得粗硅③SiHCl3与过量H2在1 0
- 阅读下面这首词,回答后面的问题(共8分): 虞美人 李煜 风回小院庭芜绿,柳眼春相续。凭阑半日独无言,依
- 读图完成4-6题 4.有关M.N两处地形,已知a>b下列叙述正确叙述是 ①M为山坡上的洼地 ②N为山坡上
- 下列说法正确的是()A. 所有原子的原子核都是由质子和中子构成 B. 在同一种物质中同种元素的化合价可能不相同 C. 由



