第一章 物质及其变化 知识点题库
 中的几种,请填写下列空白:
中的几种,请填写下列空白:
-
(1) 不用做任何实验就可以肯定原溶液中不存在的离子是。
-
(2) 取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是。
-
(3) 取(2)中滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有,写出加入氢氧化钠溶液发生的离子方程式:,。
-
(4) 原溶液中可能大量存在的阴离子是___(填字母)。A . Cl- B . NO
 C . CO
C . CO 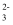 D . OH-
D . OH-
 、NO
、NO  。现进行如下检验:
。现进行如下检验:
-
(1) 不用做任何实验,就可以排除的离子是
-
(2) 用红色石蕊试纸检验,试纸变蓝色,可确定溶液中一定存在的离子是,同时排除的离子是
-
(3) 另取少量溶液逐滴滴加盐酸至过量,无气体放出,由此可以确定溶液中无
-
(4) 另取少量溶液用硝酸酸化后,加入AgNO3溶液有白色沉淀生成,写出反应的离子方程式
②CuSO4溶液和BaCl2溶液混合,反应的离子方程式为,恰好反应后,过滤后溶液的溶质为(填化学式)。
 ,下列说法正确的是( )
,下列说法正确的是( )
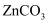 在反应中失去电子
C . 还原剂与氧化剂的物质的量之比为1∶2
D . 氧化产物与还原产物的物质的量之比为1∶1
在反应中失去电子
C . 还原剂与氧化剂的物质的量之比为1∶2
D . 氧化产物与还原产物的物质的量之比为1∶1

-
(1) 沸腾炉中发生反应的化学方程式为4FeS2+11O2
 2Fe2O3+8SO2 , 该反应被氧化的元素是(填元素名称)。
2Fe2O3+8SO2 , 该反应被氧化的元素是(填元素名称)。
-
(2) 利用Fe2O3废渣(俗称“红砂”)制备废水除砷剂的第一步是将“红砂”与硫酸混合,该步反应的化学方程式为。
-
(3) 从接触室出来的混合气体中含有SO2、SO3、O2、N2等气体,设计一个实验方案证明其中含有SO2:。
-
(4) 有些反应中物质浓度不同,性质也不同。浓硫酸有三大特性:吸水性、脱水性、强氧化性。则加热时浓硫酸与木炭反应的化学方程式为。
-
(5) 将一定量锌与100mL18mol/L 浓硫酸充分反应后,若锌完全溶解同时产生气体0.8mol, 将反应后的溶液稀释得400mL,测得c(H+)=2mol/L,则产生气体中SO2 物质的量为mol。
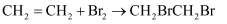 B . 乙醇在铜催化下氧化:
B . 乙醇在铜催化下氧化: 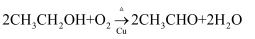 C . 氯化铵水解的离子方程式:
C . 氯化铵水解的离子方程式: 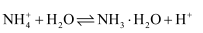 D . 碳酸氢钠在水中的电离方程式:
D . 碳酸氢钠在水中的电离方程式: 
 B . Cu
C .
B . Cu
C .  D .
D . 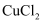
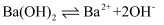 B . 钢铁发生吸氧腐蚀时的正极反应:
B . 钢铁发生吸氧腐蚀时的正极反应: 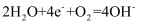 C . Na2S水解的离子方程式:
C . Na2S水解的离子方程式: 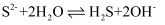 D . 电解NaCl溶液的离子方程式:
D . 电解NaCl溶液的离子方程式: 
 ,还含有
,还含有 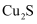 、
、 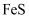 等)。一种以黝锡矿为原料提取锡的工艺流程如图所示:
等)。一种以黝锡矿为原料提取锡的工艺流程如图所示: 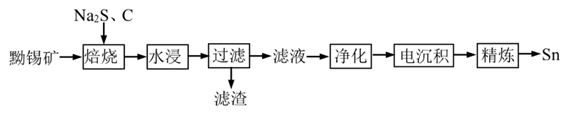
已知:“滤液”中含有的主要离子为 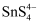 、
、 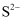 、
、  等。
等。
回答下列问题:
-
(1) “焙烧”过程中主要发生的反应为
 。
。 ①
 中
中 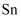 元素的化合价为。
元素的化合价为。②在反应物中加入
 粉的最主要目的是(填标号)。
粉的最主要目的是(填标号)。A.提供能量 B.防止
 被氧化 C.防止结块
被氧化 C.防止结块③加入的
 的量应为黝锡矿量的2.1倍,结合图示说明其原因。
的量应为黝锡矿量的2.1倍,结合图示说明其原因。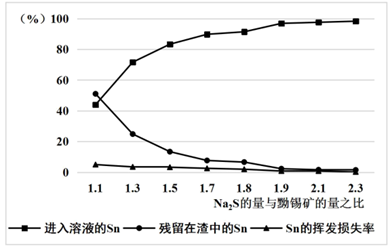
-
(2) “滤渣”中可回收的金属是(填元素符号)。
-
(3) 若黝锡矿中含有
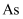 元素,则“净化”时需加入
元素,则“净化”时需加入 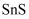 ,将
,将  转化为单质
转化为单质 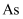 除去,发生反应的离子方程式为
除去,发生反应的离子方程式为  ,该过程可看作经历以下两步反应:
,该过程可看作经历以下两步反应: 第一步:

第二步:
-
(4) “电沉积”时,采用惰性电极作阳极,纯锡作阴极,
 溶液和“净化”后溶液(主要含
溶液和“净化”后溶液(主要含 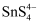 、
、  等)分别为两极区的电解液,选用阳离子交换膜。
等)分别为两极区的电解液,选用阳离子交换膜。 ①“净化”后溶液应作(填“阳极区”或“阴极区”)电解液。
②“电沉积”过程中,阳极区溶液的
 (填“增大”或“减小”或“不变”)。
(填“增大”或“减小”或“不变”)。③“电沉积”结束后,阴极区溶液的主要溶质为(填化学式)。
回答下列问题:
-
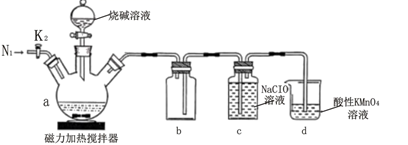
(1) 在a中加入黄磷、活性炭粉末,打开K1 , 通入N2一段时间,关闭K1 , 打开磁力加热搅拌器,滴加烧碱溶液。
①活性炭粉末作为黄磷的分散剂,目的是
②a中反应的化学方程式为
-
(2) 反应结束后,打开K1 , 继续通入N2 , 目的是d的作用是
-
(3) c中生成 NaH2PO2和NaCl,c中反应的离子方程式为;相关物质溶解度(S)如下:
s(25℃ )
s(100℃ )
NaCl
37
39
NaH2PO2
100
667
充分反应后,将a、c中溶液混合,将混合液(含极少量NaOH)蒸发浓缩,有大量晶体析出,该晶体主要成分的化学式为,然后,再冷却结晶、过滤、洗涤、干燥,得到含NaH2PO2的粗产品。
-
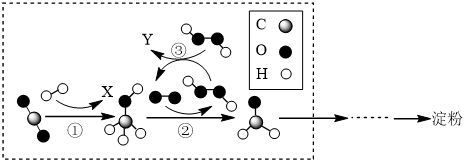
(4) 产品纯度测定:
取产品1.50克配成250mL溶液,取25mL于锥形瓶中,酸化后加入25mL,0.10mol/L碘水,于暗处充分反应后,以淀粉溶液做指示剂,用0.10 mol/L Na2S2O3溶液滴定至终点,平均消耗18.00mL,相关反应方程式为:H2PO
 +H2O+I2=H2PO
+H2O+I2=H2PO  +2H++2I- , 2S2O
+2H++2I- , 2S2O  +I2=S4O
+I2=S4O 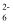 +2I-。产品纯度为
+2I-。产品纯度为
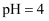 的NaHSO3溶液中,
的NaHSO3溶液中, B .
B . 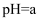 的醋酸或盐酸分别稀释10倍的pH均为
的醋酸或盐酸分别稀释10倍的pH均为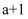 C .
C . 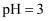 的盐酸与
的盐酸与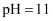 的氨水以任意比例混合后,溶液中
的氨水以任意比例混合后,溶液中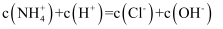 D . 向
D . 向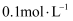 的氨水中加入少量水,溶液中
的氨水中加入少量水,溶液中 减小
减小
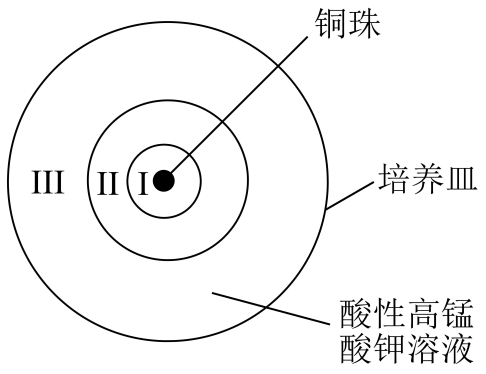
实验 | 现象 |
| 一段时间后,培养皿中由铜珠向外侧依次呈现: Ⅰ区澄清且紫色褪色明显 Ⅱ区底部覆盖棕黑色固体 Ⅲ区澄清且紫色变浅 |
已知:MnO2是棕黑色固体。下列说法不正确的是( )
 +16H+=5Cu2++2Mn2++8H2O
B . Ⅱ区棕黑色固体是由铜和酸性高锰酸钾反应产生还原产物
C . Ⅲ区紫色变浅说明在Ⅲ区MnO
+16H+=5Cu2++2Mn2++8H2O
B . Ⅱ区棕黑色固体是由铜和酸性高锰酸钾反应产生还原产物
C . Ⅲ区紫色变浅说明在Ⅲ区MnO 的浓度减小,是因为离子扩散作用
D . 如果酸性高锰酸钾过量很多,所有反应完全后,产物中可能没有Mn2+
的浓度减小,是因为离子扩散作用
D . 如果酸性高锰酸钾过量很多,所有反应完全后,产物中可能没有Mn2+
化学式 | CH3COOH | H2CO3 | H2SO3 |
Ka | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.0×10-7 |
下列说法正确的是( )
 )+c(HSO
)+c(HSO )+2c(CO
)+2c(CO )+c(HCO
)+c(HCO )-0.1
B . 25℃时,0.1mol·L-1Na2SO3溶液的pH约等于10(忽略二级水解和H2O的电离)
C . 25℃时,0.1mol·L-1CH3COONa溶液中通入HCl气体,至pH=7(溶液体积变化忽略不计):c(Na+)>c(Cl-)>c(CH3COOH)
D . 足量CH3COOH与Na2SO3溶液反应的化学方程式为:2CH3COOH+Na2SO3=2CH3COONa+SO2↑+H2O
)-0.1
B . 25℃时,0.1mol·L-1Na2SO3溶液的pH约等于10(忽略二级水解和H2O的电离)
C . 25℃时,0.1mol·L-1CH3COONa溶液中通入HCl气体,至pH=7(溶液体积变化忽略不计):c(Na+)>c(Cl-)>c(CH3COOH)
D . 足量CH3COOH与Na2SO3溶液反应的化学方程式为:2CH3COOH+Na2SO3=2CH3COONa+SO2↑+H2O
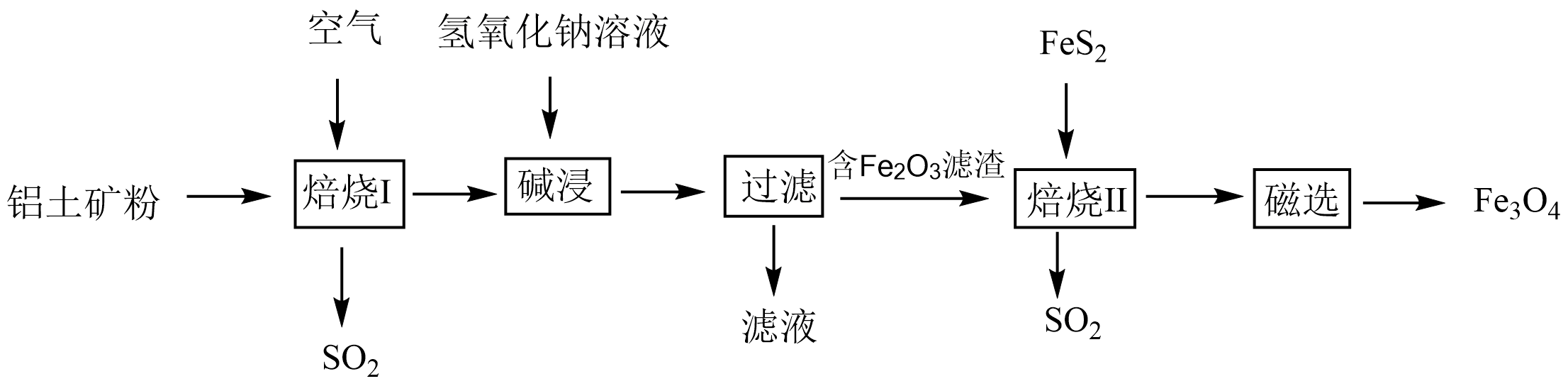
下列说法正确的是( )
 +H2O
C . 滤液中通入足量CO2 , 过滤后可得到Al2O3
D . 无氧条件下进行“焙烧II”时,理论上消耗的n(FeS2):n(Fe2O3)=1:16
+H2O
C . 滤液中通入足量CO2 , 过滤后可得到Al2O3
D . 无氧条件下进行“焙烧II”时,理论上消耗的n(FeS2):n(Fe2O3)=1:16
 与
与 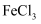 溶液的反应。
溶液的反应。
-
(1) 实验一:用如图所示实验装置制备
 ,并将足量
,并将足量  通入
通入 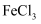 溶液中,溶液迅速变为血红色;停止通入气体,将血红色溶液密闭放置5小时后,溶液变为浅绿色。
溶液中,溶液迅速变为血红色;停止通入气体,将血红色溶液密闭放置5小时后,溶液变为浅绿色。 
制备
 的化学反应方程式为;
的化学反应方程式为; -
(2) 仪器a的名称为,按图示装好药品后,打开K之前的操作是。
-
(3) 某同学取适量酸性
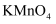 于试管中,滴入几滴血红色溶液,溶液的紫色褪去,据此推断血红色溶液中含有Fe2+。此结论(填“正确”、“不正确”),理由是。
于试管中,滴入几滴血红色溶液,溶液的紫色褪去,据此推断血红色溶液中含有Fe2+。此结论(填“正确”、“不正确”),理由是。
-
(4) 实验二:探究血红色溶液产生的原因
实验过程如下表:
实验序号
假设
实验内容
结论
①
与溶液中c(H+)有关
取适量上述血红色溶液,滴入Y溶液,溶液又变为黄色
假设不成立
②
与c(H2SO3)或c(SO2)有关
1溶液中,滴入1mol/LNaHSO3溶液,溶液呈血红色,再逐滴滴入HCl溶液,出现×××现象
假设不成立
③
与c(
 )或c(
)或c(  )有关
)有关在FeCl3溶液中加入Na2SO3溶液,立即变为血红色。
实验①中,Y是(填化学式);实验②中现象是;实验③的结论是。
-
(5) 为了进—步探究血红色物质产生主要原因,又进行了以下实验:
在0.5mL1mol/L的FeCl3溶液中,加入浓度相同的Na2SO3溶液V1mL,NaHSO3溶液V2mL并混合均匀,改变V1、V2的值并维持V1+V2=4.0进行多组实验,测得混合溶液的吸光度与
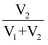 的关系如图所示。(已知吸光度越大,溶液颜色越深)。
的关系如图所示。(已知吸光度越大,溶液颜色越深)。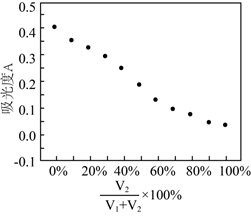
①维持V1+V2=4.0的目的是。
②该实验得出的结论是。
- 家庭厨房中常发生下列变化,其中属于物理变化的是 A.食物腐败 B. 天然气燃烧 C. 水沸腾
- 到2014年底,南充和全国多地一样,多家投资理财公司出现“跑路”的现象,涉案金额最高逾千万,民间投资借贷问题引起各方面关
- 函数的定义域为 ( )A B C D
- 18世纪,以伏尔泰为代表的启蒙思想家的思想主张在法国大革命中得到集中体现。这次革命中,资产阶级提得最多的口号是 A.“人
- 心理学实验表明,只靠耳朵听的知识,3个小时后只能记住65%左右;只靠眼睛看的知识,3个小时后可保持70%左右,3天后只能
- 在4 L密闭容器中充入6 mol A气体和5 mol B气体,在一定条件下发生反应:3A(g)+B(g)2C(g)+xD
- 同种元素的原子和离子一定相同的是 ( )A质子数 B电子数 C电子层数 D最外层电子数
- 已知关于x的方程x2-2(a-2)x+a2=0,是否存在实数a,使方程两个实数根的平方和为56?若存在,求出a的值;若不
- 已知函数 ,若,则实数取值范围是 A. () B.()
- The Olympic Games, in 776 B.C.,did not include women
- 已知cos(-α)=m(|m|≤1),求cos(π+α),sin(π-α)的值.
- 读“某海域等深线和表层年平均等温线分布图”,完成乙处洋流可能是A.加那利寒流 B.西澳大利亚寒流
- 冲动在反射弧中的传导是单方向的,其根本原因是 A.只有感受器下能感受刺激 B.只有效应器能够接受神经冲动 C.
- 高三学生小涛参加区人大代表的选举时,社区领导告诉他一定要选本社区的现任领导,小涛感到自己的基本民主权利受到侵犯,就把这个
- 以下关于生物变异的叙述,正确的是 A.基因突变都会遗传给后代 B.染色体变异产生的后代都是不育的 C.基因结构发生的改变
- 2012年9月,昆明市首家持卡消费标准化菜市场在明润菜市场正式投入运营。在该菜市场,消费者在总台购买储值卡,通过该卡可以
- Laughter produces short-term changes in the function
- New medicines and instruments ______ every day to extend lif
- 已知部分化合物的溶度积常数见下表:化学式 Ksp 化学式 Ksp AgBr 5.0×10-13 Ag2CO3 8.1×1
- 斯塔夫里阿诺斯在《全球通史》中写道:“……后的几年中,西方大规模的、似乎不可抗拒的入侵使中国的生存似乎都受到威胁,结果