第四章 剖析物质变化中的能量变化 知识点题库
 Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是( )
Na2S4+3NaBr,当闭合开关K时,X电极附近溶液变红。下列说法正确的是( )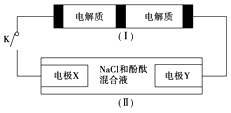
-
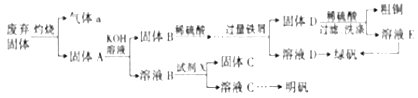
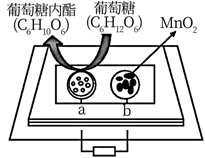
(1) 气体a是(写化学式,下同),试剂X是(已知X是一种盐),固体C是。
-
(2) 明矾可以净水,明矾净水的原理是(用离子方程式表示)。
-
(3) 利用反应2Cu+O2+2H2SO4
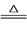 2CuSO4+2H2O可制备CuSO4 , 若将该反应设计成原电池,该电池的正极反应式为。
2CuSO4+2H2O可制备CuSO4 , 若将该反应设计成原电池,该电池的正极反应式为。
-
(4) 取少量产品绿矾,加水溶解后再滴入几滴KSCN溶液,若产品绿矾中不含有Fe3+ , 观察到的现象为;若在产品绿矾的水溶液中滴加酸性高锰酸钾溶液,观察到的现象为,原因是 (用离子方程式表示)。
-
(5) 已知绿矾受热分解的化学方程式为2FeSO4·7H2O
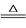 Fe2O3+SO2↑+SO3↑+14H2O。称取3.5g产品绿矾,加热分解至恒重后(杂质受热不分解),将反应所得的气体缓缓通入盛有足量蒸馏水的锥形瓶中,再用0.1000 mol·L-1的酸性KMnO4溶液滴定,滴定到终点时消耗酸性KMnO4溶液的体积为25.00mL,则产品绿矾的纯度为 (保留三位有效数字)。
Fe2O3+SO2↑+SO3↑+14H2O。称取3.5g产品绿矾,加热分解至恒重后(杂质受热不分解),将反应所得的气体缓缓通入盛有足量蒸馏水的锥形瓶中,再用0.1000 mol·L-1的酸性KMnO4溶液滴定,滴定到终点时消耗酸性KMnO4溶液的体积为25.00mL,则产品绿矾的纯度为 (保留三位有效数字)。
-
(1) 在一定温度和压强下,由最稳定单质生成1mol化合物的焓变称为该物质的摩尔生成焓。根据此定义,稳定单质的摩尔生成焓为0,某些化合物的摩尔生成焓如下表所示:
化合物
CO2
CH4
CO
摩尔生成焓(kJ·mol-1)
-395
-74.9
-110.4
CH4(g)与CO2(g)反应生成CO(g)和H2(g)的热化学方程式为
-
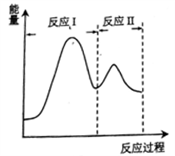
(2) 若上述反应分Ⅰ、Ⅱ两步进行,其能量曲线如图所示。则总反应的反应速率取决于反应(填“I”或“Ⅱ”)。
-
(3) 一定温度下反应:CO2(g)+CH4(g)
 2CO(g)+2H2(g)的平衡常数表达式Kp= (用平衡分压p代替平衡浓度表示)
2CO(g)+2H2(g)的平衡常数表达式Kp= (用平衡分压p代替平衡浓度表示)
-
(4) 在压强为p1、p2、p3的三个恒压密闭容器中分别通入1.0molCH4(g)与1.0mol CO2(g ), 发生反应:CO2(g)+CH4(g)
 2CO(g)+2H2(g).测得平衡时CH4的体积分数与温度、压强的关系如图所示。
2CO(g)+2H2(g).测得平衡时CH4的体积分数与温度、压强的关系如图所示。 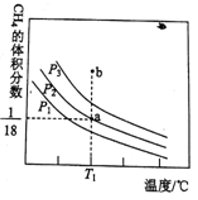
① a点时CH 4的转化率为
② 压强p 1、p 2、p 3由大到小的顺序为,判断理由是。温度为T l℃、压强为P 3时,b点处v(正) v(逆)(填“<”、“>”或“="”)
-
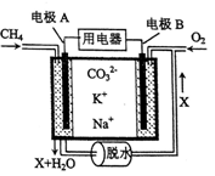
(5) 某种燃料电池以熔融碳酸钠、碳酸钾为电解质,其工作原理如图所示,该电池负极的电极反应式为.若电极B附近通入1m 3空气(假设空气中O 2的体积分数为20% )并完全反应,理论上可消耗相同条件下CH 4的体积为m3
-
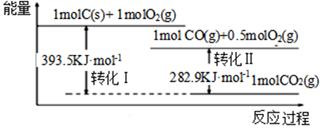
(1) FeSO4可转化为FeCO3 , FeCO3在空气中加热可制得铁系氧化物材料。已知25℃,101kPa时:4Fe(s)+3O2(g)
=2Fe2O3(s)ΔH=-1648kJ/mol,C(s)+O2(g)=CO2(g) ΔH=-393kJ/mol,2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ΔH=-1480kJ/mol,FeCO3在空气中加热反应生成Fe2O3的热化学方程式为。
-
(2) 一定条件下,向容积可变的密闭容器中通入N2和H2 , 发生反应:N2(g)+3H2(g)
 2NH3(g) ΔH<0达到平衡后,试回答下列问题:
2NH3(g) ΔH<0达到平衡后,试回答下列问题: ①达到平衡后,若其它条件不变,把容器体积缩小一半,平衡将(填“向逆反应方向”、“向正反应方向”或“不”)移动,平衡常数K将 (填“增大”、“减小”或“不变”)。
②达到平衡后,在恒压条件下,向容器中通入氦气(He),氮气的转化率将(填“增大”、“减小”或“不变”)。
-
(3) AlCl3溶液加热蒸干并灼烧最终得到物质是(填化学式),将NaHCO3与Al2 (SO4)3溶液混合后可做泡沫灭火剂,其原理是(用离子方程式表示)。
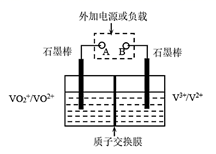
已知:
①溶液呈酸性且阴离子为SO42-;
②溶液中颜色:V3+绿色,V2+紫色,VO2+黄色,VO2+蓝色;
③放电过程中,右槽溶液的颜色由紫色变成绿色。
下列说法不正确的是( )
| 序号 | 液体 | 固体 | 混合前温度 | 混合后最高温度 |
| ① | 35 mL水 | 2.5 g NaHCO3 | 20 ℃ | 18.5 ℃ |
| ② | 35 mL水 | 3.2 g Na2CO3 | 20 ℃ | 24.3 ℃ |
| ③ | 35 mL盐酸 | 2.5 g NaHCO3 | 20 ℃ | 16.2 ℃ |
| ④ | 35 mL盐酸 | 3.2 g Na2CO3 | 20 ℃ | 25.1 ℃ |
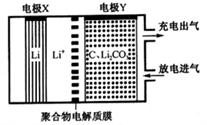
下列有关说法正确的是( )
-
(1) 已知:反应CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是(填字母)。
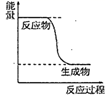
a CH3OH转变成H2的过程是一个吸收能量的过程
b H2的生成速率与CH3OH的消耗速率之比为1:2
c 化学变化不仅有新物质生成,同时也一定有能量变化
d 1molH-O键断裂的同时2molC=O键断裂,则反应达最大限度
-
(2) 某温度下;将5molCH3OH和2molO2充入2L的密闭容器中,经过4 min反应达到平衡,测得c(O)=0.2mol·L-1 , 4 min内平均反应速率v( H2)= .则CH3OH的转化率为
-
(3) 已知CO2分子中所有原子的最外层均满足8电子稳定结构,请写出CO2的电子式
-
(4) CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为CH3OH+ 8OH--6e-=CO
 +6H2O。则下列说法正确的是(填序号)。
+6H2O。则下列说法正确的是(填序号)。 ①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4 g CH3OH转移1.2 mol电子
-
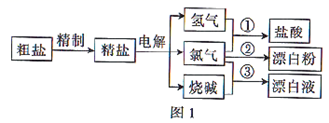
(1) 粗盐中含有
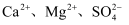 等杂质离子,欲用
等杂质离子,欲用 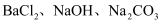 、盐酸进行精制,则这些试剂的加入顺序依次为
、盐酸进行精制,则这些试剂的加入顺序依次为  、、、。
、、、。
-
(2) 工业中制取漂白粉时是将氯气通入(填“澄清石灰水”或“石灰乳”)中,理由是。
-
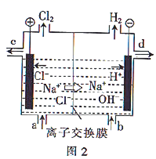
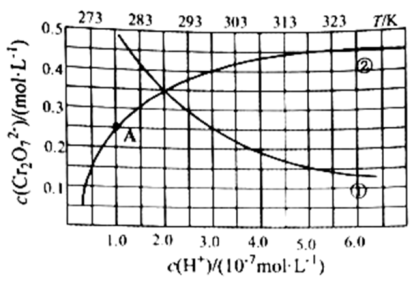
(3) 图2为离子交换膜法电解食盐水的示意图,离子交换膜的作用为、。
-
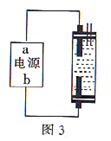
(4) 某化学课外小组用图3所示的简易装置制取“84”消毒液,则a为电源的极,阳极上的电极反应式为,生成次氯酸钠的离子方程式为。
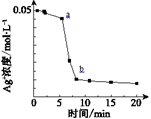
| 操作 | 现象 | Ag+ 浓度变化曲线 | |
| 实验Ⅰ | 向1 mL 0.1 mol/L FeSO4溶液中加入1 mL 0.1 mol/L AgNO3溶液 | 几分钟后,出现大量灰黑色浑浊 | |
| 实验Ⅱ | 先向试管中加入几滴Fe2(SO4)3溶液,然后重复实验Ⅰ的操作 | 现象与实验Ⅰ相同 |
(已知:Ag2SO4为白色微溶物;反应过程中测得温度几乎无变化)
下列说法正确的是( )
-
(1) 某ClO2泡腾片的有效成分为NaClO2 , NaHSO4 , NaHCO3 , 其溶于水时,NaClO2和NaHSO4反应生成ClO2和Cl- , 并逸出大量气体,逸出气体的主要成分是(填化学式)。
-
(2) 测定某水样中ClO
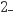 浓度可采用氧化还原滴定法:量取25.00mL水样于碘量瓶中,加水稀释至50.00mL,加入过量KI,再滴入适量稀硫酸,充分反应后,滴加1mL淀粉溶液,用0.01000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。
浓度可采用氧化还原滴定法:量取25.00mL水样于碘量瓶中,加水稀释至50.00mL,加入过量KI,再滴入适量稀硫酸,充分反应后,滴加1mL淀粉溶液,用0.01000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。已知:ClO
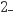 +4I−+4H+=2H2O+2I2+Cl− , I2+2S2O
+4I−+4H+=2H2O+2I2+Cl− , I2+2S2O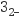 =2I−+S4O
=2I−+S4O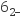
①滴定终点的现象是:。
②下列关于滴定分析的操作,不正确的是。
A.用量筒量取25.00mL水样
B.滴定时要适当控制滴定速度
C.装标准溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失,造成测定结果偏低
D.终点读数时俯视滴定管液面,会造成测定结果偏低
E.再次滴定时,须重新装液并调节液面至“0”刻度或“0”刻度以下
③计算水样中ClO
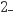 的浓度
的浓度 -
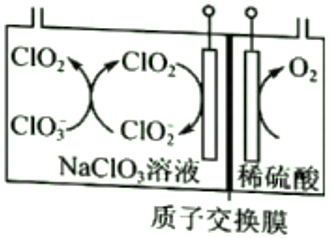
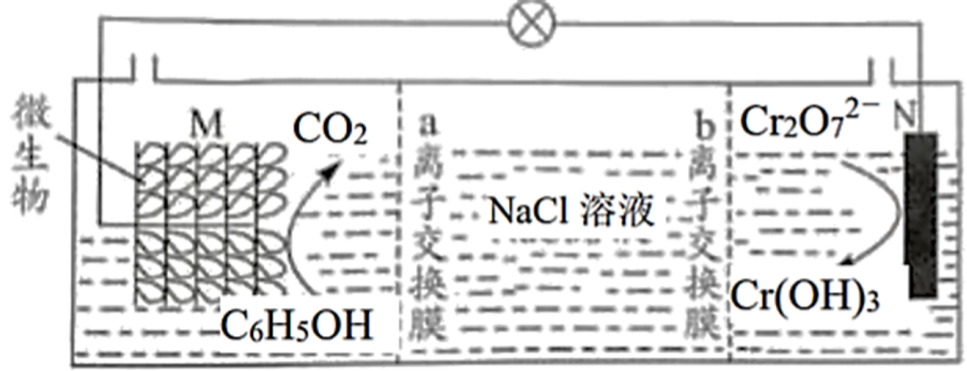
(3) ClO2可用隔膜电解NaClO3制备,装置如图所示。制备时先在NaClO3溶液中通入少量ClO2气体,写出阴极上的电极反应式:。
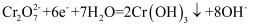
-
(1) 基态Cr原子的核外电子排布式为。
-
(2) CrO
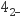 (黄色)和Cr2O
(黄色)和Cr2O
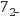 (橙色)在溶液中可相互转化。
(橙色)在溶液中可相互转化。
①用离子方程式表示Na2CrO4溶液加酸的转化反应。
②随着溶液pH降低,CrO
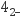 的平衡转化率(填“增大”“减小”或“不变”)。
的平衡转化率(填“增大”“减小”或“不变”)。③加水稀释Na2CrO4溶液,下列说法正确的是(选填序号)。
A.c(CrO
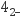 )+2c(Cr2O
)+2c(Cr2O
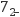 )=c(Na+) B.比值
)=c(Na+) B.比值
 逐渐增大
逐渐增大C.溶液中所有离子的浓度均减小 D.平衡常数K保持不变
-
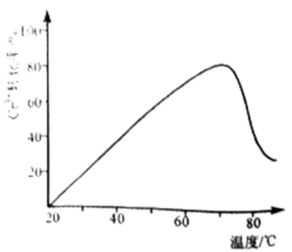
(3) Cr3+、双氧水与Pb2+作用可合成颜料铬黄(PbCrO4)。控制其他条件不变,反应温度对Cr3+转化率的影响如图所示.温度超过70℃时,Cr3+转化率下降的原因是。
-
(4) 控制Na2CrO4初始浓度为1.0mol·L-1 , 测定在室温下c(Cr2O
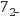 )随c(H+)的等温变化曲线、在H+恒定下c(Cr2O
)随c(H+)的等温变化曲线、在H+恒定下c(Cr2O
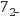 )随温度T的等pH变化曲线,结果如图所示。
)随温度T的等pH变化曲线,结果如图所示。
①等温变化曲线是(填曲线序号) 。
②结合题给信息,(填“升温”或“降温”)可使溶液橙色变深。
③根据A点数据,计算反应的平衡常数。
-
(5) 电解铬酸钾溶液制备重铬酸钾的装置示意图如图:
①该制备过程总反应的化学方程式为。
②电解一段时间后,阳极区溶液中的K+的物质的量由amol变成bmol,则生成的重铬酸钾的物质的量为mol。
选项 | 生活应用或生产活动 | 化学知识 |
A | 用二氧化碳跨临界直接制冰 | 液态二氧化碳汽化时吸热 |
B | 用小苏打焙制糕点 |
|
C | 用 |
|
D | 丙三醇可用于配制化妆品 | 丙三醇与水形成氢键,有很强的保湿性 |
反应ⅠCH4(g)+CO2(g)=2CO(g)+2H2(g) △H=247.3kJ•mol-1
反应ⅡCO2(g)+2H2(g)=CO(g)+H2O(g) △H=41.0kJ•mol-1
-
(1) 将一定最CH4与CO2充入密闭容器中,若仅发生上述两个反应,则反应达到平衡的标志是____(填序号)。A . 恒温恒容条件下,气体的密度不变 B . 恒温恒容条件下,气体的压强不变 C . 恒温恒容条件下,CO和H2的浓度相等 D . 绝热恒容条件下,反应体系的温度不变
-
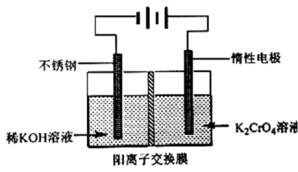
(2) 反应III为CH4(g)+CO2(g)=4CO(g)+2H2O(g),该反应的△H=kJ•mol-1 , 平衡常数表达式为K=。
-
(3) 图1为反应温度、进料
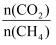 对反应出口合成气中
对反应出口合成气中 的影响。
的影响。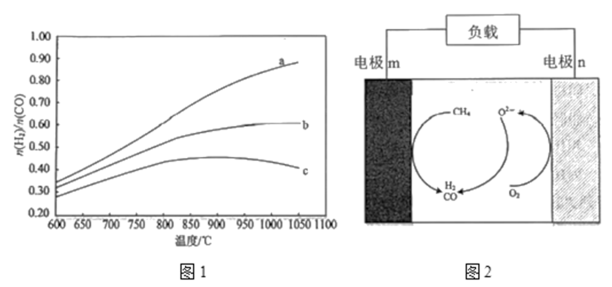
①850℃时,图1中曲线a、b、c所示
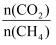 由大到小的关系是,理由是。
由大到小的关系是,理由是。②当温度大于850℃时,曲线c出现如图变化的原因可能是。
-
(4) 固体氧化物燃料电池利用CH4为原料,直接在电极上氧化合成CO、H2。其反应原理如图2所示,写出电极m上发生反应的电极方程式;若电极m上通入CH4的速率过快或过慢均会使CO、H2产率降低。其原因是。
 催化加氢可缓解
催化加氢可缓解 对温室效应的影响,其原理为:
对温室效应的影响,其原理为:Ⅰ.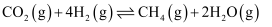
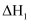
Ⅱ.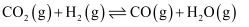
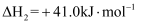
-
(1) 已知
 的燃烧热为
的燃烧热为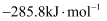 ,
,  的燃烧热为
的燃烧热为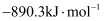 ,
, 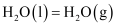
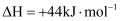 , 则
, 则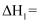
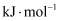 。
。
-
(2) 反应Ⅱ中,正反应速率
 , 逆反应速率
, 逆反应速率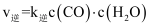 , 其中
, 其中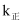 、
、 分别为正、逆反应速率常数,仅受温度影响。图1(
分别为正、逆反应速率常数,仅受温度影响。图1(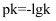 , T表示温度)所示a、b、c、d四条斜线中,有两条分别为
, T表示温度)所示a、b、c、d四条斜线中,有两条分别为 和
和 随T变化斜线,则表示
随T变化斜线,则表示 随T变化关系的斜线是。
随T变化关系的斜线是。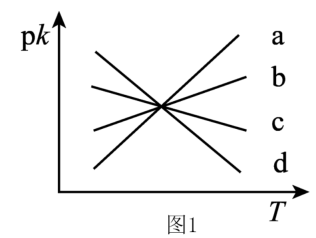
-
(3) 在0.1MPa下,将
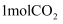 和
和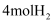 充入2L刚性密闭容器中,反应相同时间,温度对
充入2L刚性密闭容器中,反应相同时间,温度对 转化率如图2所示,温度对含碳物质的平衡产率的影响如图3所示。
转化率如图2所示,温度对含碳物质的平衡产率的影响如图3所示。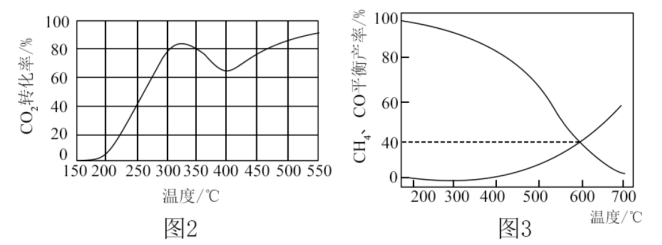
①试解释
 转化率在高于325℃时,随温度升高先减小后增大的原因。
转化率在高于325℃时,随温度升高先减小后增大的原因。②当
 和CO平衡产率均为40%时,该温度下反应Ⅱ的平衡常数
和CO平衡产率均为40%时,该温度下反应Ⅱ的平衡常数 为。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
为。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数) -
(4) 在1MPa下,将
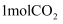 和
和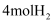 充入2L刚性密闭容器中,在图3中画出
充入2L刚性密闭容器中,在图3中画出 平衡产率的变化趋势。
平衡产率的变化趋势。
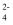 等杂质,其提纯过程一般经过以下流程:
等杂质,其提纯过程一般经过以下流程: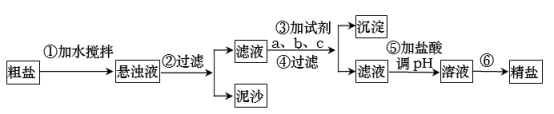
下列说法错误的是( )
- 已知二氯苯的同分异构体有三种,从而可推知四氯苯的同分异构体的数目是( ) A.1 B.2
- 有甲乙两个实心正方形铁块,边长之比为1:2,则甲乙两铁块的密度之比为_______,质量之比为________。
- (6分)以下是一些常见物质间互相转化的关系图(有些反应条件未注明)(1)将固体A充分加热至不产生气体,写出发生反应的化学
- “自……,而物竞天择之理,厘然当于人心,而中国民气为之一变。”“大忧乎今日之中国,方为世界竞争之中心点,优胜劣败之公例,
- 哥伦布在自己的航海日记中写道:“当地居民都跑来岸边……有人给我们送来淡水,有人给我们送来食物。”这里的“当地居民”是
- 下列熟语中有错别字的一项是 A.打折扣 煞风景 黄钟毁弃,瓦斧雷鸣 树犹如此,人何以堪 B.大锅
- With the government’s aid, those ________ by the earthquake
- 下列各句中。没有语病的一句是(3分)( ) A.人们通过网络进行搜索无可非议,关键是当网络搜索上升为“人肉搜索”时,
- (08年北京五中期中)(4分)如图所示,在竖直平面内有一条圆弧形轨道AB,其半径为1m,B点的切线方向恰好为水平方向,一
- 用公式法解方程: .
- 吊在室内天花板的电风扇重G,静止时固定杆对它的拉力为F1,当风扇叶片水平转动起来后,杆对它的拉力为F2,则
- 中英《南京条约》中最能反映英国侵略的本质意图是( ) A、割香港岛 B、赔款
- 同志参观某纪念馆亲笔题写了“军旗升起的地方”,你认为这一题词应该出现在 A.井冈山纪念馆
- 我国古代科学技术的主要特点是( ) A.政府是科学研究的主要组织者 B.实用技术发达 C.普遍重
- 路桥是指横贯大陆的铁路运输通道。根据有关理论,世界经济格局正在从“海岸经济”进入“路桥经济”阶段。读“亚欧大陆桥示
- 作文 不同的人生有不同的美丽,不同的视角可以看出不同的美丽。有人说亲情的温暖很美丽,同学的友谊也美丽。也有人说小草也美丽
- 下列关于细胞分裂、分化、衰老和凋亡的叙述,正确的是 A.细胞分化使各种细胞的遗传物质发生改变 B.细胞的
- (本题满分14分) 已知直三棱柱D是AB的中点. (1)求证:CD⊥平面ABB1A1; (2)求二面角D—A1C—A的正
- 2009年12月25日重庆日报报道 在“2010年全市发展改革工作会”上,市发改委副主任沈晓钟说,“备受关注的重庆至
- 1689年,洛克在《政府论》中指出:“人人放弃其自然法的执行权而把它交给公众,……这样,就授权社会,或者授权给社会的立法
 受热易分解生成气体
受热易分解生成气体 溶液蚀刻电路板上的铜
溶液蚀刻电路板上的铜


