2.2 海水中的氯 知识点题库
设NA为阿伏加德罗常数的值.下列说法中,正确的是( )
A . 标准状况下,22.4L的NO2和CO2混合气体中含有的氧原子数为4NA
B . 密闭容器中,46gNO2和N2O4的混合气体所含分子个数为NA
C . 常温常压下,22.4L的液态水含有2.24×10﹣8NA个OH﹣
D . 高温下,16.8 g Fe与足量水蒸气完全反应失去0.8NA个电子
化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等都离不开化学.
-
(1) 硅是无机非金属材料的主角.请你举出两种含硅的材料名称、;铝制品表面因有一层氧化铝薄膜而经久耐用,但该氧化膜易被酸、碱破坏.若将氧化铝与氢氧化钠溶液作用,反应的离子方程式为.
-
(2) 氯气用于漂白时,实际上起漂白作用的物质不是Cl2而是它和水反应生成的(写化学式).缺铁性贫血患者补充的铁,通常以硫酸亚铁的形式,而硫酸铁则没有这种药效.当用硫酸亚铁制成药片时外表要包有一层特殊的糖衣,这层糖衣的作用是.
-
(3) 从降低成本和减少环境污染的角度考虑,制取硫酸铜最好的方法是 (填字母).A . 铜和浓硫酸反应 B . 铜和稀硫酸反应 C . 氧化铜和稀硫酸反应 D . 铜与Fe2(SO4)3溶液反应.
实验室制取氯气如图,连接好实验装置.
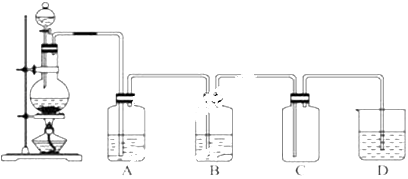
请回答下列问题:
-
(1) 图中气体发生装置中盛放浓盐酸的仪器名称是其中发生反应的离子方程式为;
-
(2) A中盛放的是,其作用为.
-
(3) B中盛放的是,其作用为.
-
(4) D中盛放的是,化学反应方程式.
饮用水质量是关系人类健康的重要问题.
-
(1) 氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为.
-
(2) 写出工业上制取漂白粉的化学反应方程式:.
-
(3) ClO2被称为“第四代”饮用水杀虫剂,因其高效率,无污染而被广泛使用.制备ClO2是发达国家普遍重视的课题,我国北京永利科技有限公司已用电解法批量生产ClO2 . 其反应原理为:4ClO3﹣+4H+═4ClO2+O2↑+2H2O,则氧化剂:;还原剂:.
-
(4) 相同物质的量的氯气与二氧化氯消毒时转移电子数目之比是.
用氯气消毒过的自来水配制下列溶液时,会使所配溶液的溶质发生变化的是( )
①NaOH ②AgNO3 ③Na2CO3 ④NaBr ⑤FeCl2 .
A . 只有①②
B . 只有①④⑤
C . 只有②④⑤
D . ①②③④⑤
设NA为阿伏加德罗常数的值,下列有关叙述正确的是 ( )
A . 在标准状况下,22.4 L C2H6中含共价键的数目为6 NA
B . 5 g KHCO3与CaCO3混合固体中阴离子数目为0.05 NA
C . 常温下,1 L 0.1 mol·L–1 CH3COONa溶液中CH3COO-离子数目为0.1 NA
D . 在Na2O2与H2O的反应中,当转移0.2 NA个电子时生成的O2体积为2.24 L
向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知:b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法不正确的是( )
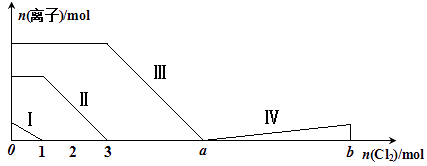
A . 线段Ⅱ表示Fe2+的变化情况
B . 线段Ⅳ发生反应的离子方程式为:I2+5Cl2+12OH-=2IO3-+10Cl-+6H2O
C . 根据图象可计算a=6
D . 原溶液中c(Fe2+)∶c(I-)∶c(Br-)=2∶1∶3
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
A . 将Na2CO3固体加入新制的氯水中,有无色气泡(H+)
B . 向淀粉KI溶液中滴加新制氯水,溶液变蓝(Cl2)
C . 将AgNO3溶液滴加到新制氯水中,有白色沉淀产生(Cl-)
D . 新制氯水使红色布条褪色(HCl)
丰富多彩的颜色变化增添了化学实验的魅力,下列有关反应颜色变化的叙述中,正确的是( )
①新制氯水久置后→浅黄绿色消失
②淀粉溶液遇单质碘→蓝色
③蔗糖中加入浓硫酸搅拌→白色
④SO2通入品红溶液中→红色褪去
⑤氨气通入酚酞溶液中→红色
⑥用稀盐酸酸化Fe(NO3)2→变黄
⑦浓硝酸涂在蓝色石蕊试纸→变红
⑧Fe(OH)3胶体通电一段时间→正极附近颜色加深
A . ①②③④⑥
B . ②③④⑤⑦
C . ①②④⑤⑥
D . ①③④⑦⑧
下列有关化学反应过程或实验现象的叙述中正确的是( )
A . 氯气的水溶液可以导电,说明氯气是电解质
B . 漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的
C . 氯气可以使鲜花褪色,说明 Cl2 有漂白性
D . 氯气可以使湿润的有色布条褪色,但实际起漂白作用的物质是次氯酸而不是氯气
置换反应的通式可表示为:单质甲+化合物A→单质乙+化合物B,请回答下列问题:
-
(1) 若甲为黄绿色气体,单质乙能使淀粉溶液变蓝色,则该反应的离子方程为。
-
(2) 若过量的单质甲 与化合物A发生反应的化学方程式为:
2Al+Fe2O3
 Al2O3+2Fe。除去反应后混合物中剩余的铝粉与生成的Al2O3所用的试剂是。
Al2O3+2Fe。除去反应后混合物中剩余的铝粉与生成的Al2O3所用的试剂是。 -
(3) 若甲为金属,其焰火为黄色,化合物B为一种常见的强碱,则该反应的化学方程式为 。
-
(4) 若单质乙是黑色非金属固体单质,化合物B是优质的耐高温材料,则该反应的化学方程式为 。
-
(5) 若化合物A可作光导纤维材料,乙为非金属半导体材料,则该反应的化学方程式为 。
在标准状况下 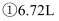

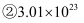 个HCl分子
个HCl分子 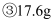

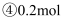
 ,下列对这四种气体的关系从大到小表达正确的是( )
,下列对这四种气体的关系从大到小表达正确的是( )
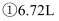

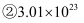 个HCl分子
个HCl分子 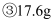

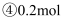
 ,下列对这四种气体的关系从大到小表达正确的是( )
,下列对这四种气体的关系从大到小表达正确的是( ) 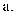 体积
体积 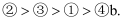 密度
密度 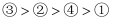
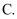 电子总数
电子总数 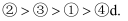 原子总数
原子总数 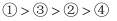
A . abcd
B . bcd
C . acd
D . abc
用 NA 表示阿伏加德罗常数的数值,下列说法正确的是( )
A . 1 mol Cl2 与足量的铁反应转移的电子数是 2NA
B . 常温常压下 22.4 L HCl气体含有的分子数是NA
C . 0.1 mol • L-1 CuCl2 溶液中 Cl-数目是 0.2 NA
D . 32 gO2 中含有的原子数是NA
不能证明S的非金属性比Cl弱的是( )
A . H2S的稳定性不如HCl
B . 氯气和铁反应生成FeCl3 , 硫和铁反应生成FeS
C . 氯气通入氢硫酸溶液中,有浅黄色浑浊
D . 盐酸的酸性比氢硫酸强
按要求填空
-
(1) 写出下列物质的化学式:漂白粉的有效成分;小苏打。
-
(2) 写出下列微粒的结构示意图:N;S2-。
-
(3) 写出下列物质的电离方程式或者化学方程式:
NH3·H2O的电离方程式;
镁条在二氧化碳中反应的化学方程式。
-
(4) 写出分离或提纯下列各组混合物时所需方法的名称:
①分离四氯化碳和水;
②提取溴水中的溴单质。
已知:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是( )
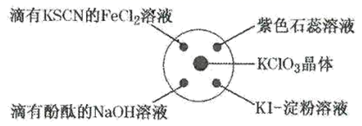
| 选项 | 实验现象 | 结论 |
| A | 滴有KSCN的FeCl2溶液变红 | Cl2具有还原性 |
| B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
| C | 紫色石蕊溶液先变红后褪色 | Cl2具有漂白性 |
| D | KI-淀粉溶液变成蓝色 | Cl2具有氧化性 |
A . A
B . B
C . C
D . D
下列解释事实的方程式正确的是( )
A . CO2通入过量的NaOH溶液中:CO2+OH-=  B . SO2的催化氧化反应:2SO2+O2
B . SO2的催化氧化反应:2SO2+O2 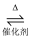 2SO3
C . 过氧化钠做呼吸面具的供氧剂:Na2O2+CO2=Na2CO3+O2
D . 氯气用于自来水消毒:Cl2+H2O⇌2H++Cl-+ClO-
2SO3
C . 过氧化钠做呼吸面具的供氧剂:Na2O2+CO2=Na2CO3+O2
D . 氯气用于自来水消毒:Cl2+H2O⇌2H++Cl-+ClO-
 B . SO2的催化氧化反应:2SO2+O2
B . SO2的催化氧化反应:2SO2+O2 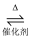 2SO3
C . 过氧化钠做呼吸面具的供氧剂:Na2O2+CO2=Na2CO3+O2
D . 氯气用于自来水消毒:Cl2+H2O⇌2H++Cl-+ClO-
2SO3
C . 过氧化钠做呼吸面具的供氧剂:Na2O2+CO2=Na2CO3+O2
D . 氯气用于自来水消毒:Cl2+H2O⇌2H++Cl-+ClO-
“84”消毒液是防疫期间常用的消毒剂,下列有关“84”消毒液的叙述不正确的是( )
A . “84”消毒液的主要成分是次氯酸钠
B . 使用时向“84”消毒液中加入少量醋酸消毒能力更强
C . “84”消毒液可适用于皮毛制品及钢铁制品的消毒
D . “84”消毒液、医用酒精均可用于新冠病毒消毒,其消毒原理不同
下列检验Cl-的方法正确的是( )
A . 向某溶液中滴加AgNO3溶液,若产生白色沉淀说明该溶液中有Cl-
B . 向某溶液中先滴加盐酸,再滴加AgNO3溶液,若产生白色沉淀,说明溶液中有Cl
C . 向某溶液中先滴加AgNO3溶液,产生白色沉淀,再滴加盐酸,沉淀不消失,说明溶液中有Cl-
D . 向某溶液中滴加用HNO3酸化的AgNO3溶液,若产生白色沉淀,说明溶液中有Cl
下列说法正确的是( )
A . 气体摩尔体积就是22.4L
B . 任何状况下,1mol任何气体的体积一定是22.4L
C . 标准状况下22.4L水含有6.02×1023个分子
D . 1molH2和O2的混合气体在标准状况下的体积约22.4L
最近更新
- 下面是表示某家系中白化病发病情况的图解,问:(1)该病属于____(显性或隐性)遗传病: (2)I1和I2的基因型分别是
- 读下面两幅示意图,回答问题。O点位于甲点的( ) A.西北方 B.西南方
- 两根相距为L的足够长的金属直角导轨如图2所示放置,它们各有一边在同一水平面内,另一边垂直于水平面.质量均为m的金属细杆a
- 某无色溶液中大量存在的离子如图所示,其中X可能是() A. CO32﹣ B. Fe3+ C. OH﹣ D. Na+
- 下列典故中,从物质变化的角度分析,主要体现化学变化的是( ) A.司马光砸缸 B.凿壁借光 C.火
- 能将水、氯氧化钡溶液、稀盐酸区分开的一种试剂是A.无色酚酞试液 B.氯化钡溶液 C.紫色石蕊试液
- 希腊文明勃兴的因素中最重要的客观条件是 A.重叠的山峦与海洋B.古罗马历史 C.中国文化影响D.迈锡尼文明
- John gets up early from Monday to Saturday,because he must g
- Read the following text and choose the most suitable heading
- 下面不属于六大板块的是 A.美洲板块 B.非洲板块 C.印度洋
- 已知是锐角,那么下列各值中,sin+cos能够取得的值是( ) A. B. C.
- 有100张奖券,其中有4张可以中奖,从中任意抽出1张,则获奖的概率为( ) A、 B、
- 选出下列各组语句中句意明确、没有语病的一句( ) A、在原始文化遗址水洞沟,人们发现了略加磨制的鸵鸟蛋穿孔饰件和骨
- 我们每天应喝适量的开水,这有利于 ( )A、对葡萄糖的吸收 B、对无机盐的吸收C、废物及时随尿排
- 2014年,自埃博拉病毒肆虐非洲以来,中国已先后派出多批次医护人员为其提供帮助,并先后向相关国家及联合国抗击疫情行动提供
- 下列是几个放射性同位素示踪实验,对其结果的叙述错误的是( ) A.提供15N标记的氨基酸给细胞,粗面内质网上的核糖体和
- 2010年正月初八上班头一天,为了狠杀“年起”,督促公务员回到正常的工作状态,扬州一民间团体市民观察团派出91名团员,带
- 下图是地质构造示意图,读图回答下题。下列山地形成与该地质构造成因相一致的是 A.喜马拉雅山脉 B.泰山 C.富士
- 在一个宇宙天然“透镜”的扭曲、放大下,天文学家观测到90亿年前一次超新星爆炸形成的被称为“爱因斯坦十字”的四重像。这种爱
- 下图表示细胞分裂和分化的简要过程。请结合图示分析有关问题:(1)过程①、②发生的不同变异类型是_____________



