第1节 碳的多样性 知识点题库
铅及其化合物可用于蓄电池,耐酸设备及X射线防护等.回答下列问题:
-
(1) 铅是碳的同族元素,比碳多4个电子层,铅在周期表的位置为 周期,第 族:非金属氧化物的水化物酸性Pb比C的 (填“强”或“弱”).
-
(2) PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为
-
(3) PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为 PbO2也可以通过石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取.阳极发生的电极反应式 , 阴极观察到的现象是:若电解液中不加入Cu(NO3)2 , 阴极发生的电极反应式 ,这样做的主要缺点是
-
(4)
PbO2在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a点为样品失重4.0%(
 ×100%)的残留固体,若a点固体表示为PbO2或mPbO2•nPbO,列式计算x值和m:n值
×100%)的残留固体,若a点固体表示为PbO2或mPbO2•nPbO,列式计算x值和m:n值 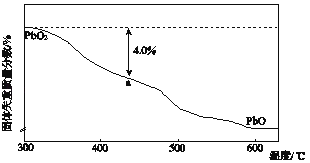
有关NaHCO3与Na2CO3的性质,下列叙述中错误的是( )
A . Na2CO3和NaHCO3粉末与同浓度盐酸反应,Na2CO3碱性强,反应放出气体速度快
B . 等物质的量的两种盐与同浓度的盐酸反应,Na2CO3消耗盐酸的体积是NaHCO3的两倍
C . 向Na2CO3饱和溶液中通入过量CO2 , 有NaHCO3结晶析出
D . Na2CO3和NaHCO3溶液分别和BaCl2溶液反应,现象不同
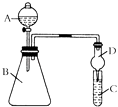
某同学为验证元素周期表中元素性质的递变规律,利用如图装置可验证同主族非金属性的变化规律.设计了如下系列实验.
-
(1) 向Na2S溶液中通入氯气出现淡黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为.
-
(2) 仪器A的名称为,
-
(3) 若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4 , (KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到混合溶液的现象,即可证明.从环境保护的观点考虑,此装置缺少尾气处理装置,可用溶液吸收尾气.
-
(4) 若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3 , C中加Na2SiO3溶液观察到C中溶液的现象,即可证明.但有的同学认为盐酸具有挥发性,应用溶液除去.
下列物质与其用途完全符合的是( )
①Na2O2﹣供氧剂 ②晶体Si﹣太阳能电池 ③AgI﹣人工降雨 ④NaCl﹣制纯碱 ⑤Al2O3﹣焊接钢轨 ⑥NaClO﹣消毒剂⑦Fe2O3﹣红色油漆或涂料 ⑧SO2﹣食品漂白剂 ⑨NH3﹣制冷剂.
A . ①④⑤⑧⑨
B . ①②③⑥⑦⑨
C . ①②③④⑥⑦⑨
D . ①②③④⑤⑥⑦⑧⑨
今有:①纯净的碳酸钠ag;②碳酸钠与碳酸氢钠的混合物ag.两者相比,下列各种情况的描述正确的是( )
A . 分别和盐酸完全反应时,混合物的耗酸量多
B . 分别和盐酸完全反应时,纯净的碳酸钠放出的CO2多
C . 分别溶于水,再加入足量澄清石灰水,混合物得到的沉淀质量大
D . 分别配成等体积的溶液,混合物溶液的Na+的物质的量浓度大
下列关于Na2O2的说法正确的是( )
A . Na2O2与SO2反应生成Na2SO3和O2
B . Na2O2投入到酚酞溶液中,溶液变红
C . Na2O2与水反应,Na2O2既是氧化剂,又是还原剂
D . Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物
下列物质中互为同分异构体的是,互为同素异形体的是,互为同位素的有,互为同系物的是,属于同一种物质的是.(填序号)
①液氯 ② 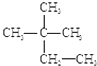 ③O2④18O ⑤
③O2④18O ⑤ 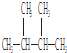
⑥O3⑦16O ⑧氯气 ⑨ ![]() ⑩
⑩ ![]()
下列关于钠的氧化物的叙述正确的是( )
A . Na2O2是白色固体,和冷水作用得到O2和NaOH
B . Na2O2与水的反应中,氧化剂是Na2O2 , 还原剂是水
C . Na2O不稳定,能继续被O2氧化生成Na2O2
D . 都能与酸反应,生成含氧酸盐,都是碱性氧化物
现有一定量含有Na2O杂质的Na2O2试样,用如图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)
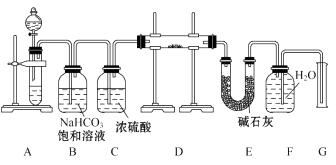
回答下列问题:
-
(1) 装置A中液体试剂选用
-
(2) 装置B的作用是,装置C的作用是,装置E中碱石灰的作用是。
-
(3) 装置D中发生反应的化学方程式是。
-
(4) 若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为。
下列各组物质混合后,不能生成NaOH的是( )
A . Na和H2O
B . Na2O2和H2O
C . Ca(OH)2溶液和Na2CO3溶液
D . Ca(OH)2溶液和NaCl溶液
以下物质间的每步转化通过一步反应能实现的是( )
A . Al→Al2O3→Al(OH)3→NaAlO2
B . Si→SiO2→H2SiO3→Na2SiO3
C . S→SO3→H2SO4→MgSO4
D . Na→Na2O2→Na2CO3→NaOH
图中,A是单质,B的焰色反应呈黄色。
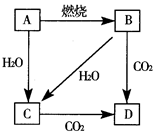
-
(1) 判断A,B,C,D的化学式:
A B C D
-
(2) 下列转化的化学方程式为:
①A→B
②B→D
③A→C
下列关于钠的描述中错误的是( )
①自然界中的钠以单质和化合物的形式存在
②实验室剩余的钠需要放同原瓶
③钠的化学性质比较活泼,少量的钠可以保存在煤油中
④当钠与硫酸铜溶液反应时,有大量红色固体铜产生
⑤金属钠与O2反应,条件不同,产物不相同
⑥燃烧时放出白色火花,燃烧后生成浅黄色固体物质
⑦钠-钾合金通常状况下呈液态,可作原子反应堆的导热剂
A . ①②④⑤⑥⑦
B . ①④⑥
C . ④⑤⑥
D . ①⑥⑦
化学与人类生产、生活、社会可持续发展密切相关,下列说法错误的是( )
A . 燃煤“气化”、“脱硫”、“钙基固硫”等措施有利于减少  排放和酸雨形成
B . 用纳米技术催化
排放和酸雨形成
B . 用纳米技术催化  合成可降解塑料聚碳酸酯,可实现“碳”的循环利用
C . 中国正积极推动可再生能源国际合作,氢能属于一次能源
D . 2021年3月20日三星堆5号祭祀坑出土的黄金面具材料属于合金
合成可降解塑料聚碳酸酯,可实现“碳”的循环利用
C . 中国正积极推动可再生能源国际合作,氢能属于一次能源
D . 2021年3月20日三星堆5号祭祀坑出土的黄金面具材料属于合金
 排放和酸雨形成
B . 用纳米技术催化
排放和酸雨形成
B . 用纳米技术催化  合成可降解塑料聚碳酸酯,可实现“碳”的循环利用
C . 中国正积极推动可再生能源国际合作,氢能属于一次能源
D . 2021年3月20日三星堆5号祭祀坑出土的黄金面具材料属于合金
合成可降解塑料聚碳酸酯,可实现“碳”的循环利用
C . 中国正积极推动可再生能源国际合作,氢能属于一次能源
D . 2021年3月20日三星堆5号祭祀坑出土的黄金面具材料属于合金
NaCl是一种化工原料,可以生产一系列物质(见图)。
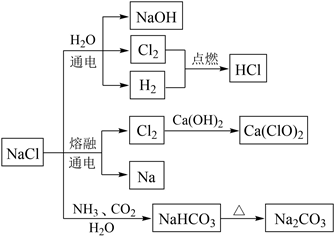
-
(1) 25℃,NaHCO3在水中的溶解度比Na2CO3的(填“大”、“小”或“不能确定”,下同),碳酸钠溶液的碱性比碳酸氢钠的碱性。
-
(2) 碳酸氢钠受热分解的化学方程式是。
-
(3) 用氯气生产氯化氢的化学方程式是。
-
(4) 氯气与氢氧化钙发生反应的化学方程式是。
化学与生活密切相关,下列物质与其用途不符合是( )
A . 过氧化钠——呼吸面具氧气来源
B . 纯碱——治疗胃酸过多
C . 次氯酸钠——消毒剂
D . 三氧化二铁——制作红色颜料
下列关于Na2CO3和NaHCO3的说法,错误的是 ( )
A . 相同条件下碱性:Na2CO3>NaHCO3
B . 相同温度下溶解度:Na2CO3>NaHCO3
C . 热稳定性:Na2CO3>NaHCO3
D . 和盐酸反应放出等量CO2 , 消耗盐酸的量:Na2CO3<NaHCO3
人类活动已经离不开各种化学材料,下列有关材料的说法不正确的是( )
A . 合金中由于原子层之间的相对滑动困难,因此纯铁的硬度比生铁小
B . 富勒烯、碳纳米管、石墨烯等碳材料,它们的物理化学性质均有着很大的差异
C . 棉花、麻与羊毛、蚕丝都是天然高分子也是天然纤维,但燃烧时产生的气味不同
D . 依据绿色化学核心思想,生产各种材料时最好选择无毒无害原料
下列关于Na2CO3、NaHCO3的叙述正确的是( )
①在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解
②分别向Na2CO3溶液和NaHCO3溶液中滴加少量盐酸,产生CO2气体较快的为NaHCO3溶液
③除去NaHCO3固体中的Na2CO3:将固体加热至恒重
④CaCl2溶液、澄清石灰水均能鉴别Na2CO3、NaHCO3溶液
⑤溶解度:Na2CO3<NaHCO3⑥物质的量相同时,消耗盐酸的量:Na2CO3>NaHCO3
A . ②⑥
B . ①③
C . ④⑤
D . ⑥
下列有关说法正确的是( )
A .  表示质子数为6、中子数为14的核素
B .
表示质子数为6、中子数为14的核素
B . 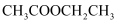 与
与 互为同分异构体
C . 葡萄糖和蔗糖互为同系物
D . 金刚石、石墨、
互为同分异构体
C . 葡萄糖和蔗糖互为同系物
D . 金刚石、石墨、 互为同素异形体
互为同素异形体
 表示质子数为6、中子数为14的核素
B .
表示质子数为6、中子数为14的核素
B . 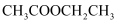 与
与 互为同分异构体
C . 葡萄糖和蔗糖互为同系物
D . 金刚石、石墨、
互为同分异构体
C . 葡萄糖和蔗糖互为同系物
D . 金刚石、石墨、 互为同素异形体
互为同素异形体
最近更新
- 类推的思想方式在化学学习与研究中经常被采用,但类推出的结论是否正确最终要经过实验的验证。以下类推的结论中正确的是() A
- 下图是19世纪以来中国出现的几个重要人物及观点,他们() A.反映了中国人坚持外交独立的原则 B.得到了资本主义
- 已知-9,a1,a2,a3,-1成等比数列,-9,b1,b2,-1成等差数列,则a2(b1-b2)= A.-
- 2012年底,我省温州市率先采用“网上直播”的方式,要求各级政府负责人宣读其的工作报告,以充分吸收群众的意见。这使公民在
- 下列图形不能围成正方体的是( ) A. B. C. D.
- 将某选手的9个得分去掉1个最高分,去掉1个最低分,7个剩余分数的平均分为91,现场做的9个分数的茎叶图后来有一个数据模糊
- 下列关于碗豆细胞有丝分裂过程中细胞器作用的叙述,不正确的是 A.在间期,核糖体上合成DNA聚合酶 B.在间期,线粒体为蛋
- 宇宙探测是一个国家综合国力的象征,2020 年中国有望实现载人登月。我国正在加强航天基地的建设,海南文昌航天基地与其它基
- 小明同学想测一石块的密度。选用天平、量筒、小石块、细线、烧杯和水,进行了如下的实验操作: A.把天平放在水平桌面上
- —What made Jack so upset? —__________three tickets for the
- 分解因式:ab3﹣ab=
- 秦朝暴政表现在 ①繁重的徭役 ②沉重的赋税 ③残酷的刑法 ④外戚专权 A.①②
- 设函数f(x)=xm+ax的导数为f′(x)=2x+1,则数列的前n项和为___________
- 已知函数 (I)当0< a < b,且f(a) = f(b)时,求的值; (II)是否存在实数a,b(a&l
- --What about the pen you bought yesterday?--It well
- 一个四棱锥和一个三棱锥恰好可以拼接成一个三棱柱.这个四棱锥的底面为正方形,且底面边长与各侧棱长相等,这个三棱锥的底面边长
- 人体甲状旁腺分泌甲状旁腺素,当人体血钙浓度下降时,甲状旁腺素分泌增加,作用于骨和肾脏使血钙浓度上升。甲状腺C细胞分泌降钙
- 时年55岁的陈玉蓉是湖北武汉一位平凡的母亲,但是最近这位母亲的故事却感动了无数国人。陈玉荣的儿子患有先天性肝功能不全,为
- 常温下,将1mL0.1mol•L-1的H2SO4溶液加入纯水中制成200mL溶液,该溶液中由水自身电离产生的c(H+)
- 本初子午线是指 A.180°经线



