专题2 从海水中获得的化学物质 知识点题库
工业上利用无机矿物资源生产部分材料的流程图如下。下列说法不正确的是( )
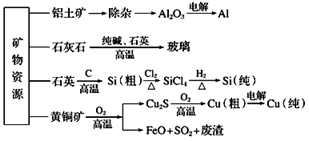
A . 在铝土矿制备较高纯度Al的过程中常用到NaOH溶液、CO2气体、冰晶石
B . 石灰石、纯碱、石英、玻璃都属于盐,都能与盐酸反应
C . 在制粗硅时,被氧化的物质与被还原的物质的物质的量之比为2∶1
D . 黄铜矿(CuFeS2)与O2反应产生的Cu2S、FeO均是还原产物
下列说法错误的是( )
A . 工业上可用铁制容器贮存浓硫酸
B . 装NaOH溶液的试剂瓶使用橡皮塞
C . 漂白粉在空气中不易变质,可敞口保存
D . 少量钠保存在煤油中
有一包白色固体,可能含有Na2CO3、KNO3、KCl、BaCl2和CuSO4 , 按下列步骤实验。
①将该固体溶于水得无色溶液。
②向溶液中加入AgNO3溶液,得到白色沉淀,再加足量的稀HNO3 , 白色沉淀部分溶解并有气泡产生,把气体通入澄清石灰水,石灰水变浑浊。根据上述现象判断:
-
(1) 一定存在的物质是;一定不存在的物质是;可能存在的物质是;
-
(2) 请写出白色沉淀部分溶解的化学方程式
下列有关钠的叙述正确的是( )
A . 2.3 g钠与97.7 g水反应后溶液中溶质的质量分数等于4%
B . 钠跟CuSO4溶液反应生成的蓝色沉淀上有时出现暗斑,这是析出了金属铜
C . 因为钠比较活泼,故将钠放入FeCl3溶液中有红褐色沉淀生成
D . 钠在空气中的缓慢氧化与其在空气中点燃的产物都一样
下列既属于放热反应又属于氧化还原反应的是( )
A . 氧化钙与水反应
B . 铁丝在氧气中燃烧
C . NaOH溶液与盐酸反应
D . Ba(OH)2·8H2O晶体与NH4Cl晶体反应
下图所示2个甲分子反应生成1个丙分子和3个乙分子,下列判断错误的是( )
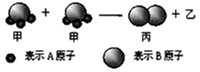
A . 1个乙分子中含有2个A原子
B . 该反应类型是分解反应
C . 相对分子质量:Mr(甲)=Mr(乙)+Mr(丙)
D . 该反应一定属于氧化还原反应
下列有关实验说法,不正确的是( )
A . 硝酸不慎溅到手上,先用大量水冲洗,再用碳酸氢钠稀溶液冲洗
B . 将两块未擦去氧化膜的铝片分别投入到 1mol•L -1CuSO4 溶液和 1mol•L -1CuCl2 溶液中,一段时间后,在CuCl2 溶液中铝片表面能观察到明显的反应现象
C . 在“火柴头中氯元素的检验”实验中,摘下几根未燃过的火柴头,将其浸于水中,稍后取少量溶液于试管中,滴加硝酸银溶液和稀硝酸后,即可判断火柴头中有氯离子的存在
D . 从 Na2S2O3 和 H2SO4 两溶液相混合开始计时,到溶液出现的浑浊将锥形瓶底部的“+”字完全遮盖时结束,通过比较记录所需时间,可判断反应速率的大小
2016年10月17日7时30分,我国“神舟十一号”载人飞船顺利升入太空。此次火箭的主要燃料是偏二甲肼(C2N2H8)和一种氮的氧化物(用R表示),当火箭发射时,这两种燃料会剧烈反应产生大量气体,并释放出大量的热,化学方程式如下(已配平):C2N2H8+2R=3N2↑+4H2O+2CO2↑
-
(1) R的化学式是;已知偏二甲肼中N元素显-2价,H元素显+1价,由此推断,C元素的化合价是。
-
(2) 该反应的还原剂是,被还原的元素是。
-
(3) 若反应生成22.4LCO2(标准状况),则反应转移电子mol。
-
(4) 火箭发射时,尾部向下喷出的气体会有明显的红棕色,该红棕色气体的化学式可能是。
-
(5) 高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。Na2FeO4能给水消毒利用的是性。用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,其净水原理与明矾相同,Fe3+净水原理是(用简要的文字叙述)。
为验证氧化性Cl2>Fe3+> SO2 , 某小组用下图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。
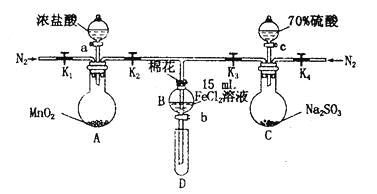
实验过程:
I.打开弹簧夹K1~K4 , 通入一段时间N2,再将T型导管插入B中,继续通入N2 , 然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的离子。
V.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
-
(1) 过程I的目的是。
-
(2) 检验B中溶液是否还有Fe2+的方法之一是:取少量B中溶液于试管中,滴加几滴含有+3价铁元素的配合物溶液,会产生蓝色沉淀.写出该反应的离子方程式。
-
(3) 若向第III步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的离子方程式。
-
(4) 若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的化学方程式为。
-
(5) 甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定不能够证明氧化性Cl2>Fe3+>SO2的是(填“甲”、“乙”或“丙”)。
过程Ⅳ,B溶液中含有的离子
过程Ⅵ,B溶液中 含有的离子
甲
有Fe3+无Fe2+
有SO42-
乙
既有Fe3+又有Fe2+
有SO42-
丙
有Fe3+无Fe2+
有Fe2+
-
(6) 将B中的FeCl2溶液换成100 mLFeBr2溶液并向其中通入1.12 LCl2(标准状况下),若溶液中有1/2的Br一被氧化成单质Br2 , 则原FeBr2溶液中FeBr2的物质的量浓度为mol/L。
已知实验室制取氯气的反应原理为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
-
(1) 该反应中氧化剂是(填化学式),被氧化的元素是(填元素符号)。
-
(2) 用单线桥法表示电子转移的方向和数目:,MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
-
(3) 有一种“地康法”制取氯气的反应原理如下所示:
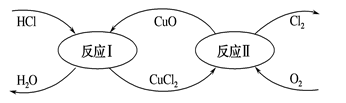
①反应Ⅰ的离子方程式为。
②反应Ⅱ属于反应。(填四种基本反应类型之一)
-
(4) 在一定条件下,Fe2O3+3CO
 2Fe+3CO2反应中,(填名称)是还原剂,(填化学式)发生还原反应.生成112gFe时,消耗CO质量是.
2Fe+3CO2反应中,(填名称)是还原剂,(填化学式)发生还原反应.生成112gFe时,消耗CO质量是.
-
(5) 维生素C又称“抗坏血酸”,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+ , 这说明维生素C具有。(填氧化性或还原性)
-
(6) 火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中氧化产物是(填化学式)
在甲、乙两烧杯溶液中,分别含有大量Cu2+、K+、H+、Cl﹣、CO  、OH﹣6种离子中的3种,已知甲烧杯的溶液呈蓝色,则乙烧杯溶液中大量存在的离子是( )
、OH﹣6种离子中的3种,已知甲烧杯的溶液呈蓝色,则乙烧杯溶液中大量存在的离子是( )
 、OH﹣6种离子中的3种,已知甲烧杯的溶液呈蓝色,则乙烧杯溶液中大量存在的离子是( )
、OH﹣6种离子中的3种,已知甲烧杯的溶液呈蓝色,则乙烧杯溶液中大量存在的离子是( )
A . K+、OH﹣、CO  B . CO
B . CO  、OH﹣、Cl﹣
C . K+、H+、Cl﹣
D . Cu2+、H+、Cl﹣
、OH﹣、Cl﹣
C . K+、H+、Cl﹣
D . Cu2+、H+、Cl﹣
 B . CO
B . CO  、OH﹣、Cl﹣
C . K+、H+、Cl﹣
D . Cu2+、H+、Cl﹣
、OH﹣、Cl﹣
C . K+、H+、Cl﹣
D . Cu2+、H+、Cl﹣
人体胃酸的主要成分是盐酸。胃酸可助消化食物,但胃酸过多会损伤胃粘膜,使人感觉不适。抗酸药(又称抑酸剂)可以减少过多的胃酸。下列物质不属于抗酸药的是( )
A . 胃得乐(主要成分:MgCO3)
B . 胃舒平[主要成分:Al(OH)3]
C . 碳酸氢钠片(主要成分:NaHCO3)
D . 阿司匹林(主要成分: 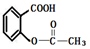 )
)
乳酸亚铁晶体  是一种良好的补铁剂。以FeSO4·7H2O和乳酸为原料可制备乳酸亚铁。
是一种良好的补铁剂。以FeSO4·7H2O和乳酸为原料可制备乳酸亚铁。
 是一种良好的补铁剂。以FeSO4·7H2O和乳酸为原料可制备乳酸亚铁。
是一种良好的补铁剂。以FeSO4·7H2O和乳酸为原料可制备乳酸亚铁。
-
(1) 碳酸亚铁的制备
将一定量的FeSO4·7H2O溶于稀硫酸,边搅拌边缓慢滴加NH4HCO3溶液至沉淀完全,过滤、洗涤、干燥,得纯净的FeCO3固体。NH4HCO3与FeSO4反应的离子方程式为。
-
(2) 乳酸亚铁晶体的制备
向纯净的FeCO3固体中加入足量乳酸溶液和少量铁粉,在75℃下搅拌使之充分反应,低温蒸发,冷却结晶,过滤,洗涤,干燥。制备乳酸亚铁晶体的过程中加入少量铁粉的目的是。
-
(3) 乳酸亚铁晶体纯度的测定:准确称取样品6.000 g,配制成250.00 mL溶液,取25.00 mL溶液于250 mL锥形瓶中,用0.1000 mol/LCe(SO4)2溶液滴定至终点(滴定过程中Ce4+与Fe2+反应生成Ce3+和Fe3+),消耗Ce(SO4)2溶液20.00 mL。则样品中乳酸亚铁晶体的纯度为(以质量分数表示;写出计算过程;乳酸亚铁晶体的相对分子质量为288)。
下列各组中的两种物质相互作用时,反应条件(温度、反应物用量比)改变,不会引起产物的种类改变的是( )
A . 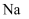 和
和  B .
B .  溶液和
溶液和  溶液
C .
溶液
C .  和
和  D .
D .  溶液和
溶液和 
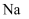 和
和  B .
B .  溶液和
溶液和  溶液
C .
溶液
C .  和
和  D .
D .  溶液和
溶液和 
下列化学反应的叙述正确的是( )
A . 铁粉与Al2O3可发生铝热反应
B . AlCl3与过量氨水生成偏铝酸铵
C . 常温下Al在稀硝酸中可发生钝化
D . 电解熔融Al2O3可制金属铝
下列属于电解质的物质是( )
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤FeSO4·7H2O ⑥稀硫酸
A . ①⑤⑥
B . ①⑤
C . ②⑤⑥
D . ③④⑤
下列各组离子中,能在水溶液中大量共存的是( )
A . Na+、Ag+、Cl-、 B . Na+、Mg2+、Cl-、
B . Na+、Mg2+、Cl-、 C . H+、K+、
C . H+、K+、 、OH-
D . Fe3+、H+、
、OH-
D . Fe3+、H+、 、I-
、I-
 B . Na+、Mg2+、Cl-、
B . Na+、Mg2+、Cl-、 C . H+、K+、
C . H+、K+、 、OH-
D . Fe3+、H+、
、OH-
D . Fe3+、H+、 、I-
、I-
下列推断合理的是( )
A . O的非金属性比S大,可推断  比
比  稳定
B . 电子云重叠程度
稳定
B . 电子云重叠程度 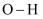 比
比 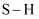 的大,可推断
的大,可推断 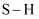 比
比 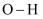 稳定
C .
稳定
C .  的相对分子质量比
的相对分子质量比  小,可推断
小,可推断  的沸点比
的沸点比  的低
D .
的低
D .  具有氧化性,可推断过硫化氢(
具有氧化性,可推断过硫化氢(  )也具有氧化性
)也具有氧化性
 比
比  稳定
B . 电子云重叠程度
稳定
B . 电子云重叠程度 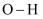 比
比 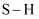 的大,可推断
的大,可推断 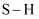 比
比 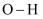 稳定
C .
稳定
C .  的相对分子质量比
的相对分子质量比  小,可推断
小,可推断  的沸点比
的沸点比  的低
D .
的低
D .  具有氧化性,可推断过硫化氢(
具有氧化性,可推断过硫化氢(  )也具有氧化性
)也具有氧化性
某100mL溶液可能含有Na+、NH 、Fe3+、CO
、Fe3+、CO 、SO
、SO 、Cl-中的若干种,取该溶液进行连续实验,实验过程如图(所加试剂均过量,气体全部逸出)。下列说法错误的是( )
、Cl-中的若干种,取该溶液进行连续实验,实验过程如图(所加试剂均过量,气体全部逸出)。下列说法错误的是( )
 、Fe3+、CO
、Fe3+、CO 、SO
、SO 、Cl-中的若干种,取该溶液进行连续实验,实验过程如图(所加试剂均过量,气体全部逸出)。下列说法错误的是( )
、Cl-中的若干种,取该溶液进行连续实验,实验过程如图(所加试剂均过量,气体全部逸出)。下列说法错误的是( )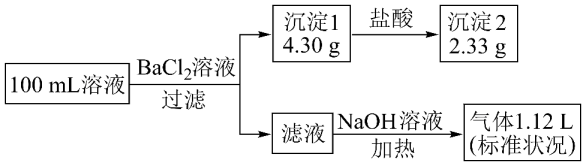
A . 原溶液一定存在CO 和SO
和SO , 一定不存在Fe3+
B . 原溶液一定存在Cl- , 可能存在Na+
C . 原溶液中c(Cl-)≥0.1mol·L-1
D . 若原溶液中不存在Na+ , 则c(Cl-)<0.1mol·L-1
, 一定不存在Fe3+
B . 原溶液一定存在Cl- , 可能存在Na+
C . 原溶液中c(Cl-)≥0.1mol·L-1
D . 若原溶液中不存在Na+ , 则c(Cl-)<0.1mol·L-1
 和SO
和SO , 一定不存在Fe3+
B . 原溶液一定存在Cl- , 可能存在Na+
C . 原溶液中c(Cl-)≥0.1mol·L-1
D . 若原溶液中不存在Na+ , 则c(Cl-)<0.1mol·L-1
, 一定不存在Fe3+
B . 原溶液一定存在Cl- , 可能存在Na+
C . 原溶液中c(Cl-)≥0.1mol·L-1
D . 若原溶液中不存在Na+ , 则c(Cl-)<0.1mol·L-1
锰铁氧体软磁材料(Fe2O3-MnO)可广泛应用在信息通讯等领域。用软锰矿(主要成分 , 含
, 含 、FeO、
、FeO、 、
、 杂质)为主要原料制备锰铁氧体软磁材料的工艺流程如下。
杂质)为主要原料制备锰铁氧体软磁材料的工艺流程如下。
 , 含
, 含 、FeO、
、FeO、 、
、 杂质)为主要原料制备锰铁氧体软磁材料的工艺流程如下。
杂质)为主要原料制备锰铁氧体软磁材料的工艺流程如下。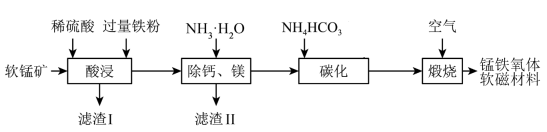
回答下列问题:
-
(1) 滤渣I的主要成分是。
-
(2) “酸浸”过程中加入过量铁粉的主要目的是将
 还原为
还原为 、。
、。
-
(3) “碳化”中生成碳酸锰沉淀的离子方程式为。
-
(4) “碳化”时,金属阳离子
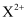 的沉淀率与温度关系如图所示。为了使
的沉淀率与温度关系如图所示。为了使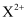 沉淀完全,最适宜的温度是。“碳化”过程需加入过量的
沉淀完全,最适宜的温度是。“碳化”过程需加入过量的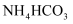 , 除了使
, 除了使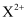 沉淀完全外,另一原因是。
沉淀完全外,另一原因是。
-
(5) “煅烧”时,碳酸亚铁发生反应的化学方程式为。
最近更新
- 物质的用途主要利用其化学性质的是() A.石墨用作电极材料 B.干冰用于人工降雨 C.一氧化碳用作燃料 D.金刚石用于切
- 最近,你校同学正在参加某英文报组织的一场讨论。讨论的主题是:公园要不要收门票?请你根据下表所提供的信息,给报社写一封信,
- 一只脚踩在钉子上,马上引起腿的收缩以避开损伤性刺激的继续作用,而另一条腿迅速伸直以支持身体,使身体不会跌倒。右图表示这一
- 计算: .
- 下列字形和加点字注音全部正确的一项是( ) A.吝啬(sè) 感概 煞有介事(shà)
- 一梯子斜靠在某建筑物上,当梯子的底端离建筑物9m时,梯子可以达到建筑物的高度是12m,你能算出梯子的长度吗?
- 在超市调查发现,面对光鲜亮丽的有机蔬菜,市民充满了矛盾之情,没有任何污染的蔬菜,谁都想购买,然而由于其价格较高,不少市民
- 如图所示,水平地面上叠放着A、B两物体,B物体受力F作用,A、B一起相对地面向右做匀减速直线运动,则B物体的受力个数为(
- 如图,根据下面的运算程序,若输入时,输出的结果 .
- 2001年11月,中国被正式批准加入世界贸易组织。这有利于中国①扩大就业②减少国 际竞争③更好地利用外资④参与国际经贸规
- 16.补写出下列名篇名句中的空缺部分。(1),问苍茫大地,谁主沉浮?(《沁园春·长沙》) (2)蒹葭萋萋,
- 下列有关碱金属的说法中,不正确的是( ) A.IA族元素都是碱金属元素 B.K的还原性强于Na C.Na和Na
- 下列各组词语中,没有错别字的一组是 ( )A. 嗔笑 僭越 衣衫褴褛 优柔寡断 B.膨胀
- 试管婴儿是指() A.在试管内把受精卵培育成足月的婴儿 B.成熟的卵和精子在试管内完成受精过程 C.把精子移植到母
- |-3|的相反数是 ( ) A.3 B.-3 C. D.-
- 在证明DNA是遗传物质的实验中,赫尔希和蔡斯分别用32P和35S标记噬菌体的DNA和蛋白质,在下图中标记元素所在部位依次
- 如图所示是做光电效应实验的装置简图。在抽成真空的玻璃管内,K为阴极(用金属铯制成,发生光电效应的逸出功为1.9eV),A
- If we can _____ our present difficulties, then everything sh
- 下图是三种稀酸对Fe–Cr合金随Cr含量变化的腐蚀性实验结果,下列有关说法正确的是A.稀硝酸对Fe–Cr合金的腐蚀性比稀
- 如图,⊙O的半径OA=2,B是⊙O上的动点(不与点A重合),过点B作⊙O的切线BC,BC=OA,连结OC,AC.当△OA



