实验3-5 比色法测定抗贫血药物中铁的含量 知识点题库
(2)有两份等体积的0.1mol/L的醋酸溶液,分别用蒸馏水和0.1mol/L的醋酸钠溶液稀释100倍,用0.1mol/L的醋酸钠溶液稀释后的溶液pH较 (填:“大”或“小”)原因:
A | B | C | D | |
纸蝴蝶上的喷洒液 | 石蕊 | 酚酞 | 酚酞 | 石蕊 |
小烧坏中的溶液 | 浓氨水 | 浓氨水 | 氢氧化钠溶液 | 浓硫酸 |
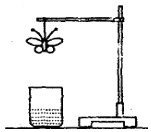
现称取研细的黄铜矿样品1.84g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的1/10置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20mL。请回答下列问题:
-
(1) 将样品研细后再反应,其目的是。
-
(2) 装置a和c的作用分别是_和(填标号,可以多选)。
a.除去SO2气体 b.除去空气中的水蒸气
c.有利于气体混合
d.有利于观察空气流速
e.除去反应后多余的氧气
-
(3) 滴定达终点时的现象是。
-
(4) 上述反应结束后,仍需通一段时间的空气,其目的是。
-
(5) 通过计算可知,该黄铜矿的纯度为。
乙同学在甲同学实验的基础上,设计了两种与甲不同的吸收方法,并对吸收产物进行有关处理,同样也测出了黄铜矿的纯度。
-
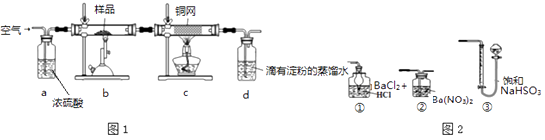
(6) 方法一:用如图2装置替代上述实验装置d,同样可以达到实验目的是(填序号)。
-
(7) 方法二:将原装置d中的试液改为Ba(OH)2 , 但测得的黄铜矿纯度却产生了+1%的误差,假设实验操作均正确,可能的原因主要有。
-
(1) 上述四种物质分别加入到紫色石蕊溶液中,溶液变红的是(填序号)。
-
(2) 写出H2SO4 的电离方程式。
-
(3) 写出过氧化钠与水反应的化学方程式。
-
(4) 碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为。
-
(5) 写出二氧化硅与氢氧化钠溶液反应的离子方程式。
-
(1) 滴定时应选用作指示剂;到达滴定终点的实验现象是。
-
(2) 下列操作会导致烧碱样品中NaOH含量测定值偏高的是____。A . 锥形瓶未用待测液润洗 B . 酸式滴定管未用标准液润洗 C . 在滴定前有气泡,滴定后气泡消失 D . 滴定前平视读数,滴定结束俯视读数 E . 滴定终点前加水清洗锥形瓶 F . 指示剂变色后立即读数
-
(3) 实验相关数据记录如下:
实验编号
V(烧碱溶液)/mL
V(HCl)/mL
初读数
末读数
1
20.00
0.60
20.62
2
20.00
0.80
20.78
3
20.00
0.20
20.90
依据表中数据,计算样品中NaOH的质量分数。
步骤1:称量4.66g草酸铁晶体进行处理后,配制成250 mL一定物质的量浓度的溶液。
步骤2:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根
恰好全部氧化成二氧化碳,同时MnO4-被还原成Mn2+。向反应后的溶液中加入一小匙锌粉,加热至溶液黄色刚好消失,过滤、洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
步骤3:用0.0200 mol·L-1KMnO4溶液滴定步骤2所得溶液至终点,消耗KMnO4溶液V1 mL,滴定中MnO4-被还原成Mn2+。
重复步骤2、步骤3的操作2次,分别滴定消耗0.0200 mol·L-1 KMnO4溶液为V2、V3 mL。
记录数据如下表:
实验编号 | KMnO4溶液的浓度(mol·L-1) | KMnO4溶液滴入的体积(mL) |
1 | 0.0200 | V1 = 20.02 |
2 | 0.0200 | V2 = 20.12 |
3 | 0.0200 | V3 = 19.98 |
请回答下列问题:
-
(1) 草酸铁溶液能做净水剂的原因(用离子方程式表示)
-
(2) 该实验步骤1和步骤3中使用的仪器除托盘天平、铁架台、滴定管夹、烧杯、玻璃棒外,一定需用下列仪器中的 (填序号)
A.酸式滴定管 B.碱式滴定管 C.量筒(10 mL) D.锥形瓶 E.胶头滴管 F.漏斗 G.250 mL容量瓶
-
(3) 加入锌粉的目的是
-
(4) 步骤3滴定时是否选择指示剂(是或否);说明理由写出步骤3中发生反应的离子方程式
-
(5) 在步骤2中,若加入的KMnO4溶液的量不够,则测得的铁含量(填“偏低”、“偏高”或“不变”);实验测得该晶体中结晶水的个数x为。
 的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是( )
的含量。先将部分变质的烧碱配制成一定浓度溶液并加入一种指示剂,用一定浓度的HCl溶液滴定至变色后,再加入另一种指示剂,继续用该HCl溶液滴定至变色,分别记录两个变色点加入HCl溶液体积进行计算。滴定过程中溶液pH的变化如图所示。下列说法错误的是( ) 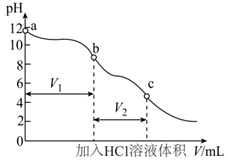
 C . 若
C . 若  ,则a点溶液中存在
,则a点溶液中存在 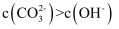 D . 原固体混合物中碳酸钠的质量分数表示为
D . 原固体混合物中碳酸钠的质量分数表示为 
-
(1) ①漂白粉有效成分的化学式是;
②写出以碳为骨架的有机物
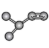 的结构简式。
的结构简式。 -
(2) 写出CH3CH=CH2使溴的CCl4溶液褪色的化学反应方程式。
-
(3) 向FeCl3溶液中滴加几滴KSCN溶液,观察到的现象是。
 和
和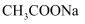 溶液等体积混合,则
溶液等体积混合,则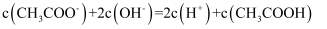 D . 用已知浓度的NaOH溶液滴定未知浓度的
D . 用已知浓度的NaOH溶液滴定未知浓度的 溶液,若选用甲基橙做指示剂,滴定过程中水的电离程度先增大后减小
溶液,若选用甲基橙做指示剂,滴定过程中水的电离程度先增大后减小
- 根据条件把流程图补充完整,求内所有奇数的和; (1) 处填 (2) 处填
- 2009年河北省组织召开了首次河北省科学技术奖励大会,对我省优秀科技成果和科技人员进行表彰奖励。据此回答下题。 河北省科
- --____________do you exercise?--Three to six times a week.
- It was considerate________them to sendflowers on my birthday
- 函数的最大值是 A B. C D
- —How many English words do you think I should know?—As many
- 常言道“春雨贵如油”,韩愈在《早春呈水部张十八员外》中写春雨和草的两句诗是:______________,_______
- 下图中a、b曲线分别代表两类商品的价格与需求量的关系。在一般情况下,可以推断出的正确结论是( )A.a商品需求弹性大
- 如图,一次函数y=kx+b的图象与反比例函数y=的图象交于A、B两点. (1)利用图中的条件,求反比例函数和一次函数的解
- 某市水果批发部门欲将A市的一批水果运往本市销售,有火车和汽车两种运输方式,运输过程中的损耗均为200元/时。其它主要参考
- 阅读下文,完成9-12题。(13分)味蕾上绽放的爱 ○黎 明1记得一位老同事,每次就餐让他点菜时,
- 下列各句中,标点符号的使用全都正确的一项是 () A.“以租养房”的方式一直被认为
- 对危险化学品要在包装标签上印有警示性标志。天然气应选用的标志是( ) A B
- 动物细胞培养是动物细胞工程的基础,如图所示,a是核移植技术,b是体外受精技术,c是胚胎分割技术,①②③依次表示其结果。据
- 下图是一个化学过程的示意图。(1)图中甲池是________装置(填“电解池”或“原电池”),其中OH-移向______
- 从2013年7月起,中国人民银行决定全面放开金融机构贷款利率管制,由金融机构根据商业原则自主确定贷款利率水平。央行的这一
- 阅读下面的文言文,完成文后各题 徐孺子祠堂记 曾 巩 汉元兴以后,政出宦者,小人挟其威福,相煽为恶,中材顾望,不知所为。
- 下列图标中,在商场、医院、车站等公共场所最常见的是() A. B. C. D.
- 古代民谚:“千生意,万买卖,不如翻地块”。这句民谚反映了中国古代农业的什么特点 A.分散性 B.自给自足
- 某化学小组的同学利用混有少量CO2的CO气体还原氧化铁,并验证反应后的气体产物。实验室现有下图所示实验装置(可重复使用)



