课题二 物质的制备 知识点题库
现代工业常以氯化钠、二氧化碳和氨气为原料制备纯碱,部分工艺流程如图:
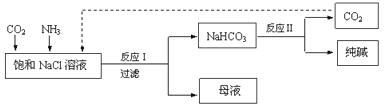
有关说法错误的是( )
一学习小组用100g某硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)制备绿矾(FeSO4•7H2O),主要流程如图:
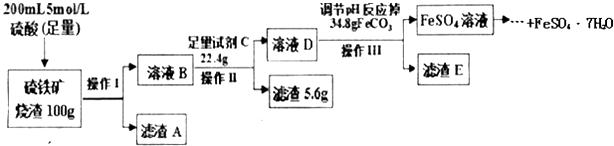
请回答下列问题:
-
(1) 硫铁矿烧渣中加入硫酸酸浸往往需要升温,目的是,操作1的名称是,滤渣A是.
-
(2) 试剂C为,加入该试剂的目的是(用离子方程式表示).
-
(3) 调节溶液D的pH目的是.
-
(4) 已知常温下Al(OH)3的Ksp=1.0×10﹣33 , 若溶液中c(Al3+)为1.0mol/L,请计算Al3+开始沉淀的pH=.
-
(5) 依据上述流程中的相关数据,求该硫铁矿烧渣中Fe2O3的质量分数为.(本实验各操作中损失的硫酸盐、硫酸及调pH后溶液呈微酸性残留的硫酸忽略不计)
选项 | 实验目的 | 主要仪器 | 试剂 |
A | 分离Br2和CCl4的混合物 | 分液漏斗、烧杯 | Br2和CCl4的混合物、蒸馏水 |
B | 制备Fe(OH)3胶体 | 烧杯、玻璃棒、酒精灯 | 1.0mol/L FeCl3溶液、蒸馏水 |
C | 实验室制取NH3 | 试管、带导管的橡皮塞 | 浓氨水、生石灰 |
D | 测定NaOH溶液浓度 | 滴定管、锥形瓶、烧杯 | NaOH溶液、0.100 0mol/L盐酸、酚酞溶液 |
选项 | 实验操作及现象 | 结论 |
A | 常温下,用pH计测得0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH,前者大 | 酸性:CH3COOH>HClO |
B | 向淀粉溶液中加入稀硫酸并加热,再加入银氨溶液,水浴加热,未见有银镜产生 | 淀粉没有水解 |
C | 向MgCl2溶液中滴加足量NaOH溶液,有白色沉淀生成;再滴加CuCl2溶液,有蓝色沉淀生成 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
D | 向Fe(NO3)2样品,溶于稀硫酸,滴加KSCN溶液,溶液变红 | Fe(NO3)2样品溶于稀硫酸前已氧化变质 |
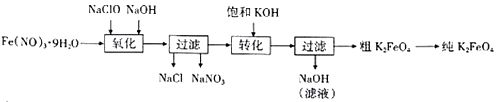
已知高铁酸钾的部分性质如下:
① 热稳定性差,溶液的pH对其稳定性的影响也很大;即在低温、碱性环境中稳定,高温、中性和酸性条件下不稳定。
② 在水中溶解度大,难溶于无水乙醇等有机溶剂。
③ 具有强氧化性,能氧化烃、80%以下的乙醇溶液等物质。
回答下列问题:
-
(1) 该生产工艺应在温度(填“较高”或“较低”)的情况下进行。
-
(2) 上述氧化过程中,发生反应的离了方程式为。
-
(3) 由流程图可见,湿法制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠中加入饱和KOH溶液,即可析出高铁酸钾
① 加入饱和KOH溶液的目的是:。
② 由以上信息可知:Ksp(K2FeO4)Ksp(Na2FeO4)(填“大于”或“小于”)。
-
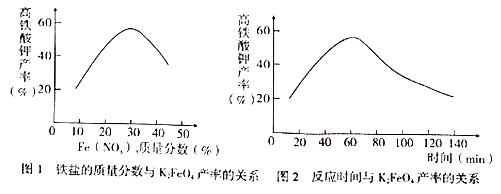
(4) 实验测得铁盐溶液的质量分数、反应时间与K2FeO4产率的实验数据分别如下图l、图2所示。为了获取更多的高铁酸钾,铁盐的质量分数应控制在附近、反应时间应控制在。
-
(5) 粗K2FeO4→纯K2FeO4包括重结晶、过滤、洗涤、干燥几个步骤。洗涤、干燥的目的是脱碱、脱水,洗涤时最好用洗涤。
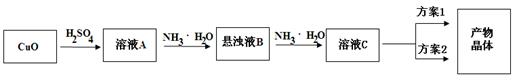
相关信息如下:
①[Cu(NH3)2]SO4·H2O在溶液中存在以下电离(解离)过程:
[Cu(NH3)4]SO4·H2O=[Cu(NH3)4]2++SO42-+H2O [Cu(NH3)4]2+  Cu2++4NH3
Cu2++4NH3
②(NH4)2SO4在水中可溶,在乙醇中难溶。
③[Cu(NH3)4]SO4·H2O在乙醇、水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如图
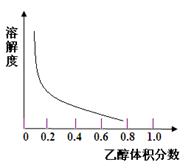
请根据以上信息回答下列问题:
-
(1) 方案1的实验步骤为:a.加热蒸发,b.冷却结晶,c.抽滤,d.洗涤,e.干燥。
①步骤1的抽滤装置如图所示,下列有关抽滤操说法作正确的是。
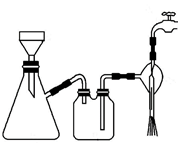
A.完毕后的先关闭水龙头,再拔下导管
B.上图装置中只有一处错误
C.抽滤后滤液可以从上口倒出,也可从支管倒出
D.滤纸应比漏斗内径小且能盖住所有小孔
②该方案存在明显缺陷,因为得到的产物晶体中往往含有杂质,产生该杂质的原因是。
-
(2) 方案2的实验步骤为:a.向溶液C中加入适量,b.抽滤,c.洗涤,d.干燥。
①请在上述空格内填写合适的试剂或操作名称。
②下列选项中,最适合作为步骤c的洗涤液是。
A.乙醇 B.蒸馏水 C.乙醇和水的混合液 D.饱和硫酸钠溶液
洗涤的具体操作是:。
③步骤d采用干燥的方法。
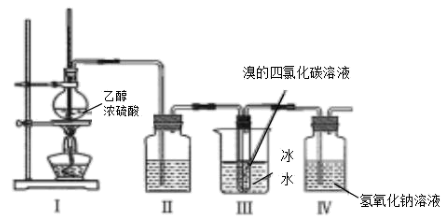
①在30mL的大试管A中按体积比2:3:2的比例配制浓硫酸、乙醇和乙酸的混合溶液。
②按如图连接好装置(装置气密性良好),用小火均匀地加热装有混合溶液的大试管5~10min。
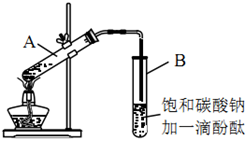
③待试管B收集到一定量产物后停止加热,撤出试管B并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。
已知下列数据:
| 物质 | 熔点(℃) | 沸点(℃) | 密度(g/cm3) |
| 乙醇 | -117.0 | 78.0 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸(98%) | ―― | 338.0 | 1.84 |
请回答下列问题:
-
(1) 配制该混合溶液时,加入这三种物质的先后顺序是;写出制取乙酸乙酯的化学方程式:。
-
(2) 该实验中,浓硫酸的作用是。
-
(3) 上述实验中饱和碳酸钠溶液的作用是___________(填字母)。A . 吸收部分乙醇 B . 中和乙酸 C . 降低乙酸乙酯的溶解度,有利于分层析出 D . 加速酯的生成,提高其产率
-
(4) 步骤②中需要小火均匀加热操作,其主要理由是。
-
(5) 步骤③中B试管内的上层物质是(填物质名称)。
-
(6) 步骤④中分离操作用到的主要仪器是;可选用的干燥剂为(填字母)。
A. 生石灰 B. NaOH固体
C. 碱石灰 D. 无水Na2SO4
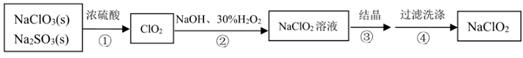
已知:ClO2浓度过高时易发生分解, NaClO2高于60℃时易分解, NaClO2饱和溶液在低于38℃时析出NaClO2·3H2O,高于38℃时析出 NaClO2。
下列说法不正确的是( )
-
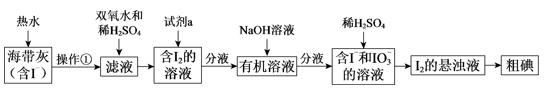
(1) 操作①的名称是。
-
(2) 向滤液中加入双氧水的作用是。
-
(3) 试剂a可以是(填序号)。
①四氯化碳 ②苯 ③酒精 ④乙酸
-
(4) I–和IO3-在酸性条件下生成I2的离子方程式是。
-
(5) 上图中,含I2的溶液经3步转化为I2的悬浊液,其目的是。
| 选项 | 实验 | 现象 | 结论 |
| A | 向浓度均为0.1mol/LNaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 常温下,测定等物质的量浓度的 Na2CO3和Na2SO3溶液的pH值 | 前者的pH值比后者的大 | 非金属性:S>C |
| C | 向某溶液中加入硝酸酸化的氯化钡溶液 | 溶液中有白色沉淀生成 | 该溶液中含有SO42- |
| D | 向FeCl3和KSCN混合溶液中,加入少量KCl固体 | 溶液颜色变浅 | FeCl3+3KSCN |
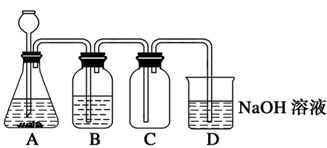
 常用于印染和电镀工业.某研究小组设计
常用于印染和电镀工业.某研究小组设计 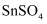 的制备路线如图:
的制备路线如图: 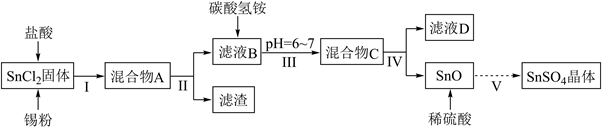 已知:
已知: 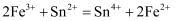 ;强酸性条件下,锡元素在水溶液中有
;强酸性条件下,锡元素在水溶液中有  、
、  两种主要存在形式,
两种主要存在形式, 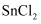 极易水解,生成对应的碱式盐。
极易水解,生成对应的碱式盐。
-
(1) 锡原子的核电荷数为50,与碳元素属于同一主族,锡元素在周期表中的位置是。
-
(2)
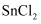 用盐酸溶解而不用水直接溶解的原因是;加入
用盐酸溶解而不用水直接溶解的原因是;加入 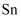 粉的作用有两个;①调节溶液
粉的作用有两个;①调节溶液  ②。
②。
-
(3) 步骤Ⅱ中用到的玻璃仪器有;
-
(4) 酸性条件下,
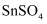 还可以用作双氧水去除剂,发生反应的离子方程式是。
还可以用作双氧水去除剂,发生反应的离子方程式是。
-
(5) 向
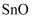 中加入稀硫酸的作用之一是控制溶液的
中加入稀硫酸的作用之一是控制溶液的  .若溶液中
.若溶液中 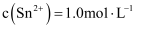 ,则室温下应控制溶液
,则室温下应控制溶液  取值范围为(已知
取值范围为(已知  )
)
-
(6) 该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):取
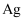 锡粉溶于盐酸中,向生成的
锡粉溶于盐酸中,向生成的 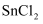 中加入过量的
中加入过量的  溶液,用
溶液,用  滴定生成的
滴定生成的  (已知酸性环境下,
(已知酸性环境下,  可被还原为
可被还原为 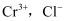 不能被
不能被  氧化),共用去
氧化),共用去  溶液
溶液 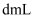 .则锡粉中锡的质量分数为.(
.则锡粉中锡的质量分数为.( 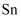 的摩尔质量为
的摩尔质量为 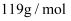 ,用含a、b、d的最简代数式表示)
,用含a、b、d的最简代数式表示)
 固体
B . 用
固体
B . 用 气体和NaOH溶液做喷泉实验
C . 直接加热
气体和NaOH溶液做喷泉实验
C . 直接加热 固体制备氨气
D . 用Mg、Al、NaOH溶液设计一个原电池装置,且Mg做电池的负极
固体制备氨气
D . 用Mg、Al、NaOH溶液设计一个原电池装置,且Mg做电池的负极
| 装置 | 实验 | 试剂a | 现象与结果 |
| | I | 10h后,液体变为浅蓝色,将铜片取出、干燥,铜表面附着蓝色固体,成分是Cu(OH)2 | |
| II | 8mL5mol/L氨水 | 立即产生大量气泡,溶液变为深蓝色,将铜片取出、干燥,铜表面附着蓝色固体,成分是Cu(OH)2 | |
| III | 8mL5mol/L氨水和1gNH4Cl固体 | 立即产生大量气泡,溶液变为深蓝色,将铜片取出、干燥,铜片依然保持光亮 |
下列说法错误的是( )
| 序号 | 操作 | 现象 | 解释或结论 |
| A | 在含0.1 mol的AgNO3溶液中依次加入NaCl溶液和KI溶液 | 溶液中先有白色沉淀生成,后来又变成黄色 | Ksp(AgCl)>Ksp(AgI) |
| B | 取FeSO4少许溶于水,加入几滴KSCN溶液 | 溶液变红色 | FeSO4全部被氧化 |
| C | 将纯净的乙烯气体通入酸性KMnO4溶液 | 溶液紫色褪去 | 乙烯具有还原性 |
| D | 在Ca(ClO)2溶液中通入SO2气体 | 有沉淀生成 | 酸性: H2SO3> HClO |
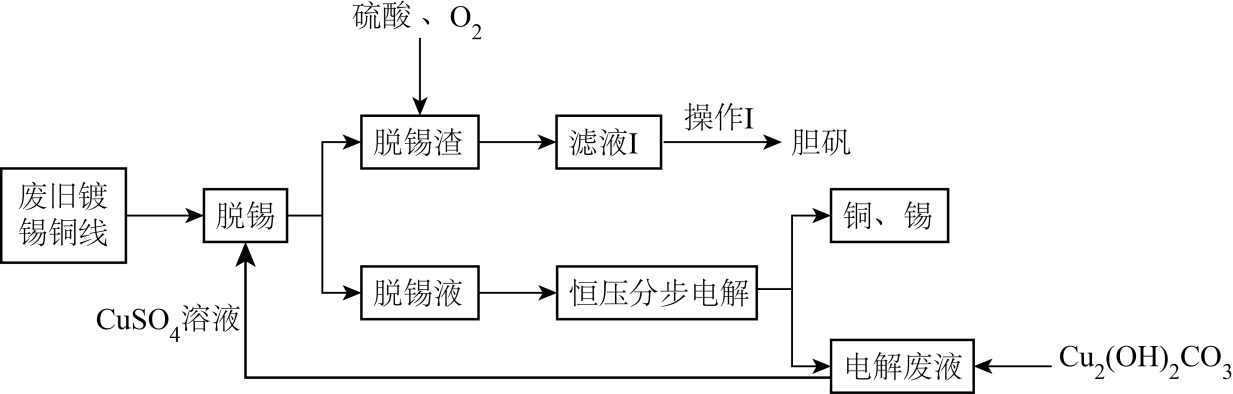
已知Sn2+容易水解。
回答下列问题:
-
(1) 加快“脱锡”速率的措施有(写出一点)。“操作I” 包含、、过滤、洗涤、干燥。
-
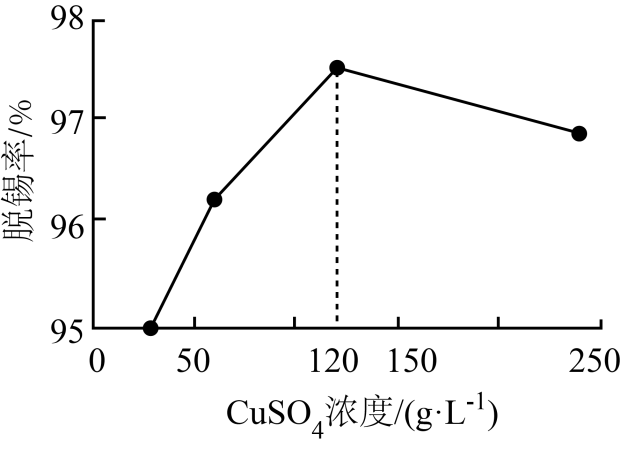
(2) “脱锡”过程中加入少量稀硫酸调控溶液pH,其目的是;硫酸铜浓度与脱锡率的关系如图所示,当浓度大于120g·L-1时,脱锡率下降的原因。
-
(3) “脱锡液”中含有的离子主要为Cu2+、Sn2+、H+、SO
 , 以石墨为电极,通过控制溶液pH、电解时电压,可以依次回收铜、锡。电解时阳极反应式为; 当阴极出现的现象时,说明电解回收锡结束。
, 以石墨为电极,通过控制溶液pH、电解时电压,可以依次回收铜、锡。电解时阳极反应式为; 当阴极出现的现象时,说明电解回收锡结束。
-
(4) “脱锡渣”溶于硫酸的离子方程式为。
-
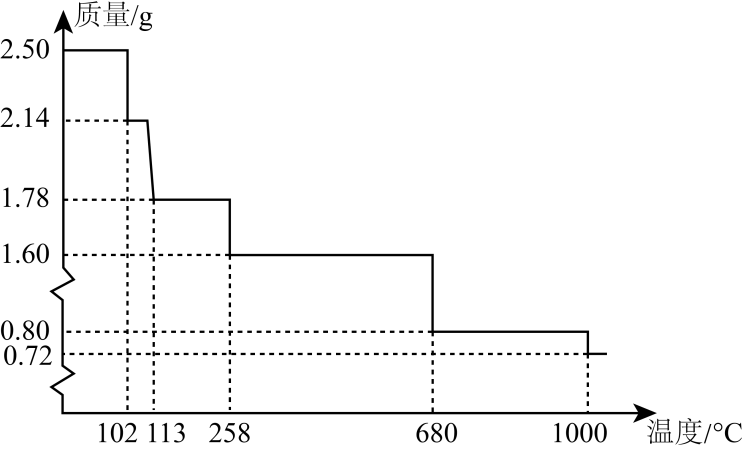
(5) 称量纯净的胆矾2.50g进行热重分析,实验测得胆矾的热重曲线如图所示。则120℃时所得固体的化学式为。
下列说法错误的是( )
- 人类先天聋哑病(d)和血友病(Xh)都是隐性遗传病,基因型DdXHXh和ddXhY的俩人婚配,他们的子女中理论上患一种遗
- “政由己出,明察善断,故当时英贤亦竟为之用”,这是《资治通鉴》对唐朝哪一位最高统治者的评价? A.唐太宗
- 设函数可导,则等于( ) A. B. C. D.
- 先取甲、乙、丙、丁四种金属粉末,分别投入相同浓度的稀盐酸中,只有甲、乙能产生气体,乙反应更剧烈;再取一小块丁投入丙的硝酸
- 计算: ;
- 修改下面的一个病句 在交通干线上设卡收费的方案必须经地方人大常委会讨论通过,并公诸于社会。
- 点(-4,3)在反比例函数图象上,则这个函数的关系式为 ▲ .
- 【2012•蚌埠一模】顾炎武决心做到:“凡文之不关乎六经之旨、当世之务者,一切不为”。由此可见他 A.强调实地调查
- 填表题秦汉文化成就表 人物 所处朝代 主要成就或贡献 造纸术 数学 地震学 医学
- 母 亲 肖复兴 ①那一年,我的生母突然去世,我不到八岁,弟弟才三岁多一点儿,我俩朝爸爸哭着闹着要妈妈。爸爸办完
- 沿着正方体的棱从一个顶点到与它相对的另一个顶点最近的路线共几条? ( ) 6条 B.5
- 如图所示,工人师傅推动一台重300N的割草机,施加力F的大小为100N,方向斜向下与水平方向成α=370角(sin37°
- 丁二酮(C4H6O2)可用作糖果增香剂。下列关于丁二酮的说法中正确的是 A.丁二酮的相对分子质量86g B.丁二酮
- 下列各组离子在指定的溶液中,―定能大量共存的是 ①能使红色石蕊试纸变蓝的溶液中:K+、Na+、CO32-、NO3-、
- (9分)如图所示,已知电源电动势E=20V,内阻r=1Ω,当接入固定电阻R=4Ω时,电路中标有“3V,4.5W”的灯泡L
- 图甲中游标卡尺(游标尺上有20个等分刻度)读数为 cm。
- 2009年3月5日至13日,十一届全国人大二次会议在北京召开。回答下题。 今年“两会”期间,在网络媒体开展的“我有问题问
- 读90°E附近海平面气压图(单位:hPA.),回答以下气压最高值出现的纬度和气压值最低处的气压带名称分别是A.50°N、
- (1)25℃时,0.1 mol·L-1的HA溶液中c(H+)/c(OH-)=1010。请回答下列问题: ①HA是____
- 为了把陷在泥坑里的汽车拉出来,司机用一条结实的绳子把汽车拴在一棵大树上,开始时相距12 m,然后在绳的中点用400 N的




