课题二 化学实验的绿色追求 知识点题库
-
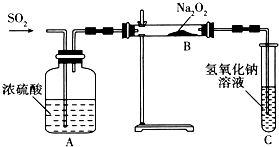
(1) 第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2 , 该反应的化学方程式是.
-
(2) 请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3 . .
-
(3) 第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成.为检验是否有Na2SO4生成,他们设计了如下方案:
将B中反应后的固体溶解于水
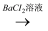 白色沉淀
白色沉淀 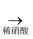 仍有部分白色沉淀不溶解,证明有Na2SO4生成
仍有部分白色沉淀不溶解,证明有Na2SO4生成上述方案是否合理?.请简要说明两点理由:
①;②.
-
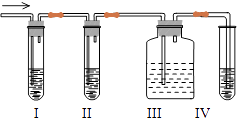
(1) Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是:Ⅰ;Ⅱ;Ⅲ;Ⅳ(将下列有关试剂的序号填入空格内).
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
-
(2) 能说明SO2气体存在的现象是.
-
(3) 使用装置Ⅱ的目的是.
-
(4) 使用装置Ⅲ的目的是.
-
(5) 确定含有乙烯的现象是.
-
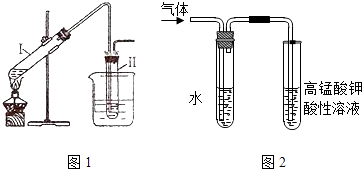
(1) 试管I中浓硫酸与溴化钠加热反应生成氢溴酸,写出氢溴酸与乙醇在加热时反应的化学方程式
-
(2) 溴乙烷的沸点较低,易挥发,为了使溴乙烷冷凝在试管Ⅱ中,减少挥发,图1中采取的措施有、
-
(3) 在进行溴乙烷与NaOH乙醇溶液共热的性质实验时,把生成的气体通过图2所示的装置.用如图2装置进行实验的目的是;图中右边试管中的现象是;水的作用是.
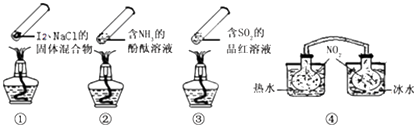
如图所示的实验,发现烧杯中酸性KMnO4溶液褪色.若将烧杯中的溶液换成含有少量KSCN的FeSO4溶液,溶液呈血红色.判断下列说法中不正确的是( )
-
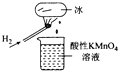
(1) 比较卤素单质的氧化性强弱,各仪器的正确连接顺序(填各接口的字母符号)
g接,接,接.
-
(2) 装置④烧瓶中反应的化学方程式为.
-
(3) 装置①中的现象是,装置③的作用是.
-
(4) 装置②中反应的离子方程式为.
-
(5) 向反应后的①中加入足量的NaOH溶液,产生的现象是,反应的方程式是.
-
(1) 往煤中添加一些石灰石,可使燃煤过程中产生的SO2转化成硫酸钙.该反应的总化学方程式是.
-
(2) 可用多种溶液做燃煤烟气中SO2的吸收液.
①分别用等物质的量浓度的Na2SO3溶液和NaOH溶液做吸收液,当生成等物质的量NaHSO3时,两种吸收液体积比V(Na2SO3):V(NaOH)=
②NaOH溶液吸收了足量的:SO2后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使NaOH溶液再生,再生过程的离子方程式是.
-
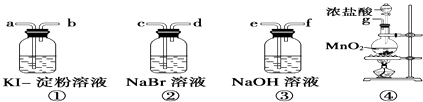
(3) 甲同学认为BaCl2溶液可以做SO2的吸收液.为此甲同学设计如下实验(夹持装置和加热装置略如图1,气密性已检验).反应开始后,A中Na2SO3固体表面有气泡产生同时有白雾生成;B中有白色沉淀.甲同学认为B中白色沉淀是SO2与BaCl2溶液反应生成的BaSO3 , 所以BaCl2溶液可做SO2吸收液.
乙同学认为B中的白色沉淀是BaSO4 , 产生BaSO4的原因是:
①A中产生的白雾是浓硫酸的酸雾,进入B中与BaCl2溶液反应生成BaSO4沉淀.
②为证明SO2与BaCl2溶液不能得到BaSO3沉淀,乙同学对甲同学的实验装置做了如下改动并实验(夹持装置和加热装置略如图2,气密性已检验):
反应开始后,A中Na2SO3固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其它现象;D中红色褪去.
③试管B中试剂是溶液;滴加浓硫酸之前的操作是
④通过甲、乙两位同学的实验,得出的结论是.
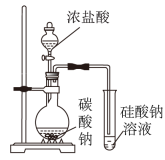
【提出问题】小松想探究分子的运动速率与相对分子质量的关系.
【假设猜想】①分子质量(相对分子质量)越大,分子运动速率越快;②分子质量(相对分子质量)越小,分子运动速率越快.
【查阅资料】已知浓氨水能挥发出氨气,浓盐酸能挥发出氯化氢气体,二者接触反应会产生白烟(即氯化铵固体).
【设计实验】如图所示,在玻璃管两端分别放入蘸有浓氨水和浓盐酸的棉花团.
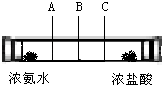
【实验现象】C处产生的白烟较多.
【解释与结论】
-
(1) 氨分子的相对分子质量(填“大于”、“等于”或“小于”)氯化氢分子的相对分子质量,由此可知,相对分子质量越(填“大”或“小”),分子的速率越(填“快”或“慢”).
-
(2) 反应的化学方程式为.
-
(3) 【拓展探究】小松在完成上述实验后,还想研究分子运动速率与温度的关系.
他将等量的品红分别滴入到等量的热水和冷水中,其实验现象如下所示.
实验过程
冷水
热水
开始
红色扩散较慢
红色扩散较快
长久放置
最终均成为红色、均匀、透明的液体
依据此实验现象,得出的结论是.
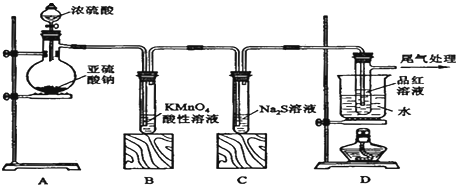
请到答F列问题:
-
(1) 装置A中盛放浓硫酸的仪器名称是,其中发生反应的化学方程式为;
-
(2) 实验过程中,装置B、C中发生的现象分别是、,这些现象分别说明SO2具有的性质是和.
-
(3) 装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象;
-
(4) 尾气可采用溶液吸收.(写化学式)
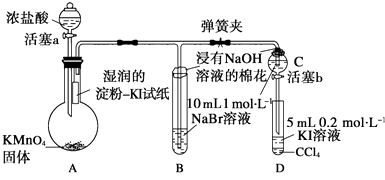
已知:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a.
Ⅳ.…
-
(1) 验证氯气的氧化性强于碘的实验现象是.
-
(2) B中溶液发生反应的离子方程式是.
-
(3) 为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是.
-
(4) 过程Ⅲ实验的目的是.
-
(5) 氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,,得电子能力逐渐减弱.
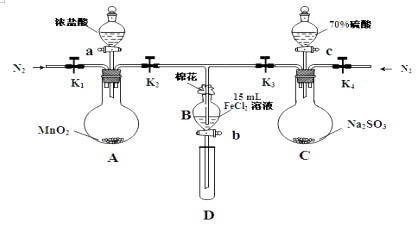
Ⅰ.打开弹簧夹K1~K4 , 通入一段时间N2 , 再将T型导管插入B中,继续通入N2 , 然后关闭K1、K3、K4 .
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2 .
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的阳离子.
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3 .
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子.
-
(1) 过程Ⅰ的目的是.
-
(2) 棉花中浸润的溶液为.作用是
-
(3) A中发生反应的化学方程式.
-
(4) 导致步骤Ⅲ中溶液变黄的离子反应是.用(写试剂化学式)检验氧化产物,现象是.
-
(5) 能说明氧化性Fe3+>SO2的离子方程式是.
-
(6) 甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是(填“甲”“乙”“丙”).
过程ⅣB溶液中含有的离子
过程ⅥB溶液中含有的离子
甲
有Fe3+无Fe2+
有SO42﹣
乙
既有Fe3+又有Fe2+
有SO42﹣
丙
有Fe3+无Fe2+
有Fe2+
实验编号 | 实验操作 | 实验现象 |
Ⅰ |
| ⅰ.溶液变为浅黄色 ⅱ.溶液变蓝 |
Ⅱ |
| ⅰ.溶液保持无色 ⅱ.溶液不变蓝,溶液的pH=10 |
【资料】:碘的化合物主要以I−和IO3−的形式存在。酸性条件下IO3−不能氧化Cl− , 可以氧化I−。ClO−在pH<4并加热的条件下极不稳定。
-
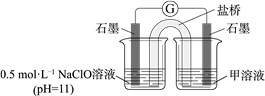
(1) 0.5 mol·L−1 NaClO溶液的pH=11,用离子方程式表示其原因:。
-
(2) 实验Ⅰ中溶液变为浅黄色的离子方程式是。
-
(3) 对比实验Ⅰ和Ⅱ,研究实验Ⅱ反应后“溶液不变蓝”的原因。
① 提出假设a:I2在碱性溶液中不能存在。设计实验Ⅲ证实了假设a成立,实验Ⅲ的操作及现象是。
② 进一步提出假设b:NaClO可将I2氧化为IO3−。进行实验证实了假设b成立,装置如下图,其中甲溶液是,实验现象是。
-
(4) 检验实验Ⅱ所得溶液中的IO3−:
取实验Ⅱ所得溶液,滴加稀硫酸至过量,整个过程均未出现蓝色,一段时间后有黄绿色刺激性气味的气体产生,测得溶液的pH=2。再加入KI溶液,溶液变蓝,说明实验Ⅱ所得溶液中存在IO3−。
① 产生的黄绿色气体是。
② 有同学认为此实验不能说明实验Ⅱ所得溶液中存在IO3− , 理由是。欲证明实验Ⅱ所得溶液中存在IO3− , 改进的实验方案是。
③ 实验Ⅱ中反应的离子方程式是。
(实验)
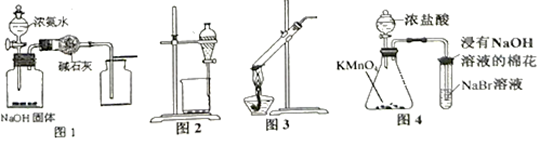
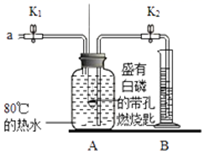
①检查装置的气密性,气密性良好。
②向A瓶中加满80℃热水,将盛有白磷的带孔燃烧匙快速浸没热水中,塞紧瓶塞,白磷不燃烧。
③打开K1、K2 , 从a口向A瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭K1、K2。此时进入量筒B中水的体积为200mL,观察到A瓶中的白磷燃烧。
-
(1) 对比步骤②和③的现象可知,可燃物燃烧的条件之一是;白磷燃烧的反应方程式为。
-
(2) 待装置冷却一段时间后,打开K2 , 如果观察到,说明空气中氧气的体积约占1/5。如何确定此装置气密性良好?(忽略燃烧匙位置漏气情况)。
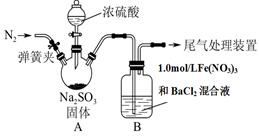
已知:1.0 mol/L的Fe(NO3)3溶液的pH=1。
请回答:
-
(1) 装置A中用于添加浓硫酸的仪器名称为。
-
(2) 实验前鼓入N2的目的是。
-
(3) 装置B中产生了白色沉淀,其成分是,说明SO2具有性。
-
(4) 分析B中产生白色沉淀的原因。
观点1:SO2与Fe3+反应;
观点2:在酸性条件下SO2与NO3-反应;
①若观点1正确,除产生沉淀外,还应观察到的现象是。
②按观点2,装置B中反应的离子方程式是,
③有人认为,如将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验,也可验证观点2是否正确。此时应选择的最佳试剂是(填序号)。
A.1 mol/L稀硝酸
B.1.5 mol/L Fe(NO3)2溶液
C.6.0 mol/L NaNO3溶液和0.2 mol/L盐酸等体积混合的溶液
D.3.0 mol/L NaNO3溶液和0.1mol/L硫酸等体积混合的溶液
| 选项 | 实验操作和现象 | 实验结论 |
| A | 将相同大小的K和Na放入等体积的水中,钾比钠反应剧烈 | 钾元素的金属性比钠元素强 |
| B | 向装有蔗糖的烧杯里滴加浓硫酸,固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| C | 将石蜡油加强热产生的气体通入溴的四氯化碳溶液中,溶液褪色 | 石蜡油分解的产物一定含有乙烯 |
| D | 金属钠分别投入乙醇和水中,钠与水反应更剧烈 | 分子中羟基的活泼性:水>乙醇 |
【提出猜想】CO2与Na反应可能生成4种物质:C、CO、Na2O和Na2CO3。
【查阅资料】向PdCl2溶液中通入CO,能产生黑色沉淀。
【实验过程】同学们在化学老师的指导下设计了如图所示装置(部分夹持仪器已略去)。

-
(1) 实验记录
步骤
实验操作
主要实验现象
实验结论及解释
Ⅰ
打开a,关闭b,由长颈漏斗注入盐酸
A中产生大量气泡,E中出现浑浊
①A中反应的离子方程式为
Ⅱ
当E中出现浑浊时,打开b,关闭a,点燃酒精灯
D中Na剧烈燃烧,产生白烟,内壁附着黑色、白色固体,G中产生黑色沉淀
②反应产物一定有和
Ⅲ
取部分D中白色固体于试管中,加水溶解,再滴加CaCl2溶液
产生白色沉淀
③反应产物还有
-
(2) 实验反思
①B中的试剂是溶液(填化学式)。
②步骤Ⅱ中,E中出现浑浊再点燃酒精灯的目的是。
③该实验需要配制80 mL 0.5 mol/L CaCl2溶液备用,所需要的玻璃仪器除了量筒、烧杯、玻璃棒、胶头滴管外,还有。
④如何确定是否含有Na2O,请简述理由。
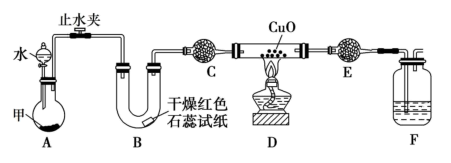
回答下列问题:
-
(1) 检验装置A气密性良好的方法,实验中观察到B中的试纸变为蓝色,则化合物甲的化学式为。
-
(2) 装置C的作用为,F中盛有稀硫酸和四氯化碳,四氯化碳的作用为,F装置中发生化学反应的方程式为。
-
(3) 实验结束后装置D得到紫红色固体,E中无水硫酸铜变蓝,F中有无色无味气体逸出,写出D中发生反应的化学方程式。
A | B | C | D | |
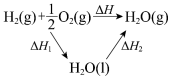
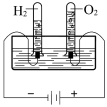
目的 | 探究温度对平衡移动的影响 | 比较元素的非金属性 | 探究△H与反应历程的关系 | 探究气体体积与的分子数的关系 |
实验方案 |
2NO2(g) |
|
|
电解水(添加稀硫酸) |
结果 | 左侧气体颜色加深,右侧气体颜色变浅 | 烧瓶中产生气泡,试管中出现浑浊 | 测得△H=△H1+△H2 | H2与O2的体积比约为2∶1 |
- 解方程x2-4x+1=0
- 两列振幅和波长都相同而传播方向相反的波(如图甲所示),在相遇的某一时刻(如图乙所示),两列波“消失”,此时介质中X、Y两
- 教师节到了,请你拟一条短信祝表达你对老师节日的祝贺,要求至少要用到两种修辞手法。(4分)
- 东晋建立初,江南出现了“荆扬晏安,户口殷实”的局面,其最主要的原因是 A.东晋采取抵抗政策,阻止了北方少数民族军队南下
- 《大自然的语言》节选(18分)①几千年来,劳动人民注意了草木荣枯、候鸟去来等自然现象同气候的关系,据以安排农事。②杏花开
- △ABC中,点D是边BC延长线上一点,,则____度.
- 下列各组物质的俗称、学名与化学式表示同一物质的是() A.干冰 水 H2O B.酒精 乙醇
- 小红从小有个梦想。到祖国宝岛台湾去欣赏秀丽风景。领略风土人情。2009年春节,她终于乘上了厦门直飞台北的航班,实现了自己
- 神经冲动在两个神经元之间传递时,以下生理活动不会发生的是A.生物膜的融合和转化 B.离子通道的开放和关闭 C.AT
- There was a big fire yesterday. ______ no one was hurt. A.
- 阅读下文,完成小题(共27分)要不要叫醒她张曼娟(台湾) (1)要不要叫醒她? (2)她睡得好熟呢。 (3)还是叫起来吧
- 如下图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在
- 同学在做电学实验时,不慎将电压表和电流表的位置对换,如图。若开关闭合其后果是( )A.两表会被烧坏B.两表不会被烧
- 阅读下面文章,做1—5题。 抽打心中的樱桃花 ①年少时家中的院子里种了两棵樱桃树。每年春天,樱桃树上总会挂满红得
- 某同学在研究性学习中,收集到某制药厂车间工人数(单位:十人)与药品产量(单位:万盒)的数据如表所示:工人数:x(单位:十
- (二) 用所学过的短语替换下列各句中的下划线部分,每空一词。(每小题1分,共10分) 1. A: It’s bad ma
- 阅读下面的文字,完成17~21题。生命的化妆林清玄①我认识一位化妆师。她是真正懂得化妆,而又以化妆闻名的。②对于这生活在
- 以下为沿海开放区的有() A.海南 B.深圳 C.长江三角洲 D.上海
- — How about your journey to Shanghai? —Everything was wo
- α是第二象限角,为其终边上一点,且,则的值为 ( ) A. B.


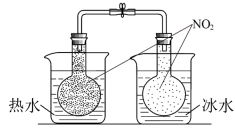
 N2O4(g) △H<0
N2O4(g) △H<0